Clear Sky Science · fr
Escherichia coli favorise les métastases du cancer colorectal en maintenant les boucles enhancheur‑promoteur via la libération de filets extracellulaires de neutrophiles
Les microbes intestinaux et l’autoroute secrète du cancer
Le cancer colorectal tue souvent non pas à cause de la tumeur initiale dans l’intestin, mais parce que des cellules cancéreuses migrent vers le foie et s’y implantent. Cette étude révèle un complice inattendu de ce voyage : une bactérie intestinale commune, Escherichia coli. En suivant la chaîne d’événements depuis les bactéries de l’intestin jusqu’aux tumeurs agressives du foie, les chercheurs montrent comment microbes, cellules immunitaires et architecture de l’ADN à l’intérieur des cellules cancéreuses peuvent agir de concert pour alimenter les métastases — et suggèrent de nouvelles façons de rompre cette chaîne.
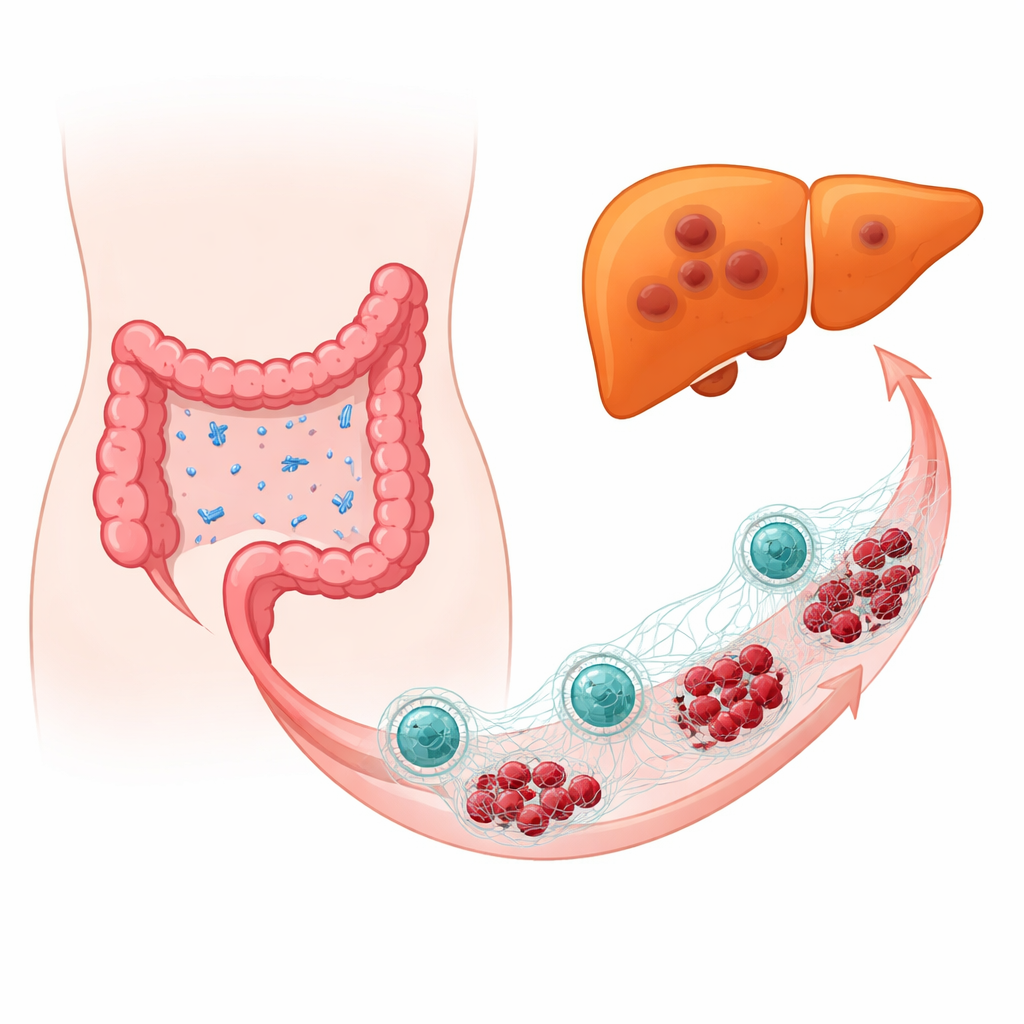
Quand des bactéries amies deviennent hostiles
L’équipe a examiné des échantillons tumoraux de personnes atteintes d’un cancer colorectal, en comparant celles dont le cancer s’était propagé au foie à celles dont il ne l’avait pas fait. Grâce à un profilage microbien basé sur l’ADN à haute résolution, ils ont constaté qu’E. coli était beaucoup plus abondante dans les cancers qui avaient déjà colonisé le foie. Chez la souris et dans des modèles murins à système immunitaire humanisé, l’introduction délibérée d’E. coli à proximité des tumeurs colorectales a augmenté la taille et la fréquence des métastases hépatiques et a poussé les cellules tumorales vers un état plus mobile et invasif. Même lorsque la plupart de la flore intestinale normale avait été éliminée par des antibiotiques et qu’E. coli seule avait été réintroduite, la bactérie favorisait toujours la croissance et la dissémination tumorales, impliquant E. coli elle‑même plutôt qu’une perturbation générale du microbiote.
Des filets immunitaires qui aident le cancer à s’échapper
Les neutrophiles — cellules immunitaires de première ligne qui emprisonnent et tuent normalement les microbes — se sont révélés des intermédiaires cruciaux. En réponse à E. coli, les neutrophiles libèrent des structures en forme de filet appelées filets extracellulaires, composées d’ADN et de protéines toxiques. Ces filets sont destinés à capturer les bactéries, mais, dans ce contexte, ils protègent et renforcent involontairement les cellules cancéreuses. Lorsque les chercheurs dégradèrent ces filets avec des enzymes ou bloquèrent des enzymes clés nécessaires à leur formation, les métastases hépatiques diminuèrent et les tumeurs devinrent moins agressives. L’épuisement des neutrophiles produisit un effet protecteur similaire, soulignant un paradoxe : la même réponse immunitaire qui combat l’infection est détournée pour aider la dissémination du cancer.
Des signaux électriques aux interrupteurs génétiques
Comment des filets d’ADN collants à l’extérieur d’une cellule tumorale peuvent‑ils modifier ce qui se passe au cœur de son noyau ? La réponse réside dans le calcium, un ion simple qui sert de signal électrique dans les cellules. L’étude montre que les filets de neutrophiles augmentent le niveau d’une protéine canal, TRPC1, à la surface des cellules du cancer colorectal. TRPC1 laisse entrer du calcium supplémentaire dans la cellule, ce qui active à son tour un régulateur sensible au calcium appelé NFATC3 et crée une boucle auto‑entretenue maintenant des niveaux élevés de TRPC1. Cette montée de calcium favorise l’association de deux petites protéines, S100A8 et S100A9, qui se lient ensuite à une protéine de contrôle de croissance majeure, STAT3. Le trio migre vers le noyau où il réalise quelque chose d’assez frappant : il aide à plier et à boucler l’ADN de façon à rapprocher physiquement des régions régulatrices distantes et des sites de démarrage des gènes, stabilisant ainsi des « boucles enhancheur–promoteur » qui augmentent l’expression de certains gènes.
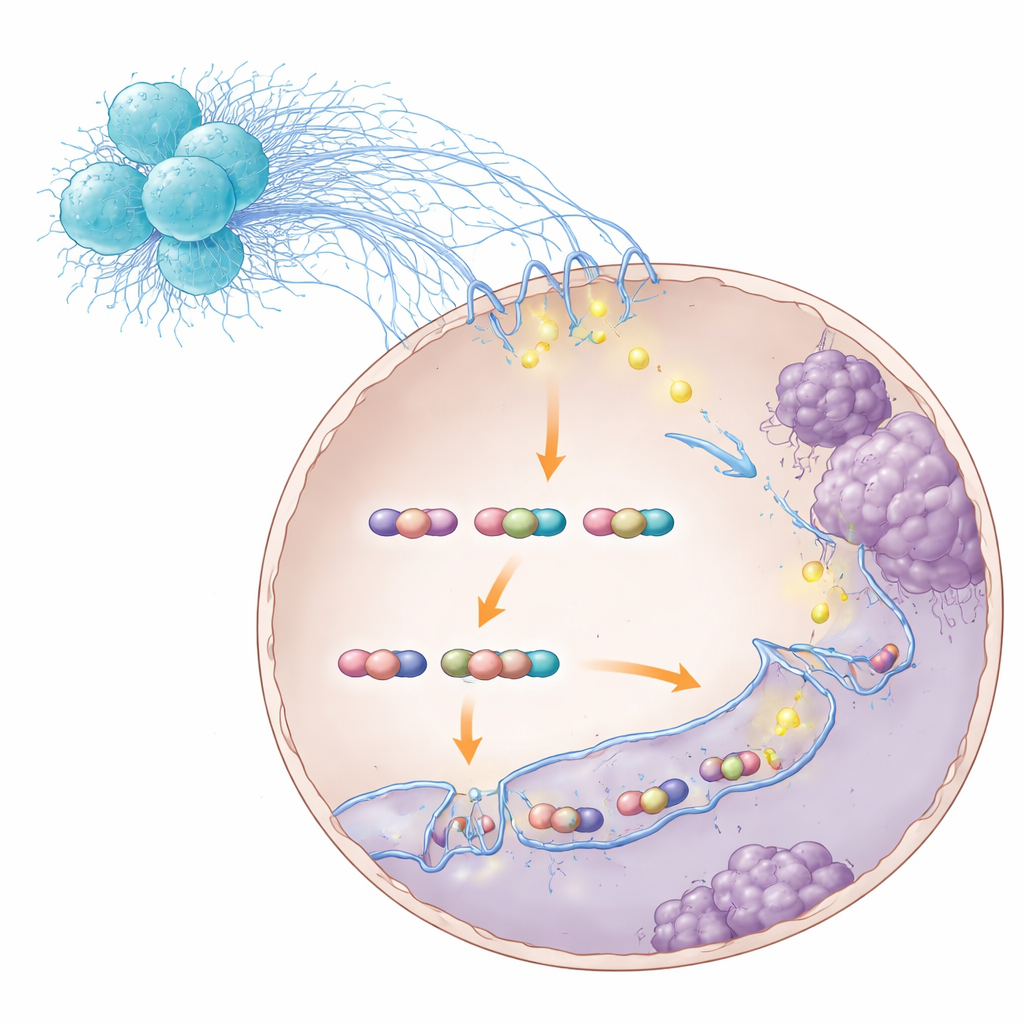
Recâbler les cellules cancéreuses pour la métastase
En cartographiant les contacts tridimensionnels le long du génome, les chercheurs ont constaté que le complexe STAT3–S100A8/9 favorisait des boucles qui stimulent l’expression de gènes impliqués dans le mouvement et l’invasion cellulaires. Un gène remarquable était TNS1, qui pousse les cellules à relâcher leurs attaches et à migrer plus facilement. Lorsque le complexe STAT3–S100A8/9 était perturbé, nombre de ces boucles s’affaiblissaient ou disparaissaient, les niveaux de TNS1 chutaient et les cellules cancéreuses perdaient une partie de leur capacité d’invasion et d’ensemencement hépatique. Il est important de noter que cette perturbation n’empêchait pas STAT3 d’interagir avec l’ADN dans l’absolu — elle déstabilisait spécifiquement l’architecture en boucle qui suralimente les programmes métastatiques. Dans des modèles animaux, le blocage de différentes étapes de cette chaîne — depuis la molécule de détection bactérienne RIPK2 dans les neutrophiles, jusqu’à S100A8/9, puis STAT3 lui‑même — réduisait les métastases hépatiques et améliorait la survie.
Rompre la chaîne entre microbes et tumeurs
Pour les non‑spécialistes, le message clé est qu’une bactérie intestinale commune peut favoriser la propagation du cancer colorectal en provoquant d’abord les cellules immunitaires à lancer des filets d’ADN, puis en utilisant ces filets pour déclencher une cascade alimentée par le calcium qui recâble la manière dont les gènes cancéreux sont activés. Plutôt que de recourir à des antibiotiques à large spectre, qui peuvent nuire aux microbes bénéfiques et affaiblir l’immunothérapie anticancéreuse, ce travail met en lumière des cibles médicamenteuses plus précises : des capteurs bactériens comme RIPK2, la cascade TRPC1–calcium–S100A8/9, et les boucles d’ADN pilotées par STAT3 qui verrouillent les gènes liés à la métastase en position active. Interrompre cette chaîne à un ou plusieurs niveaux pourrait offrir une nouvelle stratégie pour empêcher le cancer colorectal de transformer un problème local dans l’intestin en une maladie mortelle au foie.
Citation: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Mots-clés: métastases du cancer colorectal, microbiote intestinal, filets extracellulaires de neutrophiles, signalisation STAT3, régulation épigénétique des gènes