Clear Sky Science · fr
La conception d’inhibiteurs covalents confère une activité contre les formes liées au GDP et au GTP de KRAS G12C
Pourquoi cela compte pour les traitements contre le cancer à venir
Les cancers pilotés par des mutations du gène KRAS ont longtemps été considérés comme parmi les plus difficiles à traiter. Récemment, de nouveaux médicaments qui neutralisent une forme mutante courante, KRAS G12C, ont été mis à la disposition des patients et ont commencé à modifier cette donne. Cet article explore une idée encore plus ambitieuse : peut‑on concevoir des médicaments qui bloquent KRAS G12C dans ses deux principaux modes de fonctionnement à l’intérieur de la cellule, et cela rendrait‑il le traitement du cancer plus rapide, plus puissant ou plus durable ?
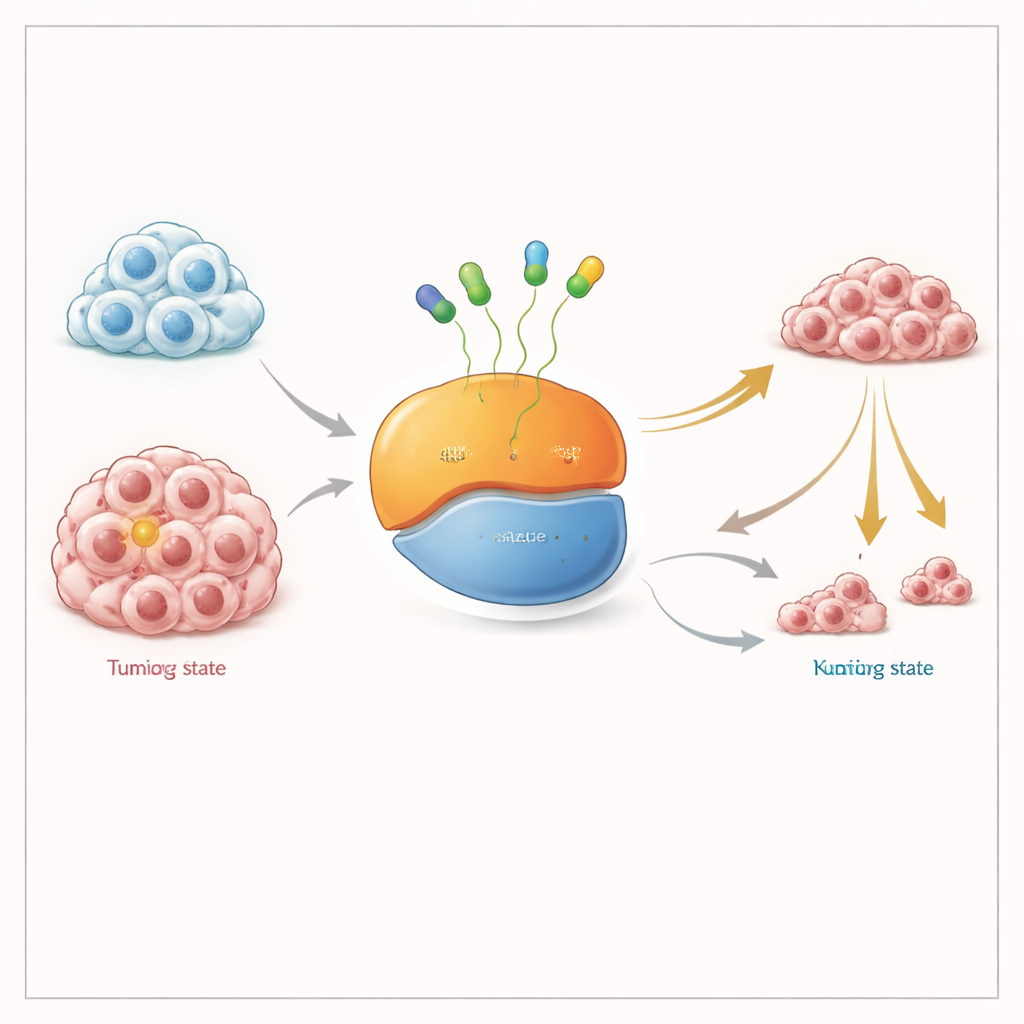
Éteindre un interrupteur moléculaire à deux positions
KRAS agit comme un petit interrupteur marche‑arrêt pour les signaux de croissance cellulaire. Il bascule entre un état « éteint », où il porte une molécule d’énergie appelée GDP, et un état « allumé », où il porte une autre molécule, le GTP. La mutation KRAS G12C maintient cet interrupteur partiellement activé et alimente la croissance tumorale. Les médicaments existants approuvés par la FDA se fixent à la forme « éteinte » et la verrouillent ; au fil du temps, à mesure que davantage de KRAS passent par cette forme, la totalité du pool de protéines mutantes est neutralisée. De nombreux chercheurs ont soutenu qu’un médicament capable d’attraper KRAS dans ses formes allumée et éteinte devrait mieux fonctionner, en particulier dans les tumeurs qui s’adaptent en maintenant plus de KRAS à l’état actif.
Concevoir un nouveau type d’hameçon moléculaire
Les auteurs se sont attelés à concevoir de tels médicaments à double usage. Ils se sont concentrés sur une petite gorge proche d’une région flexible de KRAS appelée Switch II, où les médicaments actuels se lient déjà. Au lieu de modifier l’affinité de leurs molécules pour cette gorge, ils ont réingénieré la partie « warhead » qui forme une liaison chimique permanente avec la cystéine mutante en position 12. Grâce à la modélisation informatique et à la synthèse de dizaines de variantes, ils ont découvert une warhead spéciale en trois parties qui aborde la cystéine sous un angle légèrement différent. Ce déplacement subtil crée suffisamment d’espace pour la molécule de GTP plus volumineuse, permettant aux nouveaux composés de se lier à KRAS qu’il porte du GDP ou du GTP. Des tests biochimiques ont confirmé que les composés principaux pouvaient perturber le partenariat de KRAS avec un partenaire clé de signalisation, RAF, dans les deux états.
Voir comment la protéine se reconfigure
Pour comprendre pourquoi ces molécules fonctionnaient, l’équipe a déterminé des structures cristallographiques à haute résolution du médicament lié à KRAS. Ces clichés ont montré que la nouvelle warhead réagit à un site inhabituel sur l’échafaudage chimique, en libérant un atome de fluor et en formant une liaison covalente sur un carbone différent de celui des médicaments anticancéreux typiques ciblant les cystéines. Cette chimie modifiée aide le médicament à s’insérer dans la poche Switch II même lorsque le GTP est présent. Les structures ont également révélé que, lorsque l’inhibiteur se lie, il déplace une minuscule molécule d’eau et réarrange subtilement une autre boucle, Switch I, qui contacte normalement les protéines de signalisation en aval. Cette remodelage « allostérique » rapproche deux acides aminés pour former un pont salin serré, déformant la surface de sorte que RAF ne peut plus s’ancrer et transmettre les signaux de croissance.
Arrêt rapide, mais pas d’effet à long terme supérieur
Armés de ces informations structurales, les chercheurs ont affiné deux molécules principales qui se lient efficacement et sélectivement à KRAS G12C, tout en épargnant en grande partie d’autres protéines contenant des cystéines. Dans des lignées cellulaires cancéreuses, ces inhibiteurs à double état ont rapidement bloqué un relais de signalisation clé connu sous le nom de voie MAPK, comme mesuré par la perte d’un marquage chimique sur la protéine ERK et une forte suppression de la croissance cellulaire. Ils ont inactivé KRAS dans les cellules plus rapidement qu’un médicament de référence qui ne cible que l’état inactif. Dans des modèles tumoraux murins, un composé principal a montré une bonne disponibilité orale, a rapidement formé des liaisons covalentes avec la cible et a réduit la taille des tumeurs ou ralenti leur croissance. Néanmoins, lorsque l’équipe a comparé à plus long terme les inhibiteurs à double état et ceux ciblant l’état inactif, les deux classes ont fini par atteindre des niveaux similaires de neutralisation de KRAS, d’inhibition de la voie et de contrôle tumoral.
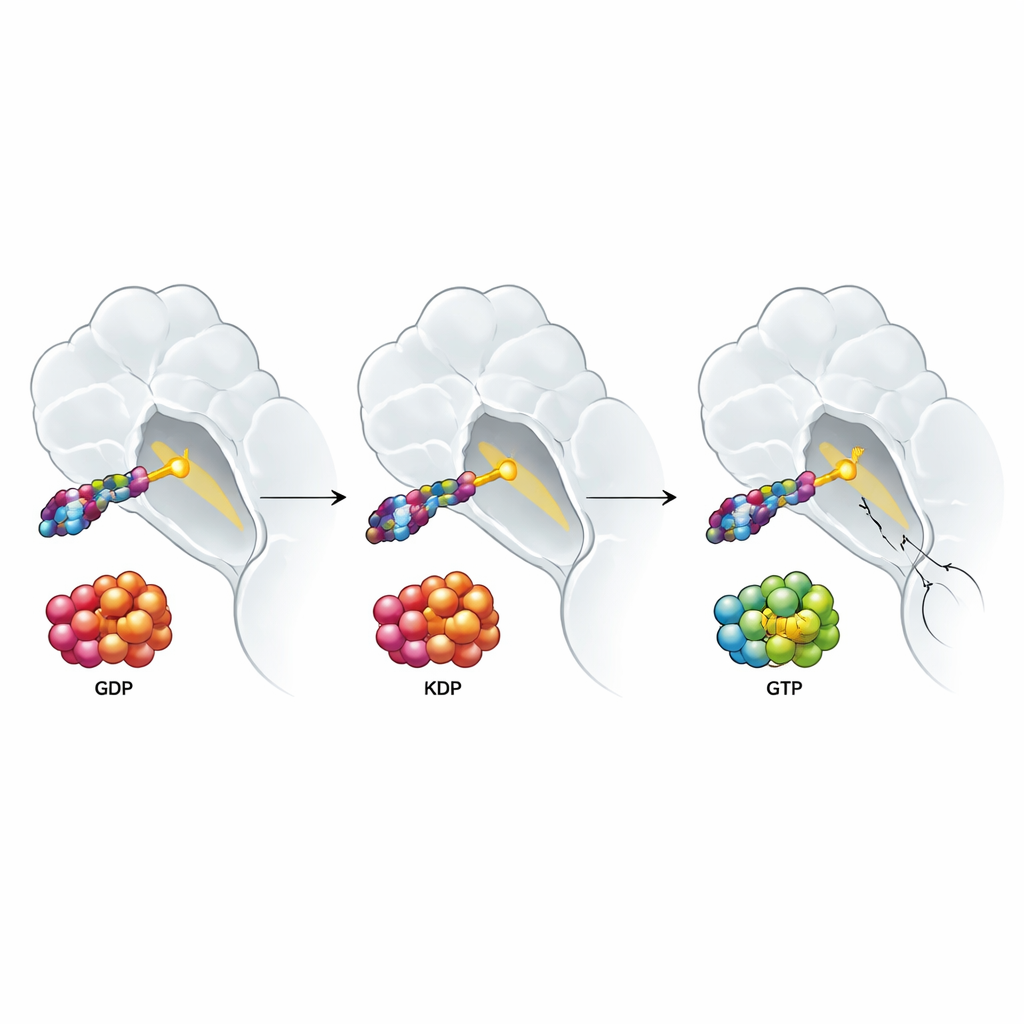
Pourquoi les signaux de croissance de l’environnement tumoral l’emportent encore
L’étude a également examiné comment les signaux provenant de l’environnement tumoral affectent ces médicaments. Des facteurs de croissance tels que l’EGF et le HGF, abondants autour de nombreuses tumeurs, poussent les protéines RAS vers la forme active chargée en GTP et sont connus pour atténuer les réponses aux thérapies ciblées. On pourrait s’attendre à ce qu’un médicament qui se lie à la forme active de KRAS G12C contourne ce problème. Au lieu de cela, les auteurs ont constaté que les inhibiteurs à double état et ceux ciblant l’état inactif perdaient tous deux en puissance en présence de ces facteurs de croissance. Des expériences détaillées ont identifié un coupable surprenant : l’activation des formes normales non mutées de RAS (H‑RAS et N‑RAS), qui peuvent contourner KRAS G12C et maintenir la transmission des signaux de croissance. Lorsque les chercheurs ont supprimé H‑RAS et N‑RAS dans une lignée cellulaire de cancer du poumon, la résistance induite par les facteurs de croissance a en grande partie disparu pour tous les types de médicaments ciblant KRAS G12C, alors qu’un médicament bloquant une étape en aval de la voie était moins affecté dès le départ.
Ce que cela signifie pour les patients et le développement de médicaments
Dans l’ensemble, ce travail démontre qu’il est chimiquement et structurellement faisable de concevoir des médicaments covalents contre KRAS G12C qui saisissent la protéine dans ses états actif et inactif, et que ces inhibiteurs à double état peuvent arrêter la signalisation plus rapidement que les médicaments existants. Cependant, cet engagement rapide ne s’est pas traduit par un contrôle tumoral clairement supérieur ni par une solution à la résistance induite par les facteurs de croissance dans des modèles précliniques. Pour les patients, cela suggère que simplement ajouter une activité contre la forme active de KRAS peut ne pas suffire ; des stratégies en combinaison ciblant également d’autres membres de la famille RAS ou des nœuds de signalisation en aval pourraient être nécessaires. La nouvelle warhead et le plan structural présentés ici élargissent néanmoins la boîte à outils pour cibler KRAS et informeront les générations futures de thérapies de précision contre le cancer.
Citation: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
Mots-clés: KRAS G12C, inhibiteur covalent, inhibition à double état, signalisation MAPK, résistance aux médicaments