Clear Sky Science · fr
Coloration chimique pour des études fondamentales et l’optimisation des liants dans les électrodes négatives des batteries Li‑ion
Voir la colle cachée à l’intérieur des batteries
Les batteries lithium‑ion alimentent nos téléphones, nos voitures et bientôt des quartiers entiers, pourtant un ingrédient crucial à l’intérieur reste presque invisible : le liant, un fin « colle » polymère qui maintient les particules ensemble. Cet article présente une nouvelle méthode pour « teindre » chimiquement cette colle cachée afin qu’elle apparaisse au microscope électronique. En voyant enfin où le liant se trouve réellement, les auteurs montrent comment fabriquer des batteries plus durables, plus rapides à charger et améliorer des procédés industriels qui reposent aujourd’hui sur l’essai‑erreur.
Pourquoi l’emplacement du liant compte
Dans une électrode négative typique, plus de 95 % du volume est constitué de matériau actif comme le graphite ; moins de 5 % sont le liant et le carbone conducteur qui assurent la résistance mécanique et les voies électriques. Malgré cette fraction minime, la distribution spatiale du liant influence fortement l’adhésion des particules entre elles et au collecteur de courant métallique, la facilité de déplacement des électrons et des ions, et la stabilité des couches de surface pendant le cyclage. Jusqu’à présent, cartographier l’emplacement des liants hydrosolubles dans des électrodes commerciales en graphite ou en graphite‑silicium était extrêmement difficile, si bien que les ingénieurs modifiaient surtout la chimie du liant plutôt que sa répartition.
Faire briller le liant invisible
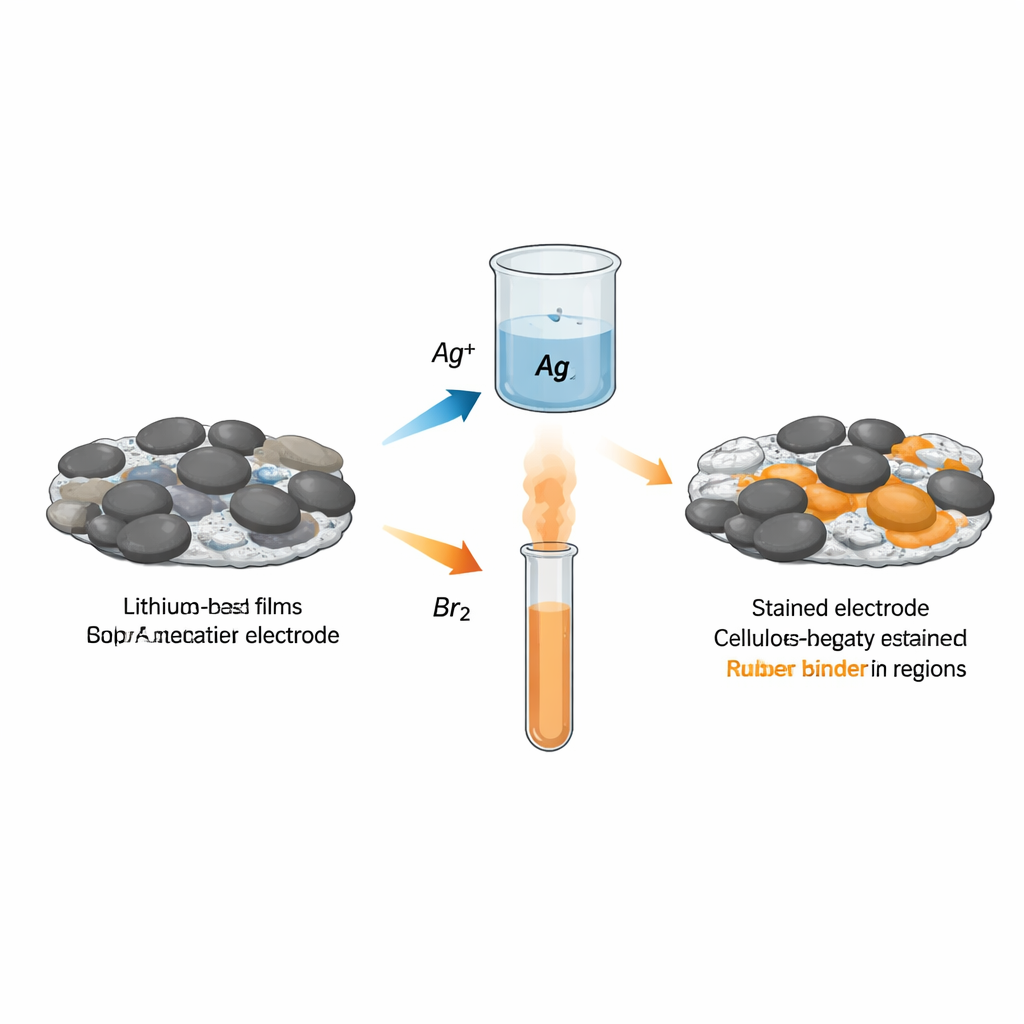
Les auteurs présentent deux colorants chimiques simples adaptés aux liants à traitement aqueux les plus utilisés : la carboxyméthyl cellulose (CMC) et le caoutchouc styrène‑butadiène (SBR). L’immersion d’une électrode dans une solution de nitrate d’argent provoque la fixation sélective d’ions argent sur les groupes acides de la CMC, tandis que l’exposition à la vapeur de brome ajoute des atomes de brome aux doubles liaisons carbone‑carbone du SBR. Ces atomes d’argent ou de brome ajoutés sont suffisamment lourds pour ressortir en imagerie par électrons rétrodiffusés et peuvent être précisément mesurés par spectroscopie X. Des tests sur des films de liant purs et sur des électrodes mixtes confirment que l’argent marque la CMC et le brome marque le SBR avec une bonne spécificité et sensibilité aux teneurs en liant rencontrées en pratique.
Révéler des films cachés et des structures fragiles
Avec les électrodes teintées en main, l’équipe a utilisé l’imagerie électronique avancée pour explorer l’organisation du liant à plusieurs échelles. À l’échelle micrométrique, ils ont identifié différents types d’agrégats riches en liant : certains dominés par le carbone conducteur et la CMC qui favorisent la percolation électronique, d’autres plus riches en SBR élastique qui apportent de la souplesse. À l’échelle nanométrique, la coloration à l’argent a révélé un film ultra‑fin d’environ 10–15 nanomètres de CMC qui enrobe de manière conforme les particules de graphite dans des électrodes fraîches non comprimées. Ce revêtement continu avait longtemps été théorisé mais rarement observé directement. Fait marquant, le calandrage industriel (l’étape de laminage à chaud utilisée pour densifier les électrodes) a brisé ce film fragile en patchs dispersés, laissant de larges zones de graphite à nu dans des échantillons de laboratoire et commerciaux. Cette hétérogénéité modifie probablement les endroits où les ions peuvent entrer, où se forment les couches protectrices de surface, et où peut débuter un dépôt délétère de lithium.
Transformer les images en meilleures pratiques de fabrication
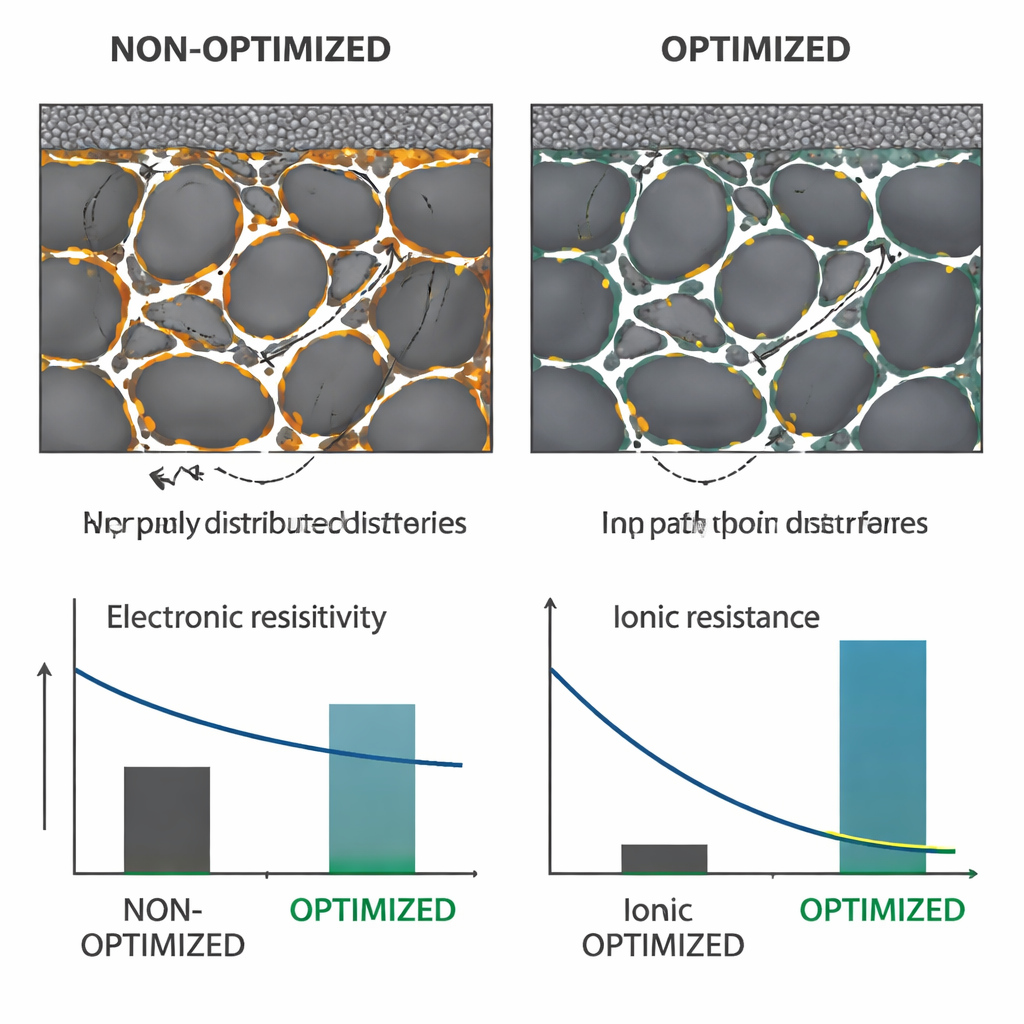
Parce que les liants teintés sont maintenant mesurables, les auteurs ont pu relier microstructure, performances et choix de procédés. En ajustant la manière de mélanger la pâte—plus précisément en commençant par une solution de CMC plus concentrée—ils ont fortement réduit la formation de gros agrégats carbone‑liant sans changer la recette globale. Cela a conduit à une diminution mesurable de 14 % de la résistivité électronique du revêtement de graphite. Dans une seconde étude, ils ont utilisé la coloration pour suivre la migration du liant lors d’un séchage rapide à haute température, un goulot d’étranglement clé sur les lignes de revêtement industrielles. Une simple étape de « inversion de phase »—tremper brièvement le revêtement humide dans de l’acétone avant le séchage—a poussé davantage de liant vers le collecteur de courant plutôt que vers la surface supérieure. Les électrodes obtenues se pliaient sans se fissurer, adhéraient mieux et présentaient environ 40 % de résistance ionique plus faible à travers leurs pores, le tout sans modifier l’épaisseur, la porosité ou la composition.
Limites, opportunités et implications pour les batteries
La méthode de coloration n’est pas universelle : des matériaux hautement réactifs comme le nano‑silicium ou le phosphate de fer lithié peuvent interférer avec la chimie, et l’argent ou le brome doivent être appliqués sur des échantillons tests, pas sur des cellules en fonctionnement. Néanmoins, l’approche fonctionne bien pour les liants aqueux dominants dans les anodes au graphite et dans de nombreux anodes contenant du silicium, en n’exigeant qu’un équipement de laboratoire modeste. Pour les non‑spécialistes, la conclusion essentielle est que la façon dont la « colle » à l’intérieur d’une électrode est disposée—jusqu’à l’échelle de dizaines de nanomètres—peut influencer significativement la puissance, la durée de vie et la sécurité. En donnant aux fabricants une image claire de la localisation du liant, ce travail ouvre des voies pratiques vers un séchage plus rapide, une meilleure robustesse mécanique et une distribution de courant plus uniforme, contribuant in fine à des batteries lithium‑ion plus fiables et plus efficaces.
Citation: Zankowski, S.P., Wheeler, S., Barthelay, T. et al. Chemical staining for fundamental studies and optimization of binders in Li-ion battery negative electrodes. Nat Commun 17, 1438 (2026). https://doi.org/10.1038/s41467-026-69002-1
Mots-clés: batteries lithium‑ion, liants d’électrode, anodes en graphite, microscopie électronique, fabrication de batteries