Clear Sky Science · fr
Un circuit basalo-préfrontal-thalamique défini au niveau moléculaire régule les dimensions sensorielles et affectives de la douleur chez la souris mâle
Pourquoi ce circuit cérébral compte pour la douleur
La douleur n’est pas qu’une piqûre aiguë ou une douleur sourde ; elle comporte aussi une dimension émotionnelle et peut remodeler notre humeur et notre comportement pendant des années. De nombreux patients souffrant de douleurs chroniques trouvent peu de soulagement avec les médicaments actuels et subissent souvent des effets secondaires importants. Cette étude chez la souris mâle met au jour un circuit cérébral précisément défini qui permet au cerveau d’amplifier ou d’atténuer la douleur, tant en intensité qu’en caractère désagréable. En cartographiant et en contrôlant cette voie, les travaux ouvrent la voie à des approches plus ciblées pour soulager la douleur chronique sans s’appuyer uniquement sur les analgésiques traditionnels.
Une autoroute cachée du cerveau pensant vers le centre de la douleur
Les chercheurs se sont concentrés sur le cortex préfrontal médial, une région frontale impliquée dans la prise de décision, l’émotion et le contrôle de la douleur, et sur le thalamus, un centre relais profond qui module à la fois l’intensité et le caractère pénible de la douleur. Ils ont découvert qu’un groupe spécifique de cellules du cortex préfrontal médial, marqué par le gène Foxp2, forme une voie de sortie majeure vers le thalamus. Ces cellules se trouvent principalement dans la couche corticale la plus profonde et envoient de longues fibres vers des noyaux thalamiques particuliers, tout en négligeant en grande partie d’autres cibles typiques du préfrontal. Grâce à des méthodes de traçage et à une cartographie cérébrale globale, l’équipe a montré que ces neurones marqués par Foxp2 se connectent fortement à trois régions thalamiques connues pour influencer le traitement de la douleur : le noyau parataénial, le thalamus médiodorsal et le thalamus ventromédial. 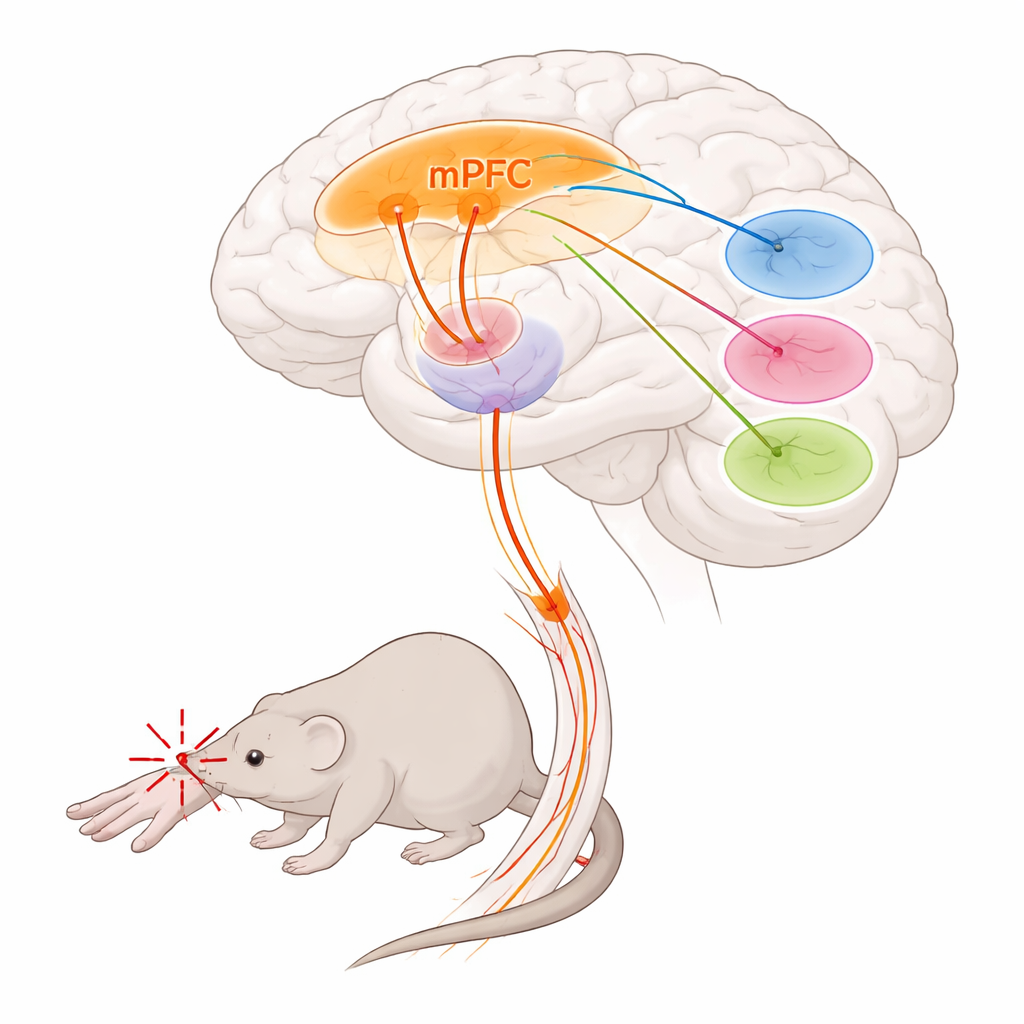
Lorsque la douleur survient, un centre de contrôle clé se tait
Pour observer le comportement de cette voie pendant la douleur, les scientifiques ont implanté de minuscules lentilles au‑dessus du cortex préfrontal médial et enregistré l’activité de neurones individuels marqués par Foxp2 chez des souris éveillées. Lors de pincements mécaniques brefs, de douleurs chimiques induites par la formaline et de douleurs inflammatoires durables, ces cellules se sont systématiquement mises au repos : la plupart présentaient moins d’épisodes d’activité pendant les épisodes douloureux et dans les jours suivant la lésion inflammatoire. Cette extinction n’était pas ténue ; dans certaines conditions, plus d’un tiers à près de la moitié des cellules devenaient nettement moins actives. Cette observation suggère que les états de douleur aigüe et chronique reflètent en partie le silence d’un système préfrontal de freinage naturel qui, autrement, aiderait à maintenir la douleur sous contrôle.
Allumer et éteindre le circuit modifie la douleur
L’équipe a ensuite cherché à savoir si cet arrêt était un simple effet secondaire de la douleur ou un mécanisme causal. À l’aide d’outils génétiques, ils ont soit bloqué de façon durable la sortie des neurones marqués par Foxp2, soit stimulé brièvement leur activité. L’inactivation persistante a rendu les souris plus sensibles au toucher et à la chaleur, indiquant que cette voie restreint normalement les signaux douloureux entrants. En revanche, une activation de courte durée a élevé le seuil des stimulations douloureuses, réduit le léchage en phase tardive dans le test à la formaline (une mesure de la douleur inflammatoire persistante) et poussé les souris à préférer des environnements où le circuit avait été activé, signe d’un soulagement du fardeau émotionnel de la douleur. En éclairant des branches spécifiques de la voie, les chercheurs ont montré que les projections vers le thalamus parataénial réduisent à la fois la sensibilité physique et les réponses d’adaptation, tandis que les projections vers les thalamus médiodorsal et ventromédial règlent principalement les dimensions émotionnelles et comportementales. Ensemble, ces résultats révèlent un câblage finement séparé dans lequel différentes branches d’une même population préfrontale contrôlent différentes facettes de l’expérience douloureuse.
Ajustement chimique : un renfort cholinergique pour soulager la douleur
Qu’est‑ce qui commande ces neurones préfrontaux de soulagement de la douleur ? Des expériences de traçage ont mis en évidence un fort apport d’une région cholinergique du prosencéphale basal appelée bande diagonale horizontale. Nombre des cellules envoyant des signaux depuis cette zone vers les neurones marqués par Foxp2 utilisent l’acétylcholine, un messager impliqué dans l’attention et l’éveil. L’activation de cette projection cholinergique a réduit la sensibilité mécanique et les comportements d’adaptation et a atténué l’hypersensibilité inflammatoire, bien qu’elle n’ait pas modifié de façon nette la tonalité émotionnelle négative de la douleur. Du côté des récepteurs, les neurones marqués par Foxp2 se sont révélés enrichis pour un type particulier de récepteur à l’acétylcholine, connu sous le nom de récepteur nicotinique α4β2. L’administration directe d’un agoniste sélectif α4β2 dans le cortex préfrontal médial a rendu les souris moins sensibles à la chaleur et au toucher douloureux, même dans des états inflammatoires chroniques, et a augmenté l’activité des neurones marqués par Foxp2. Le blocage de ces neurones a annulé l’effet bénéfique du médicament, montrant que ce récepteur soulage la douleur spécifiquement en excitant ce type cellulaire. 
Ce que cela signifie pour les futurs traitements de la douleur
Concrètement, l’étude identifie une voie en trois étapes précise : une région cholinergique « déclencheuse » dans le prosencéphale basal, un ensemble spécialisé de cellules de contrôle dans le cortex préfrontal médial, et des relais distincts dans le thalamus qui gouvernent séparément l’intensité ressentie de la douleur, son impact émotionnel et nos réactions. La douleur semble réduire l’activité de ce circuit ; le réactiver, soit par stimulation directe soit en ciblant ses récepteurs à l’acétylcholine, atténue à la fois la piqûre et la détresse de la douleur inflammatoire chez la souris mâle. Bien que de nombreux travaux restent nécessaires pour traduire ces conclusions à l’homme et à d’autres formes de douleurs chroniques, les résultats soulignent une stratégie prometteuse : au lieu d’engourdir toute sensation, les traitements futurs pourraient restaurer ou affiner les circuits naturels de soulagement de la douleur du cerveau pour une thérapie à long terme plus efficace et potentiellement plus sûre.
Citation: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
Mots-clés: douleur chronique, cortex préfrontal médial, thalamus, signalisation cholinergique, récepteurs nicotiniques