Clear Sky Science · fr
Modification covalente d’un acide glutamique inspirée par la technologie HaloTag
Transformer des « ancres » protéiques en cibles médicamenteuses
Beaucoup de médicaments anticancéreux modernes agissent en s’accrochant à des protéines à l’intérieur de nos cellules. Mais certaines des protéines les plus importantes n’offrent pas de « poignées » faciles pour les médicaments. Cette étude présente une astuce chimique ingénieuse, inspirée d’un outil de laboratoire populaire appelé HaloTag, pour se fixer sur un site normalement difficile d’accès d’une protéine qui contrôle des signaux de croissance pertinents en oncologie. Ce travail pourrait ouvrir de nouvelles voies pour des médicaments qui éteignent de manière plus durable des voies conduisant les tumeurs.
Pourquoi la plupart des médicaments covalents visent le même résidu
Ces dernières années, les médicaments covalents « ciblés » sont devenus une classe prometteuse. Ils portent un groupe chimique légèrement réactif qui forme une liaison permanente avec un acide aminé spécifique d’une protéine, verrouillant ainsi le médicament sur sa cible. Presque tous ces médicaments s’attaquent à la cystéine, un acide aminé relativement rare mais très réactif. En revanche, deux autres acides aminés — l’aspartate et le glutamate — sont beaucoup plus fréquents et souvent cruciaux pour la conformation et la fonction d’une protéine, mais leurs groupes carboxylates acides sont beaucoup moins réactifs dans l’environnement aqueux de la cellule. Cela rend leur modification sélective difficile, et avant ce travail seuls quelques exemples réussis d’inhibiteurs covalents ciblant le glutamate ou l’aspartate existaient.
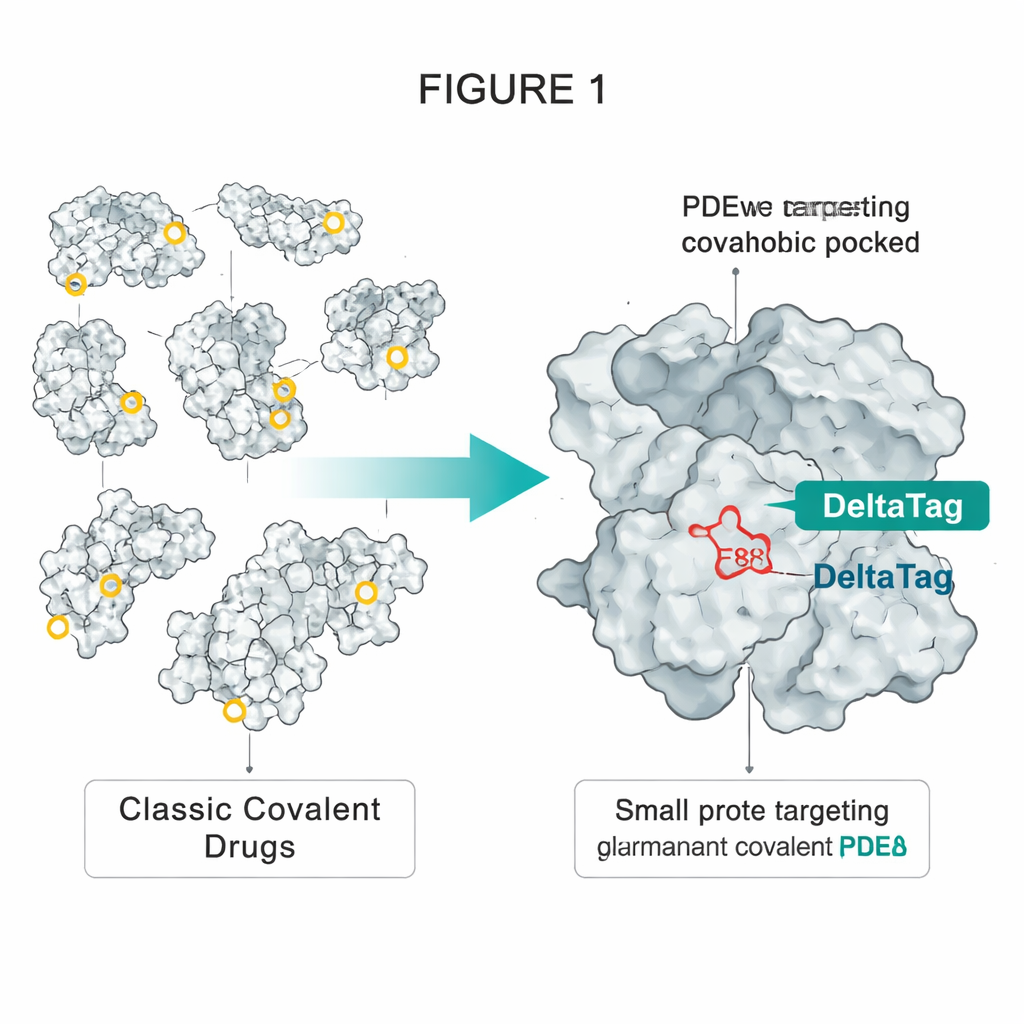
Emprunter une astuce à la technologie HaloTag
Les auteurs se sont inspirés de HaloTag, une protéine modifiée largement utilisée qui peut être marquée de façon permanente par des colorants fluorescents. Dans HaloTag, un aspartate placé en profondeur dans une poche hydrophobe réagit avec une simple chaîne chloroalcanes du colorant, formant une liaison ester stable. L’équipe a remarqué qu’une autre protéine, PDEδ, possède une poche hydrophobe assez similaire contenant un glutamate accessible unique, appelé E88. PDEδ transporte des protéines de signalisation modifiées par lipides, comme la petite GTPase Rheb, à travers la cellule, les aidant à atteindre les membranes où des complexes promoteurs de croissance tels que mTORC1 sont activés. Des inhibiteurs non covalents antérieurs de PDEδ pouvaient bloquer ce transporteur, mais leur effet était limité car une autre protéine, Arl2, peut les chasser de la poche au fil du temps.
Concevoir DeltaTag pour se lier au glutamate
Pour surmonter ce problème d’« expulsion », les chercheurs sont partis d’un inhibiteur de PDEδ déjà connu pour sa forte affinité et ont ré‑ingénieré l’une de ses chaînes latérales pour porter un « warhead » haloalcane semblable à ceux utilisés dans les ligands HaloTag. Après plusieurs séries d’ajustements structurels guidés par des structures cristallographiques de la protéine, ils sont arrivés à un composé appelé DeltaTag. Sa caractéristique clé est un groupe phénéthylbromure positionné de sorte que, une fois la molécule nichée dans la poche lipidique de PDEδ, le bromure soit précisément aligné pour réagir avec E88. Des mesures biophysiques et des structures cristallographiques à haute résolution ont confirmé que DeltaTag forme un lien ester covalent spécifiquement avec ce glutamate et que d’autres acides aminés potentiellement plus réactifs sur PDEδ restent intacts. Le composé est suffisamment réactif pour marquer la protéine efficacement, tout en restant assez stable en milieu aqueux et en présence du principal antioxydant sulfuré de la cellule, le glutathion, afin d’éviter des dommages généralisés et non spécifiques.
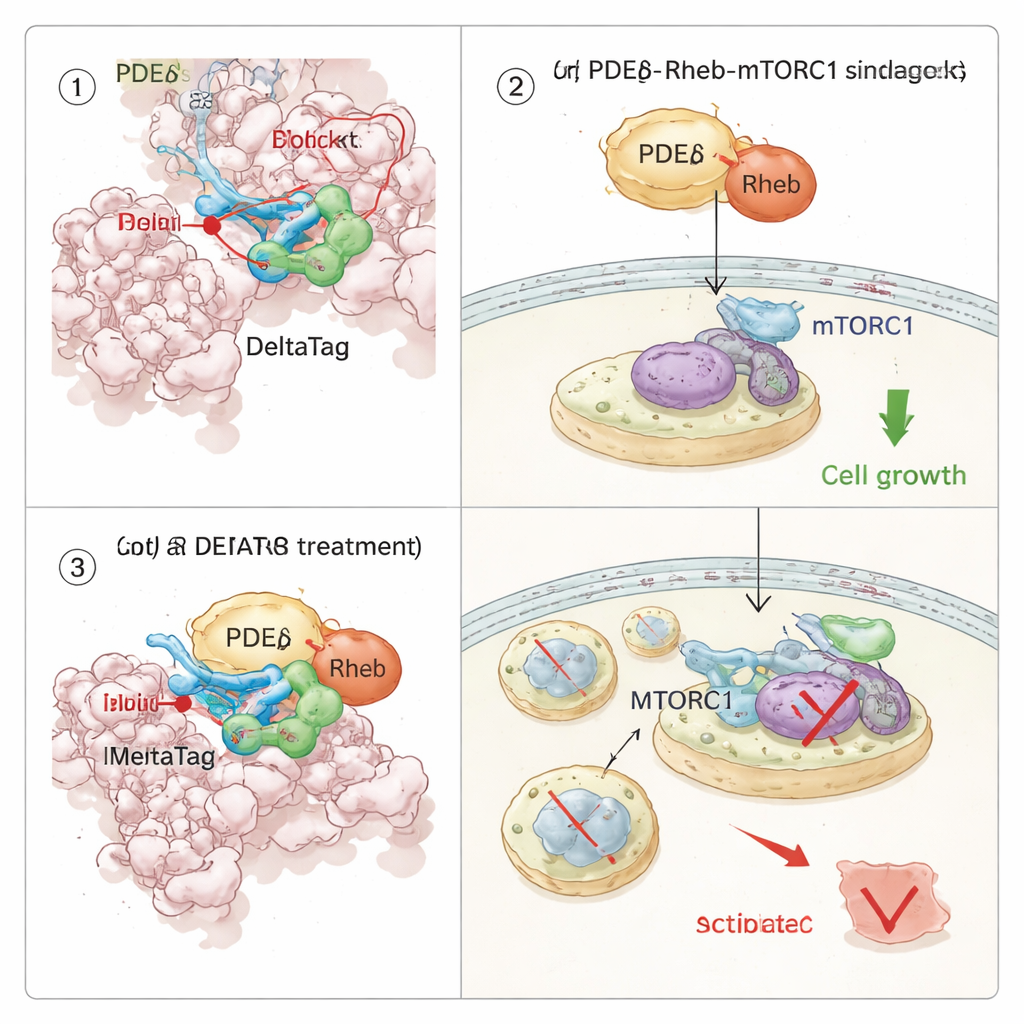
Reconfigurer une voie de croissance à l’intérieur des cellules cancéreuses
Parce que PDEδ accompagne Rheb, et que Rheb active à son tour la voie de croissance mTORC1, l’équipe a examiné comment l’inhibition covalente de PDEδ se répercuterait sur la signalisation cellulaire. En utilisant le profilage de stabilité thermique à l’échelle de milliers de protéines, ils ont montré que DeltaTag se lie sélectivement à PDEδ dans des extraits cellulaires et perturbe des protéines liées à l’axe Rheb–mTOR. Dans des expériences d’imagerie de cellules vivantes, DeltaTag a provoqué le reclassement de Rheb, passant d’un motif diffus dans le cytoplasme à des membranes internes plus regroupées, conforme à une perturbation de son transport normal. La phosphoprotéomique globale et des western blots ciblés ont révélé que l’activité de mTORC1, suivie par la phosphorylation d’une protéine ribosomale appelée S6, diminuait au fil du temps, tandis que des signaux compensateurs dans des voies voisines augmentaient. Fait important, dans plusieurs lignées cellulaires cancéreuses humaines porteuses de KRAS mutant et dépendantes d’une forte signalisation mTOR, DeltaTag a ralenti la prolifération cellulaire plus efficacement que des inhibiteurs réversibles étroitement apparentés, et son effet était atténué dans des cellules dépourvues de PDEδ, soutenant que son action principale est sur la cible prévue.
Ouvrir la voie à de nouveaux types de cibles médicamenteuses
Ce travail montre qu’il est possible de concevoir de petites molécules formant une liaison permanente et hautement spécifique avec un seul glutamate enfoui dans une poche hydrophobe d’une protéine, en utilisant une chimie haloalcane relativement simple empruntée à HaloTag. Dans le système modèle PDEδ, ce lien covalent procure un blocage plus durable d’une voie de croissance pertinente pour le cancer que les médicaments réversibles antérieurs. Plus largement, la même logique de conception pourrait s’appliquer à d’autres protéines qui possèdent des cavités hydrophobes mais manquent des acides aminés « réactifs » habituels, pourvu qu’elles présentent un glutamate ou un aspartate positionné stratégiquement. Avec une optimisation supplémentaire, des inhibiteurs covalents ciblant le glutamate comme DeltaTag pourraient devenir des outils utiles pour la biologie chimique et, ultimement, des pistes pour de nouvelles thérapies visant des protéines jusqu’ici difficiles à cibler.
Citation: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
Mots-clés: inhibiteurs covalents, ciblage du glutamate, PDEδ, signalisation mTOR, conception de médicaments contre le cancer