Clear Sky Science · fr
Concevoir des cellules synthétiques avec des domaines intramembranaires présentant des asymétries distinctes des deux feuillets
Pourquoi de minuscules bulles synthétiques comptent
Chaque cellule vivante est entourée d’une membrane qui se comporte comme une peau souple et intelligente. Cette peau n’est pas uniforme : les faces interne et externe, et même des zones distinctes à la surface, peuvent avoir des compositions et des formes très différentes. Ces différences aident les cellules à transmettre des signaux, à fixer des protéines et même à se diviser. Pourtant il a été remarquablement difficile de construire des membranes modèles simples et contrôlables qui reproduisent cette complexité. Cette étude présente une méthode pratique pour fabriquer des « cellules synthétiques » de taille cellulaire dont les membranes sont asymétriques entre les deux feuillets et lateralement structurées en régions distinctes — ouvrant la voie à des modèles cellulaires plus réalistes et à l’étude de la façon dont les motifs membranaires conduisent au bourgeonnement et à la division. 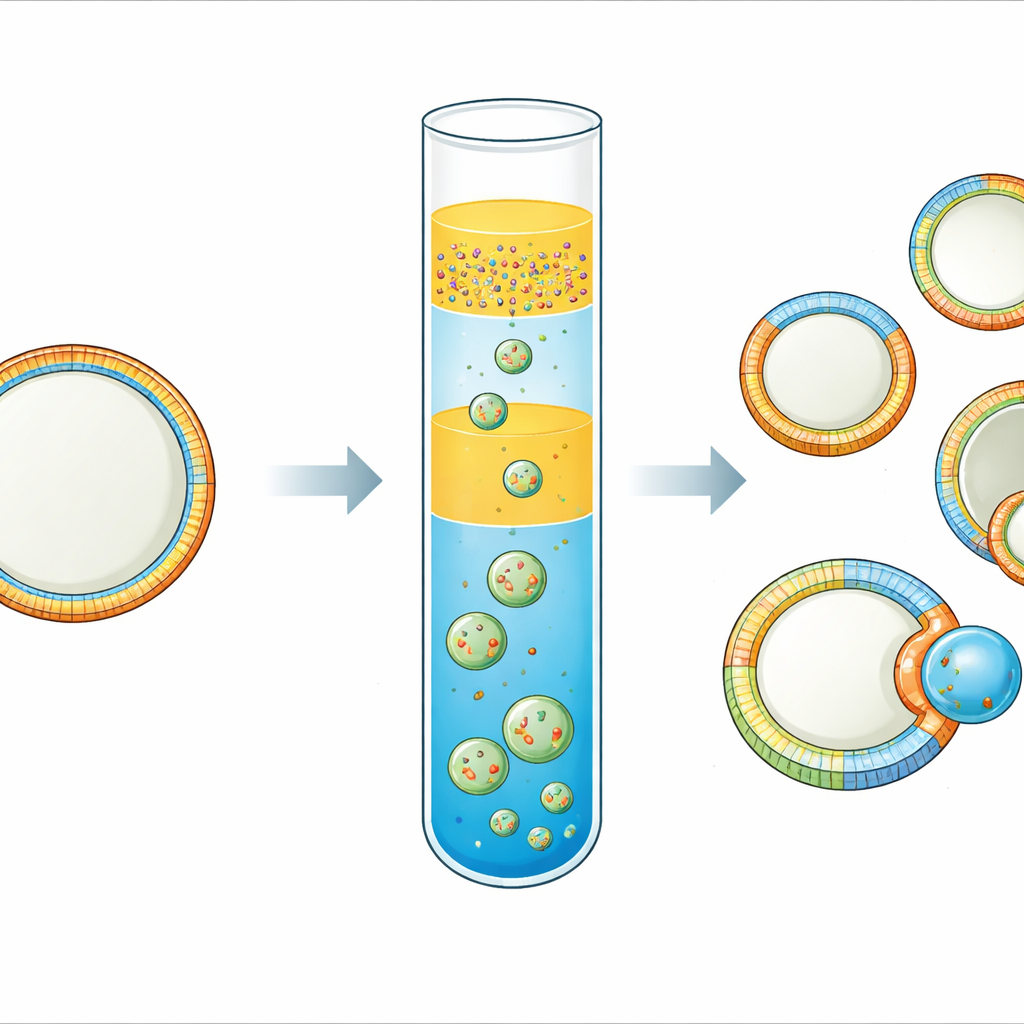
Construire de meilleurs modèles cellulaires
Les membranes cellulaires réelles sont asymétriques : la face interne est riche en lipides chargés négativement qui recrutent des protéines de signalisation, tandis que la face externe porte d’autres lipides qui médiatisent la reconnaissance cellule–cellule. De nombreuses méthodes de laboratoire peuvent produire de grandes vésicules — des sphères creuses de molécules lipidiques — mais leurs deux feuillets finissent généralement identiques, et l’intérieur est difficile d’accès. D’autres approches qui créent de l’asymétrie nécessitent souvent des dispositifs complexes, des lipides spéciaux ou laissent les vésicules collées à une surface. Les auteurs ont cherché à créer des vésicules libres de taille cellulaire qui combinent une encapsulation élevée de biomolécules avec une asymétrie robuste et modulable, plus proche de celle d’une cellule vivante.
Une recette à trois couches pour des membranes asymétriques
L’équipe a perfectionné une technique d « émulsion inversée », dans laquelle de minuscules gouttelettes d’eau recouvertes de lipides sont poussées à travers une interface huile–eau pour former des vésicules. Leur innovation clé est une configuration à triple couche d’huile. En bas se trouve une huile contenant les lipides destinés au feuillet externe de la membrane. Au-dessus, ils placent une fine couche d’huile intermédiaire sans lipides, et au sommet une émulsion de gouttelettes d’eau entourées d’une deuxième huile portant les lipides du feuillet interne. Lors d’une brève étape de centrifugation, les gouttelettes traversent la couche intermédiaire et la couche du bas, acquièrent une seconde couche lipidique et se referment en vésicules. Le choix de deux huiles de densités différentes et l’inclusion de l’espaceur limitent nettement le mélange entre les réservoirs lipidiques, de sorte que les compositions des feuillets interne et externe restent distinctes.
Vérifier que les deux faces restent différentes
Pour vérifier que les feuillets étaient réellement distincts, les chercheurs ont utilisé des lectures chimiques et à base de protéines. Dans une série de tests, ils ont ajouté un lipide fluorescent à un seul feuillet puis exposé les vésicules à un réactif dans la solution extérieure qui éteint la fluorescence mais ne traverse pas la membrane. Quand le lipide fluorescent se trouvait sur la face externe, le signal chutait presque complètement ; quand il était sur la face interne, il changeait à peine, montrant que la plupart des lipides marqués restaient là où on les avait placés. Dans une seconde série d’expériences, ils ont mis des lipides qui lient des protéines spécifiques — tels que des lipides marqués par la biotine pour la streptavidine ou des têtes spéciales pour une protéine fluorescente verte porteuse d’un tag His — sur un seul feuillet. Les protéines ajoutées au compartiment opposé (à l’intérieur ou à l’extérieur) se lient uniquement lorsque leur lipide correspondant est du même côté de la membrane, confirmant à la fois une forte asymétrie et la conservation de la fonction protéique.
Créer des radeaux et observer le bourgeonnement membranaire
Les membranes cellulaires réelles contiennent aussi des « radeaux » : de petites régions enrichies en certains lipides comme le cholestérol et la sphingomyéline, qui peuvent regrouper des protéines et influencer la forme. Obtenir une telle séparation de phases avec la méthode d’émulsion inversée avait été difficile parce que le cholestérol avait tendance à rester dissous dans l’huile plutôt qu’à rejoindre la membrane. En utilisant du squalène dans la couche d’huile inférieure, qui retient le cholestérol moins fortement que l’huile minérale standard, les auteurs ont pu former de façon reproductible des vésicules dont les membranes se séparent en régions coexistant en état liquide ordonné et liquide désordonné, à la manière des radeaux. Ils ont ensuite combiné ce patron latéral avec l’asymétrie des feuillets : un domaine portait un ligand sur le feuillet interne liant la streptavidine à l’intérieur, tandis qu’un autre domaine portait des glycolipides qui lient la toxine cholérique à l’extérieur. 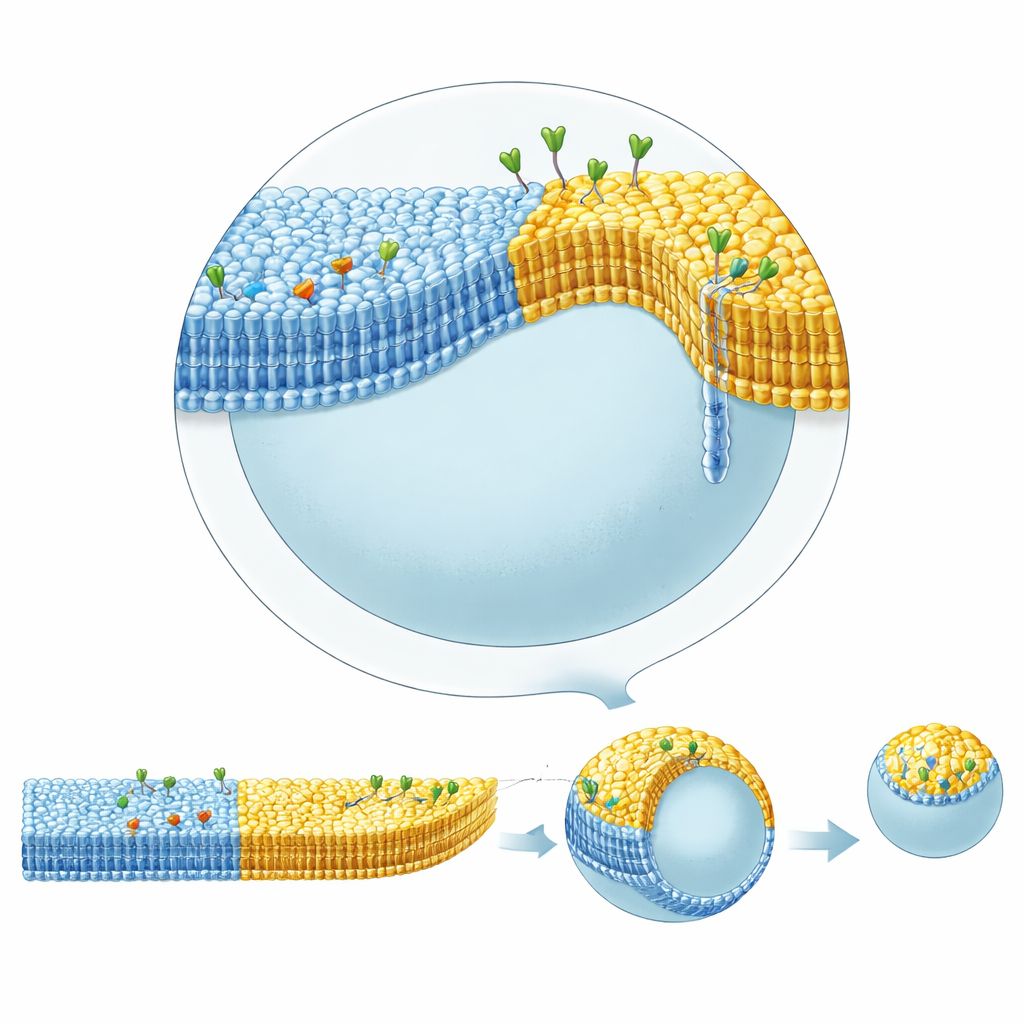
Comment les protéines et les motifs entraînent des changements de forme
Ces vésicules complexes ont montré des dynamiques de forme spectaculaires. Quand la toxine cholérique se liait aux glycolipides du domaine ordonné du côté externe, ce domaine se renflait vers l’extérieur en formant un bourgeon courbé relié par un col étroit, et sous une légère déflation osmotique il pouvait se détacher complètement comme une vésicule fille. Ce bourgeonnement ne nécessitait pas de molécules porteuses d’énergie comme l’ATP ni d’un appareil de division spécialisé ; il résultait purement de l’interaction entre la composition lipidique, les frontières de domaines et la fixation asymétrique de protéines. En augmentant la quantité de streptavidine liée du côté interne du domaine désordonné, l’équipe pouvait contrer la courbure vers l’extérieur du domaine ordonné et rétablir progressivement une forme plus sphérique. Une analyse géométrique détaillée des contours des vésicules a montré que la courbure de la membrane saute à la frontière entre domaines, et que les cols étroits se formant pendant le bourgeonnement doivent résister à des forces d’au moins plusieurs dizaines de piconewtons — quantifiant ainsi comment la structure des domaines et l’encombrement protéique peuvent sculpter mécaniquement les membranes.
Ce que cela signifie pour les futures cellules synthétiques
En termes simples, les auteurs ont mis au point une recette pour fabriquer des bulles molles de taille cellulaire dont les « peaux » sont structurées et bifeuilletées de la même manière que les membranes cellulaires réelles. Parce que la méthode est relativement simple, fonctionne avec de nombreux lipides différents et permet d’emprisonner des protéines et autres grosses molécules à l’intérieur, elle ouvre la voie à la construction, de bas en haut, de cellules artificielles plus réalistes. De telles cellules synthétiques pourraient aider les scientifiques à disséquer comment les motifs membranaires contrôlent la signalisation, le trafic et la division, et elles pourraient éventuellement être exploitées comme vecteurs thérapeutiques intelligents qui changent de forme ou se scindent sur commande dans l’organisme.
Citation: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
Mots-clés: cellules synthétiques, membranes lipidiques, asymétrie membranaire, Ségrégation de phases, bourgeonnement membranaire