Clear Sky Science · fr
Plate-forme de nanodisques de glycoprotéines virales pour l’analyse des vaccins
Transformer les protéines virales en cibles mesurables
Les vaccins modernes reposent de plus en plus sur des versions précisément conçues des protéines qui ornent la surface des virus. Ces protéines sont les principales cibles des anticorps protecteurs, mais elles sont notoirement difficiles à étudier dans leur forme naturelle ancrée dans la membrane. Cet article décrit une nouvelle plate-forme de laboratoire qui place des protéines de surface virales en pleine longueur dans de minuscules particules lipidiques plates appelées nanodisques. Ce dispositif permet aux chercheurs de mesurer dans quelle mesure les candidats vaccins imitent les virus réels, comment les anticorps s’y fixent et comment retravailler ces vaccins pour améliorer la protection.
Pourquoi recréer la surface virale est important
Beaucoup des protéines virales les plus importantes sont ancrées dans une membrane lipidique, comme c’est le cas sur un virus réel. Les approches traditionnelles en laboratoire coupent la partie membranaire pour rendre ces protéines plus faciles à produire et à purifier en solution. Mais ce raccourci supprime des régions proches de la membrane qui hébergent des cibles d’anticorps particulièrement précieuses, y compris un segment du VIH connu sous le nom de région externe proche de la membrane (MPER). Ces régions proches de la membrane peuvent avoir une apparence et un comportement différents lorsqu’elles ne sont pas intégrées dans un environnement lipidique réaliste, ce qui signifie que des fragments protéiques solubles peuvent donner une image incomplète ou trompeuse de la façon dont un vaccin se comportera dans l’organisme.
Construire une plate-forme nanodisque polyvalente
Les auteurs ont développé un protocole rationalisé sur cinq jours pour prélever des protéines de surface virales en pleine longueur à partir de cellules humaines, préserver leurs segments transmembranaires natifs et les réinsérer dans un disque lipidique contrôlé. Ils ont d’abord exprimé des glycoprotéines du VIH et d’Ebola modifiées à la surface des cellules, puis les ont extraites délicatement avec un détergent et capturées sur une matrice de purification. Alors que les protéines étaient encore attachées, ils ont ajouté des lipides définis et une protéine ceinture qui s’auto-associe en une petite membrane de forme discoïdale. À mesure que le détergent était éliminé, les protéines virales se sont intégrées dans ces nanodisques. Les préparations obtenues étaient de haute pureté, stables pendant des mois au réfrigérateur et portaient des revêtements glycanes (sucre) très proches de ceux observés sur les pointes virales natives. 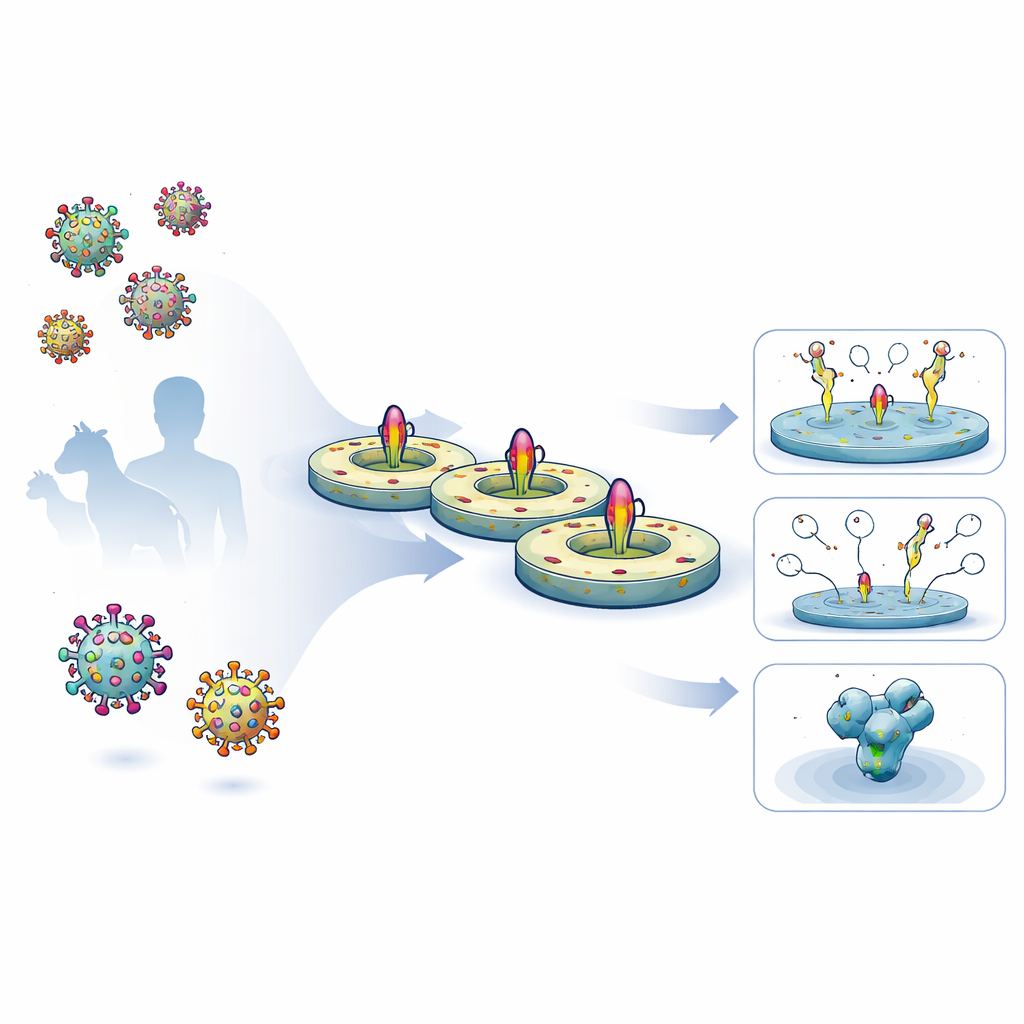
Mesurer la fixation des anticorps et les réponses immunitaires
Grâce aux protéines intégrées aux nanodisques, l’équipe a testé la capacité de différents anticorps à se lier dans plusieurs configurations de résonance plasmonique de surface (SPR), une technique qui suit les interactions en temps réel. En utilisant des nanodisques du VIH conçus pour exposer la région MPER, ils ont montré qu’un puissant anticorps neutralisant à large spectre appelé 10E8 se liait environ 70 fois plus fortement à la construction ingénierée qu’à une conception antérieure, principalement parce qu’il se détachait beaucoup plus lentement. Des mutations témoins perturbant la région MPER éliminaient totalement la liaison de 10E8, confirmant que la plate-forme peut rapporter de manière sensible comment les modifications de conception affectent des épitopes clés. Les mêmes nanodisques ont servi de sondes en cytométrie en flux, où ils ont aidé à isoler des cellules B provenant de souris et de singes immunisés reconnaissant la forme transmembranaire complète de la protéine du VIH, y compris des parties absentes des sondes solubles classiques. 
Voir la cible entière en détail atomique
Pour comprendre exactement comment les anticorps reconnaissent la MPER dans son contexte natif, les auteurs ont utilisé la cryo-microscopie électronique pour imager des nanodisques du VIH conçus, liés à trois anticorps neutralisants différents. Ils ont obtenu une structure à 3,5 angströms d’un anticorps, 10E8, en interaction avec le segment MPER pendant que le reste de la pointe du VIH restait ancré dans le disque lipidique. Cela a révélé un réseau continu de contacts entre 10E8 et à la fois la MPER et des portions voisines de la protéine externe, y compris une poche profonde à la jonction entre deux sous-unités. En comparant cette structure avec des images précédentes de 10E8 lié uniquement à un court peptide, l’équipe a montré que l’environnement membranaire et la pointe en pleine longueur permettent des contacts supplémentaires et des mouvements dynamiques invisibles dans des modèles plus simples, et que des acides aminés spécifiques du virus influencent fortement la facilité avec laquelle 10E8 peut le neutraliser.
Usages larges pour des vaccins plus intelligents
Concrètement, cette plate-forme de nanodisques offre aux concepteurs de vaccins un moyen d’évaluer des candidats vaccins transmembranaires avec les mêmes outils analytiques puissants longtemps réservés aux fragments protéiques solubles. Elle fonctionne pour différents virus, prend en charge des mesures de liaison détaillées, permet un tri et un séquençage précis des cellules B induites par le vaccin, et fournit des structures à haute résolution qui capturent des épitopes réalistes proches de la membrane. Pour le lecteur non spécialiste, la conclusion est que les scientifiques disposent désormais d’un banc d’essai plus fidèle pour les protéines de surface virales, capable de montrer quelles conceptions de vaccins ressemblent et se comportent réellement comme le virus et comment les affiner pour déclencher des réponses d’anticorps plus fortes et plus larges. Cela devrait accélérer le développement des vaccins de nouvelle génération non seulement contre le VIH mais aussi contre de nombreux autres virus enveloppés.
Citation: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Mots-clés: nanodisques, vaccins contre le VIH, glycoprotéines virales, anticorps neutralisants à large spectre, cryo-EM