Clear Sky Science · fr
Les variations en C-terminal des protéines influent sur la protéostasie
Comment l’extrémité des protéines façonne la santé
Toute protéine de nos cellules se termine par une petite « queue » composée de quelques éléments seulement. Ces queues peuvent sembler accessoires, mais cette étude montre qu’elles déterminent en silence quelles protéines persistent et lesquelles sont rapidement éliminées. Comme les niveaux protéiques sous-tendent le cancer, les maladies génétiques et la réponse cellulaire au stress, comprendre ces queues offre de nouvelles façons d’évaluer le risque de maladie et même de concevoir de futurs traitements.
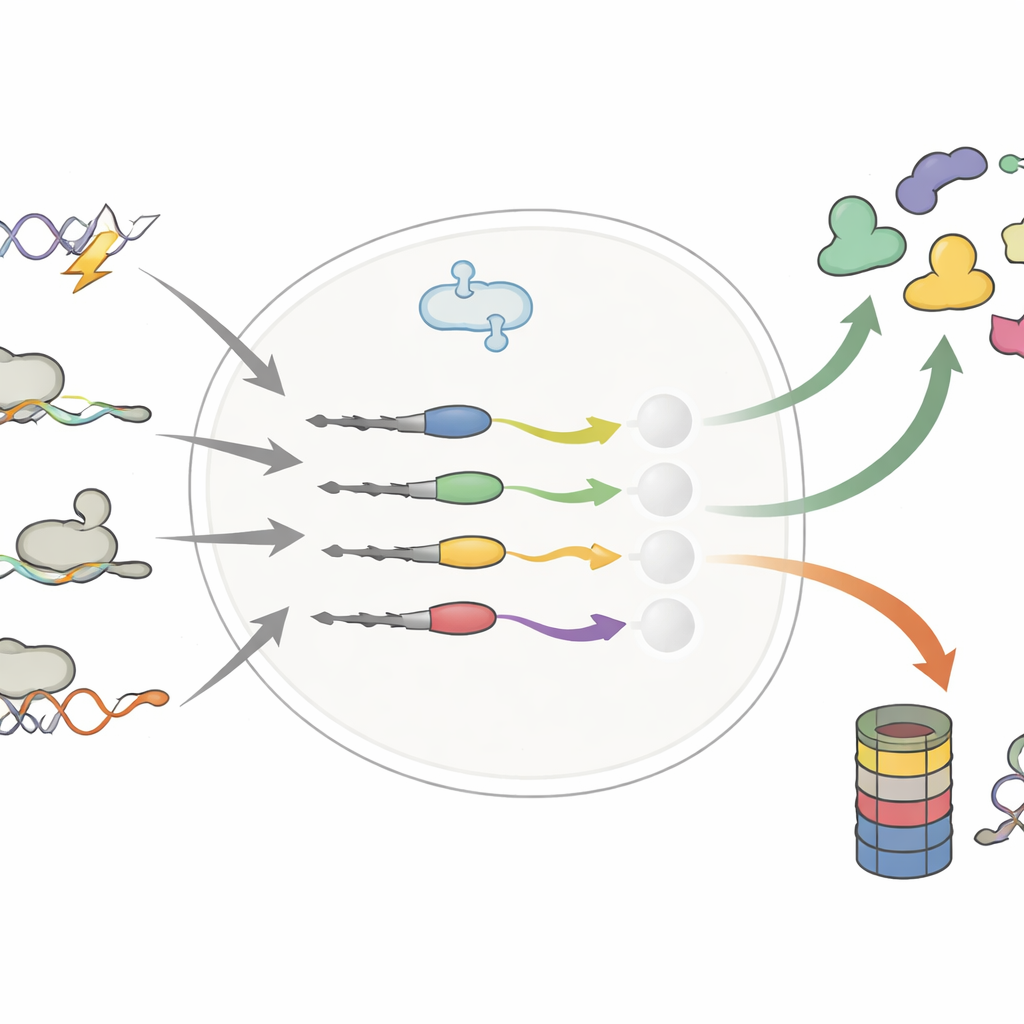
Petits changements à la queue, grands écarts dans la durée de vie
Les auteurs se sont concentrés sur l’extrémité des protéines — le C-terminal — où même l’ajout ou l’échange de quelques éléments peut apparaître via des mutations de l’ADN, l’épissage alternatif de l’ARN ou la lecture au-delà du signal d’arrêt par les ribosomes. Des travaux antérieurs suggéraient que ces queues « erronées » servent surtout d’étiquettes de mise au rebut, envoyant les protéines défectueuses vers le broyeur cellulaire. En comparant systématiquement des milliers de queues normales et altérées, cette étude renverse cette vision simpliste. L’équipe montre que les queues modifiées peuvent soit raccourcir, soit allonger la vie d’une protéine, parfois en stabilisant des oncoprotéines ou en déstabilisant des suppresseurs de tumeur.
Quand les erreurs génétiques aident ou nuisent aux protéines
Une source majeure de changements de queue est constituée par les mutations dites « nonstop », qui suppriment un signal d’arrêt normal et laissent le ribosome continuer dans une région d’ARN normalement silencieuse. Les chercheurs ont testé plus de 3 000 variants nonstop liés à des maladies en utilisant un rapporteur bicolore mesurant dans quelle mesure chaque queue protège ou affaiblit une protéine modèle. En moyenne, les queues mutantes rendaient encore les protéines moins stables que leurs homologues normales, mais une fraction significative produisait l’effet inverse : environ une mutation nonstop sur dix stabilisait les protéines, tandis qu’à peu près un tiers les déstabilisait. Ces variations concernaient des oncoprotéines et des suppresseurs de tumeur bien connus, ce qui implique que des mutations apparemment subtiles peuvent en réalité faire pencher l’équilibre entre croissance et mort cellulaire.
Variations intégrées issues de l’épissage et du readthrough
Toutes les différences de queue ne sont pas des accidents. Nos gènes produisent régulièrement plusieurs versions protéiques via l’épissage alternatif et le readthrough programmé des codons stop. En analysant les catalogues de gènes humains, les auteurs ont constaté que près des deux tiers des gènes codent pour des protéines possédant plus d’un type de queue, et beaucoup ne diffèrent que par les derniers éléments. Des tests sur des exemples sélectionnés ont montré que ces versions presque identiques ont souvent des demi-vies clairement différentes. Certaines queues générées par readthrough rendaient les protéines plus stables, d’autres moins. Cela suggère que les cellules utilisent délibérément la variation de queue comme un réglage fin, ajustant la durée de vie de formes protéiques spécifiques selon les tissus ou les conditions.
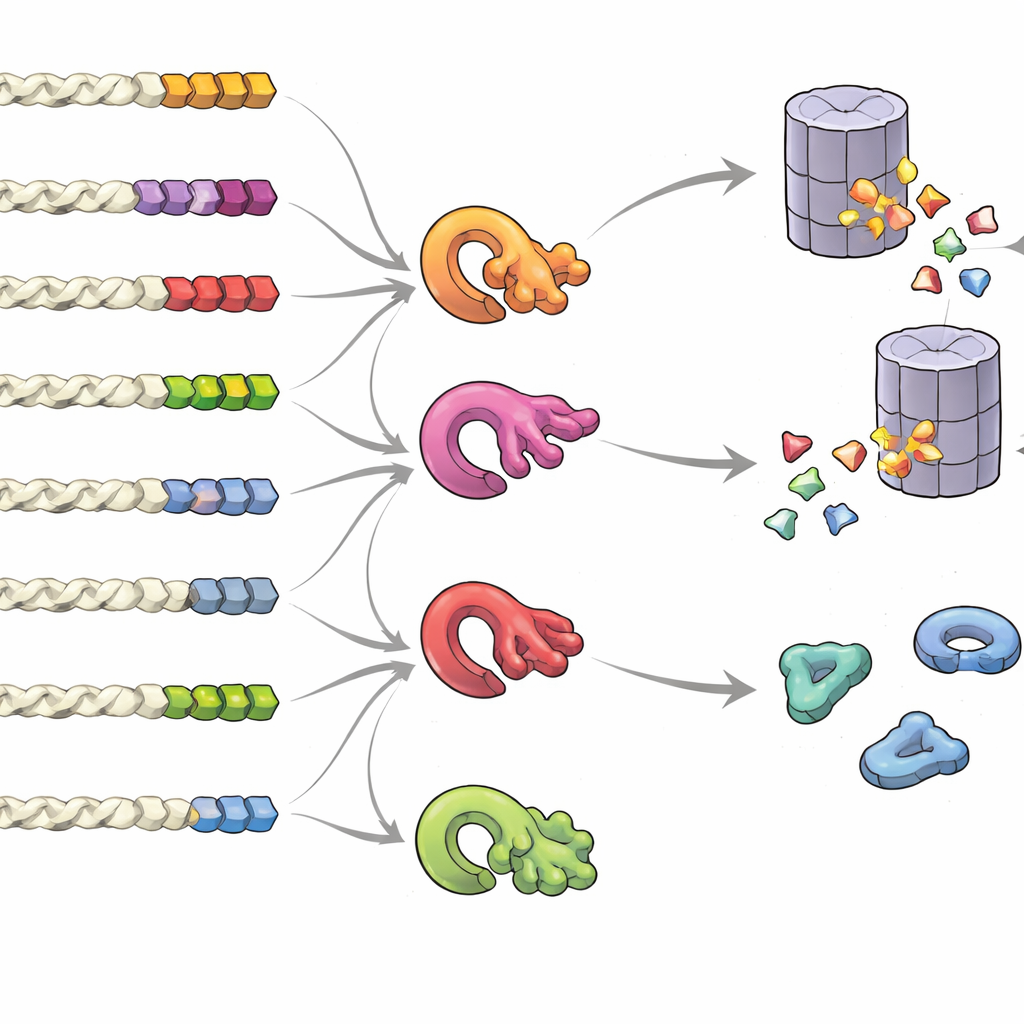
Qu’est-ce qui fait d’une queue un signal « garde-moi » ou « jette-moi »
Pour comprendre quelles caractéristiques d’une queue influencent le sort d’une protéine, l’équipe a créé des banques de queues aléatoires et mesuré leur impact en masse. Ils ont découvert qu’il ne s’agit pas d’un seul « motif » fixe mais de la composition globale, de la position et du regroupement de certains résidus qui comptent. Les queues riches en résidus petits ou hydrophobes, ou contenant les plus rares cystéine et tryptophane, avaient tendance à favoriser la dégradation, surtout quand ces résidus formaient des grappes. En revanche, les queues enrichies en acides favorisaient la stabilité. En examinant de nombreuses espèces, les queues protéiques normales montraient des signes clairs d’une pression évolutive visant à éviter les motifs à risque, tandis que les queues issues de readthrough ou de décalages de cadre, plus sujettes aux erreurs, étaient biaisées vers des compositions déstabilisantes. Le groupe a aussi découvert que plusieurs enzymes de contrôle qualité — différentes ligases d’ubiquitine — se spécialisent dans la reconnaissance de motifs hydrophobes distincts en queue, formant un réseau complexe qui décide quelles protéines sont détruites.
Pourquoi cela compte pour la médecine et la biotechnologie
Ce travail requalifie les queues protéiques, qui ne sont plus de simples terminaisons passives mais des régulateurs actifs de l’abondance protéique. Pour un non-spécialiste, cela signifie que de nombreuses maladies peuvent résulter non seulement de protéines défectueuses mais aussi de changements subtils de la durée de vie des protéines, provoqués par de minuscules différences à leurs extrémités. Cela met aussi en garde contre les thérapies qui favorisent délibérément le readthrough des signaux d’arrêt, utilisées pour traiter certains troubles génétiques, car elles pourraient involontairement modifier la durée de vie de nombreuses protéines normales. En même temps, les résultats suggèrent de puissantes nouvelles stratégies : en concevant des séquences de queue ou en incitant les cellules à favoriser certaines formes d’épissage ou d’événements de readthrough, les chercheurs pourraient un jour ajuster avec précision les niveaux protéiques à la hausse ou à la baisse.
Citation: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Mots-clés: stabilité des protéines, queue C-terminale, dégradation des protéines, mutations génétiques, protéostasie