Clear Sky Science · fr
VSIG10L est un déterminant majeur de l’homéostasie œsophagienne et de la prédisposition héréditaire à l’œsophage de Barrett
Pourquoi cela importe pour les personnes souffrant de brûlures d’estomac
Les brûlures d’estomac chroniques sont fréquentes, mais seule une petite proportion de personnes développe un œsophage de Barrett, une affection pouvant évoluer en cancer de l’œsophage. Cette étude pose une question simple mais essentielle : pourquoi certaines familles sont-elles beaucoup plus exposées que d’autres au risque d’œsophage de Barrett ? En retracer un seul gène et en observant comment il façonne la muqueuse œsophagienne chez l’homme et la souris, les chercheurs mettent au jour un lien manquant entre le risque hérité, les lésions dues au reflux et la capacité de l’organisme à maintenir la santé de l’œsophage.
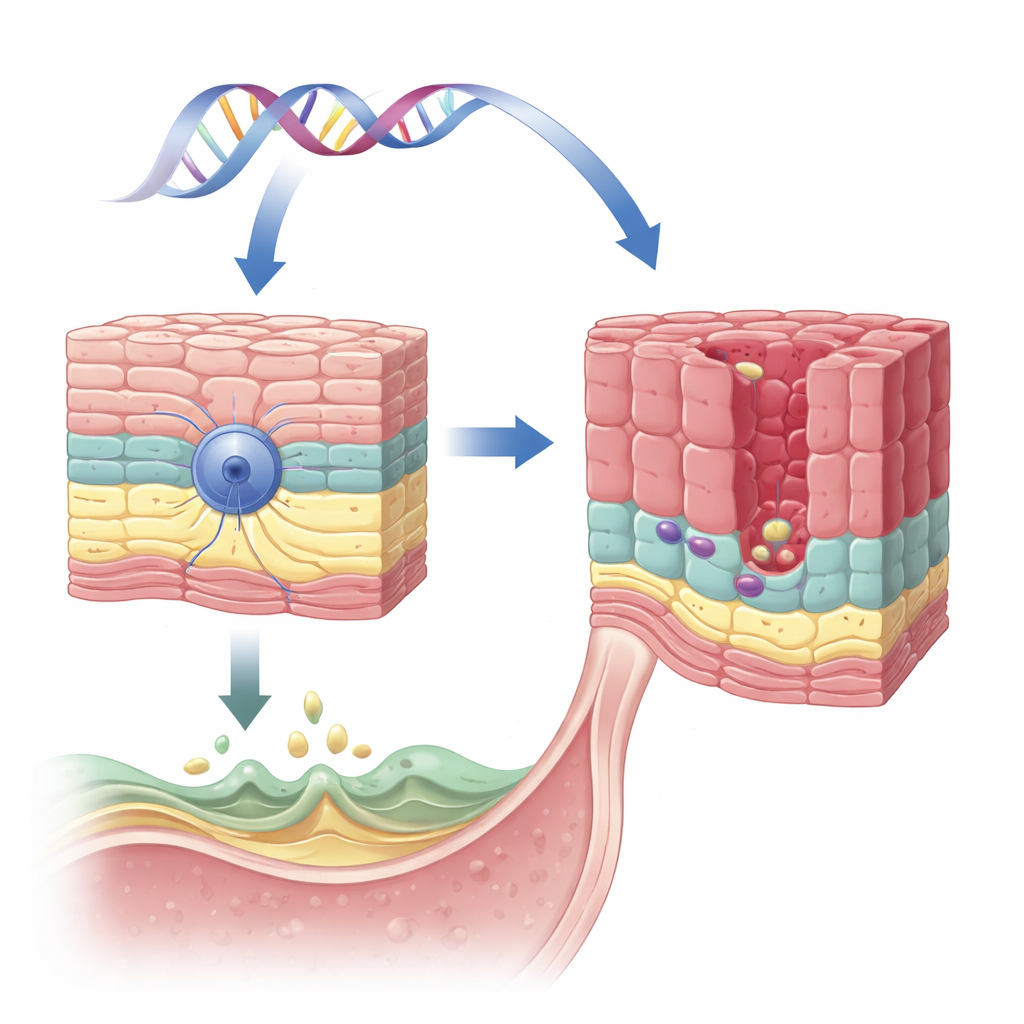
Un gène protecteur dans l’épithélium œsophagien
L’équipe s’est concentrée sur un gène nommé VSIG10L, déjà identifié dans une grande famille comptant de nombreux cas d’œsophage de Barrett et de cancers associés. VSIG10L est exprimé dans les couches superficielles des cellules squameuses plates qui tapissent l’œsophage, mais pas dans les cellules basales plus profondes, de type souche. À l’aide d’une méthode sensible de détection de l’ARN sur des tissus humains, porcins et murins ainsi que sur des cultures tridimensionnelles de cellules œsophagiennes humaines, les chercheurs ont montré que VSIG10L est systématiquement activé uniquement dans les cellules en « maturation » juste au‑dessus de la couche basale. Ce schéma suggère que VSIG10L aide les cellules squameuses à achever leurs derniers pas de maturation et à former une barrière stable.
Variantes héréditaires qui affaiblissent la barrière
En séquençant le gène VSIG10L chez 684 personnes issues de 302 familles touchées par l’œsophage de Barrett et le cancer œsophagien, les investigateurs ont découvert plusieurs variants rares et délétères. Pour tester l’effet de ces variants, ils ont conçu des organoïdes œsophagiens dérivés de cellules souches humaines à partir d’un patient porteur d’une telle mutation. Comparés aux organoïdes d’un donneur sain, les organoïdes mutants n’ont pas réussi à reconstruire la structure squameuse normale en couches. Ils ont plutôt formé souvent des amas cellulaires anormaux, de type glandulaire, qui restaient bloqués dans un état basal immature, marqué par la présence de la protéine p63. Cette déformation de la stratification et de la maturation rappelle les étapes initiales supposées précéder l’apparition de l’œsophage de Barrett chez les patients.
Modèles murins qui reproduisent la maladie humaine
Pour aller au‑delà des cultures cellulaires, l’équipe a créé des souris portant soit une copie précise de la mutation familiale humaine de VSIG10L, soit une perte complète du gène. Chez les souris saines, le gène correspondant Vsig10l est à nouveau exprimé uniquement dans les cellules squameuses suprabasales. Au microscope électronique, les souris mutantes ont montré une perte marquée de desmosomes — les petites « rivets » qui fixent les cellules voisines entre elles — dans ces couches. Les cartes d’activité génique issues de l’estomac forestomacal squameux, une région murine ressemblant à l’œsophage inférieur, ont révélé une perturbation étendue des programmes structurels et de différenciation. Lorsqu’on a donné aux souris un régime contenant de l’acide biliaire déoxycholate, simulant un reflux chronique, 70–100 % des animaux mutants pour Vsig10l ont développé d’importantes plages riches en mucine de type Barrett à la jonction squameuse–colonnaire, tandis que les souris de type sauvage n’ont présenté que de petites lésions limitées.
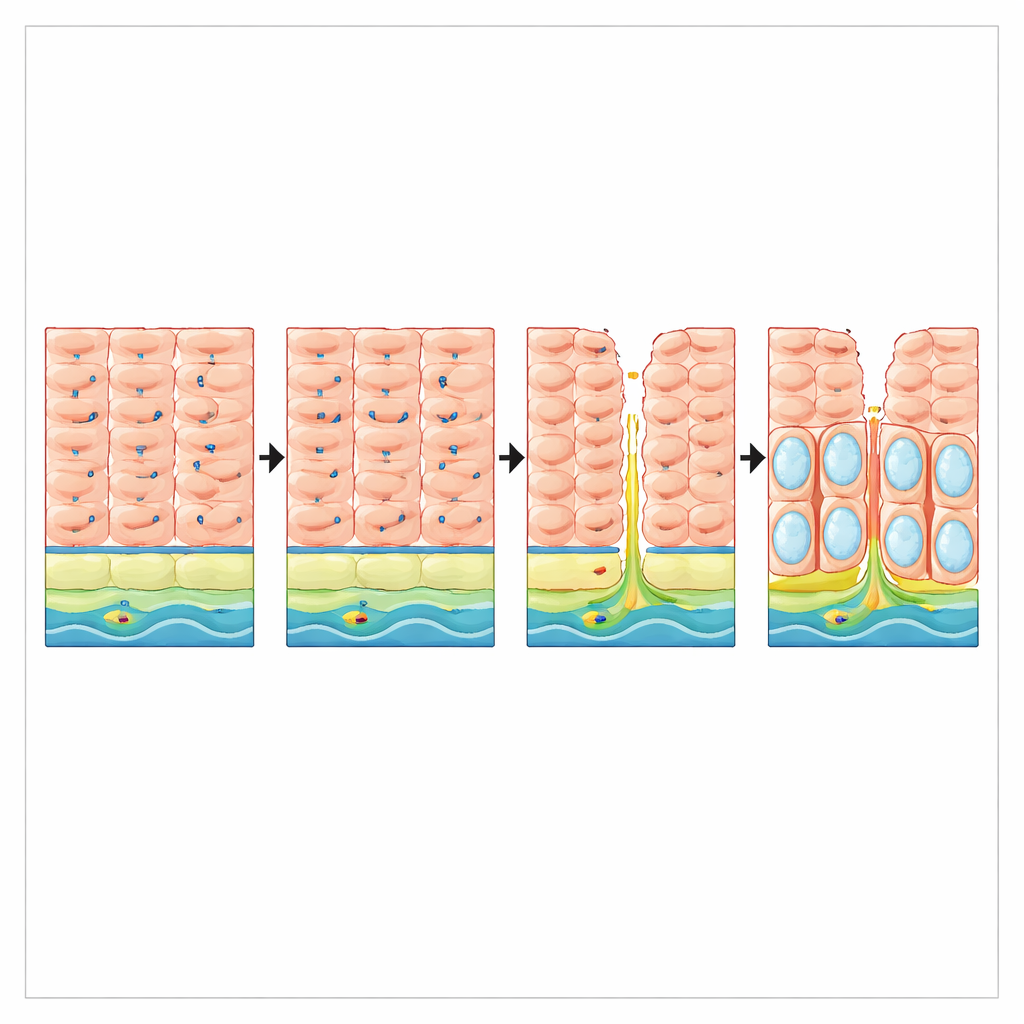
Lésions liées au reflux et perte de protection chez les patients
Les chercheurs ont ensuite demandé si le reflux lui‑même pouvait perturber VSIG10L chez l’homme. Dans des biopsies de patients atteints d’un reflux gastro‑œsophagien de longue date mais sans œsophage de Barrett, les niveaux d’ARN de VSIG10L étaient environ trois fois plus bas que chez des personnes sans reflux, alors que le marqueur basique des cellules squameuses TP63 était inchangé. Dans des coupes tissulaires, la muqueuse œsophagienne saine montrait une bande nette de cellules positives pour VSIG10L au‑dessus d’une couche basale. En revanche, la muqueuse endommagée par le reflux affichait une expansion de cellules de type basale riches en p63 et une perte quasi totale du gradient de différenciation positif pour VSIG10L. Ces résultats suggèrent que le reflux chronique érode non seulement l’intégrité physique de la muqueuse, mais aussi le programme génique qui assure son renouvellement ordonné.
Assembler les pièces du puzzle
Dans l’ensemble, ce travail soutient un modèle simple : VSIG10L est un gardien clé de la barrière squameuse œsophagienne. Des défauts héréditaires de ce gène, ou sa suppression acquise par un reflux chronique, entraînent une mauvaise maturation de la muqueuse, moins de points d’ancrage entre cellules et une surface plus perméable. Dans cet état vulnérable, l’exposition répétée à l’acide et à la bile favorise une cicatrisation anormale en structures glandulaires plutôt que la restauration de l’épithélium squameux initial, préparant le terrain pour l’œsophage de Barrett. Pour les patients et les familles, cette recherche ouvre la voie à de futurs tests génétiques permettant d’identifier les personnes à risque élevé et à de nouvelles thérapies visant à préserver ou restaurer la fonction de VSIG10L, avec pour objectif à long terme de prévenir l’œsophage de Barrett et sa progression vers le cancer.
Citation: Ravillah, D., Singh, S., Katabathula, R.M. et al. VSIG10L is a major determinant of esophageal homeostasis and inherited predisposition to Barrett’s esophagus. Nat Commun 17, 2167 (2026). https://doi.org/10.1038/s41467-026-68975-3
Mots-clés: Œsophage de Barrett, reflux gastro-œsophagien, prédisposition génétique, homéostasie épithéliale, risque de cancer de l’œsophage