Clear Sky Science · fr
Exploiter l’allostérie humaine de la fucosyltransférase 8 avec un inhibiteur covalent pour supprimer la fucosylation centrale
Pourquoi bloquer un petit sucre peut avoir de l’importance pour le cancer
Nos cellules décorent en permanence les protéines de courtes chaînes sucrées qui ajustent finement leur fonction. Une marque sucrée particulière, appelée fucosylation centrale, favorise la croissance tumorale, la dissémination, l’évasion immunitaire et même la résistance aux médicaments anti‑cancer contemporains. Cet article décrit comment des scientifiques ont identifié un point de commande caché sur l’enzyme humaine qui ajoute ce sucre, puis conçu une nouvelle molécule à faible toxicité qui se fixe sur ce point de contrôle pour désactiver l’enzyme. Leur travail ouvre une voie nouvelle pour des médicaments qui reprogramment subtilement les sucres de surface des cellules au lieu d’attaquer directement l’ADN ou les protéines.
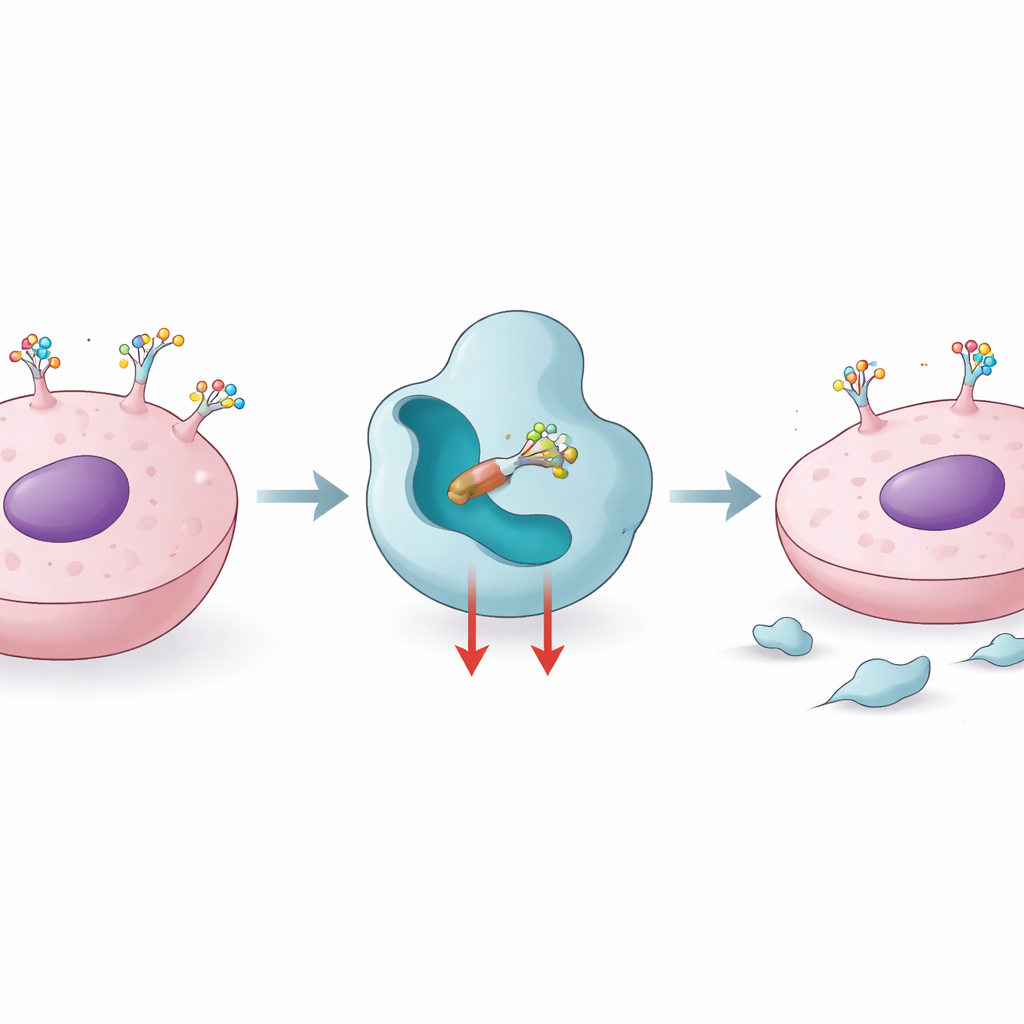
Comment les cellules utilisent les étiquettes sucrées pour façonner la maladie
Les protéines quittant la « fabrique » intracellulaire passent par une sorte de « ligne de finition » moléculaire où des chaînes sucrées sont ajoutées et modifiées. La fucosylation centrale est l’une de ces étapes finales, assurée par une enzyme nommée FUT8, qui ajoute un résidu de fucose à une position clé sur de nombreux glycannes liés aux protéines. Lorsque les niveaux de FUT8 augmentent, cette marque sucrée devient plus fréquente sur des molécules qui contrôlent la croissance cellulaire, la mobilité et la reconnaissance immunitaire. Des études ont relié une activité élevée de FUT8 à des mélanomes agressifs, des cancers du sein triple négatifs, des cancers du poumon, ainsi qu’à la résistance à des traitements ciblés et à certaines thérapies par anticorps. Bloquer FUT8 peut dépouiller certaines protéines immunorégulatrices, comme PD‑1, de la surface cellulaire et rendre les tumeurs plus visibles pour le système immunitaire, faisant de FUT8 une cible attrayante pour l’immunothérapie anticancéreuse et pour l’amélioration des médicaments biologiques.
Le besoin de bloqueurs plus intelligents et plus sélectifs
Concevoir des médicaments contre FUT8 a été difficile car de nombreuses enzymes apparentées utilisent toutes la même source sucrée de base. Les inhibiteurs antérieurs imitaient souvent ce carburant, entraînant une inhibition vaste et non sélective de nombreuses voies de fucosylation et des effets indésirables, y compris des problèmes de coagulation qui ont stoppé un essai clinique. Les auteurs ont estimé qu’une meilleure stratégie serait d’éviter le site actif principal très encombré et de rechercher plutôt un site « lointain » unique sur FUT8 pouvant agir comme un interrupteur de commande. En utilisant un test de criblage à haut débit mesurant l’activité enzymatique, ils ont passé en revue plus de six mille composés et identifié quelques molécules allongées qui ralentissaient FUT8 tout en réduisant l’invasion des cellules tumorales en culture.
Découverte d’une poche de contrôle cachée
Par cristallographie aux rayons X, l’équipe a résolu les structures tridimensionnelles de FUT8 liées à deux de ces inhibiteurs. À leur surprise, aucun des composés ne se trouvait dans l’emplacement habituel où se lient le donneur et l’accepteur de sucre. Ils s’inséraient plutôt dans une longue poche en forme de canal entre deux grands lobes de l’enzyme, proche mais distincte du centre actif. La liaison à ce site déplaçait certaines boucles et acides aminés clés, en particulier des éléments qui aident normalement à fixer le donneur de sucre. Des simulations informatiques ont montré que, lorsque la poche était occupée, le mouvement global et le paysage énergétique de FUT8 changeaient, favorisant des conformations peu efficaces pour catalyser la réaction. En d’autres termes, les inhibiteurs agissaient allostériquement : ils appuyaient sur un bouton lointain qui désalignait les parties actives de l’enzyme.
Transformer une molécule « hit » en un outil covalent précis
Munis de cette carte structurale, les chercheurs ont cherché des molécules qui pourraient non seulement occuper la poche mais aussi former une liaison permanente à une lysine voisine (K216) qui bascule naturellement vers le canal. Ils ont constaté qu’un réactif appelé SSO, portant un ester N‑hydroxysuccinimide réactif, se liait dans la même rainure et formait un lien covalent avec K216, verrouillant l’enzyme dans un état inactif. En combinant les caractéristiques communes de SSO et de leur première molécule candidate NH125, ils ont fusionné des fragments des deux pour créer une nouvelle molécule nommée CAIF. Les structures cristallines ont confirmé que CAIF s’insère le long du canal, s’ajuste parmi des résidus hydrophobes et forme une liaison covalente à K216. Cette conception a multiplié l’inhibition de FUT8 par rapport aux composés parents tout en épargnant des enzymes étroitement apparentées, soulignant la forme unique de la poche allostérique de FUT8.
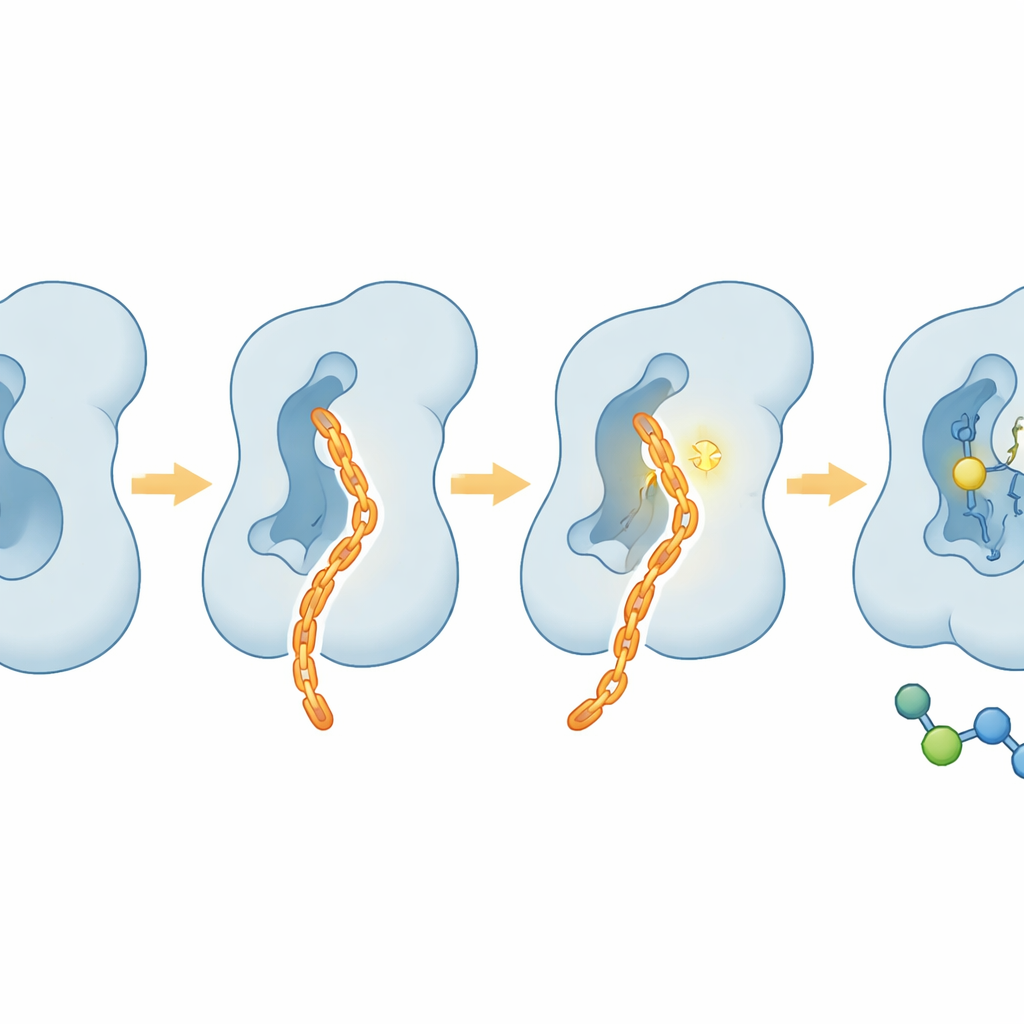
Peu toxique pour les cellules, sévère sur le comportement tumoral
Au‑delà des éprouvettes, l’équipe a examiné le comportement de CAIF dans des cellules vivantes. Dans plusieurs lignées cellulaires humaines, CAIF a montré une toxicité minimale même à fortes doses, indiquant qu’il ne pollue pas largement la machinerie cellulaire. Pour autant, il réduisait nettement la fucosylation centrale à la surface cellulaire, comme l’ont révélé des sondes de liaison aux sucres, et ce avec une bien meilleure sélectivité pour FUT8 que les anciens inhibiteurs pan‑fucosylants. Dans des essais d’invasion cellulaire, CAIF a surpassé un bloqueur à base de sucre couramment utilisé pour limiter la capacité des cellules tumorales à migrer à travers une matrice, un marqueur du potentiel métastatique. Ces effets correspondent au rôle connu de FUT8 dans l’augmentation de l’invasion et de l’évasion immunitaire plutôt que dans la stimulation directe de la division cellulaire.
Ce que cela signifie pour les traitements anticancéreux futurs
Cette étude ne prétend pas que CAIF soit lui‑même prêt à devenir un médicament. Elle montre en revanche que FUT8 contient une poche allostérique jusque‑là inconnue et pharmacologiquement exploitable, qui peut être ciblée par des molécules finement ajustées formant une liaison durable à une lysine unique. En exploitant ce site, les chercheurs peuvent réduire sélectivement l’activité d’une enzyme modifiant les sucres qui se situe au carrefour de la progression tumorale, de l’évasion immunitaire et de la résistance aux traitements, tout en laissant les enzymes apparentées largement intouchées. Ce travail offre une feuille de route pour concevoir des inhibiteurs de nouvelle génération qui remodèlent les motifs sucrés pertinents pour la maladie sur les protéines et pourraient, en fin de compte, élargir la boîte à outils de l’immunothérapie anticancéreuse et l’amélioration des anticorps thérapeutiques.
Citation: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
Mots-clés: Inhibition de FUT8, fucosylation centrale, inhibiteurs allostériques covalents, glycosylation et cancer, conception de médicaments contre les glycosyltransférases