Clear Sky Science · fr
Transformations photoinduites par inadéquation de polarité : isoquinolines en naphthalenes
Éclairer de nouvelles voies pour les médicaments
De nombreux médicaments modernes reposent sur des structures carbonées planes et annelées. Remplacer un type d’anneau par un autre peut modifier profondément le comportement d’un médicament dans l’organisme, mais cela exige généralement des synthèses longues et coûteuses. Cette étude présente un raccourci activé par la lumière : une méthode pour remodeler directement un anneau azoté courant, l’isoquinoline, en un anneau proche constitué uniquement de carbone, le naphthalène. La méthode fonctionne dans des conditions douces, tolère de nombreux groupes fonctionnels et peut être appliquée tard dans la chaîne de synthèse d’un médicament, ouvrant des voies plus rapides vers des traitements améliorés.
Pourquoi changer le cœur d’un anneau importe
En découverte de médicaments, les chimistes construisent et testent d’immenses bibliothèques de molécules apparentées pour ajuster des propriétés comme la puissance, la sélectivité et la stabilité. Même le remplacement d’un seul atome dans l’anneau central peut modifier fortement l’aptitude d’un composé à se lier à sa cible biologique ou sa durée de vie dans l’organisme. Les isoquinolines et les naphthalenes sont des exemples classiques de cœurs « sosies » interchangeables : ils ont des dimensions et des formes similaires, mais l’un porte un atome d’azote alors que l’autre est uniquement carboné. Traditionnellement, passer d’un cœur à l’autre exige de reconstruire la molécule depuis le début, étape par étape et laborieusement. Une conversion directe en une seule étape permettrait aux chimistes de recycler des molécules existantes en de nouvelles variantes au lieu de tout recommencer.
Transformer une inadéquation électronique en avantage
Le défi tient au fait que les isoquinolines et les alcynes employés pour construire des naphthalenes sont tous deux relativement appauvris en électrons, de sorte qu’ils se repoussent habituellement lors de l’étape clé de formation de liaison, un type de réaction de fermeture d’anneau à six atomes. Les auteurs ont contourné cette « inadéquation de polarité » en faisant appel à la lumière visible et à une base inorganique simple. Lorsqu’une isoquinoline est convertie en sel et associée au carbonate, les deux forment une association lâche capable d’absorber la lumière bleue. Des études computationnelles ont guidé la conception et montré que l’excitation lumineuse transfère un électron du carbonate vers l’isoquinoliniums, le transformant temporairement en radical riche en électrons. Dans cet état activé, l’isoquinoline peut alors s’additionner pas à pas à un alcyne appauvri en électrons, formant un nouveau système annulaire qui se réarrange finalement en naphthalène en expulsant un fragment contenant de l’azote.
Examiner la réaction en laboratoire
Expérimentalement, la transformation est simple à réaliser : des sels d’isoquinolinium, des alcynes et du carbonate de sodium sont agit és dans de l’éthanol sous LED bleues sans photocatalyseur additionnel. L’équipe a optimisé les conditions, montrant que le carbonate est crucial non seulement en tant que base mais aussi en tant que donneur d’électrons, et que les ions bromure favorisent le processus. Des pièges à radicaux interrompent la réaction et capturent des adduits intermédiaires, soutenant la voie radicalaire proposée par les calculs. Des expériences spectroscopiques ont confirmé que le complexe isoquinolinium–carbonate est le véritable absorbeur de lumière, et le changement d’ions contre‑ioniques ou de bases a modifié les rendements de manière cohérente avec leur aptitude à participer au transfert d’électrons.
Des systèmes modèles aux molécules de type médicament
Une fois les conditions optimisées, les auteurs ont démontré un vaste éventail d’applications. De nombreux alcynes substitués différemment ont réagi, y compris ceux portant des groupes sensibles comme l’iode, des doubles liaisons supplémentaires, et des fragments issus de produits naturels ou de médicaments existants. Une large gamme de sels d’isoquinolinium a également fonctionné, même des composés encombrés ou contenant des hétérocycles, donnant accès à des naphthalenes multi‑substitués difficiles à préparer par des voies traditionnelles. La méthode a même pu remodeler des molécules bioactives complexes comme l’inhibiteur PRMT3 SGC707 et le médicament anti‑vasospasme fasudil en leurs analogues naphthalenes en une seule opération en phase finale. Les nouveaux produits portent des groupes esters qui servent à la fois de points d’ancrage potentiels pour la liaison aux protéines et d’entrées synthétiques polyvalentes.
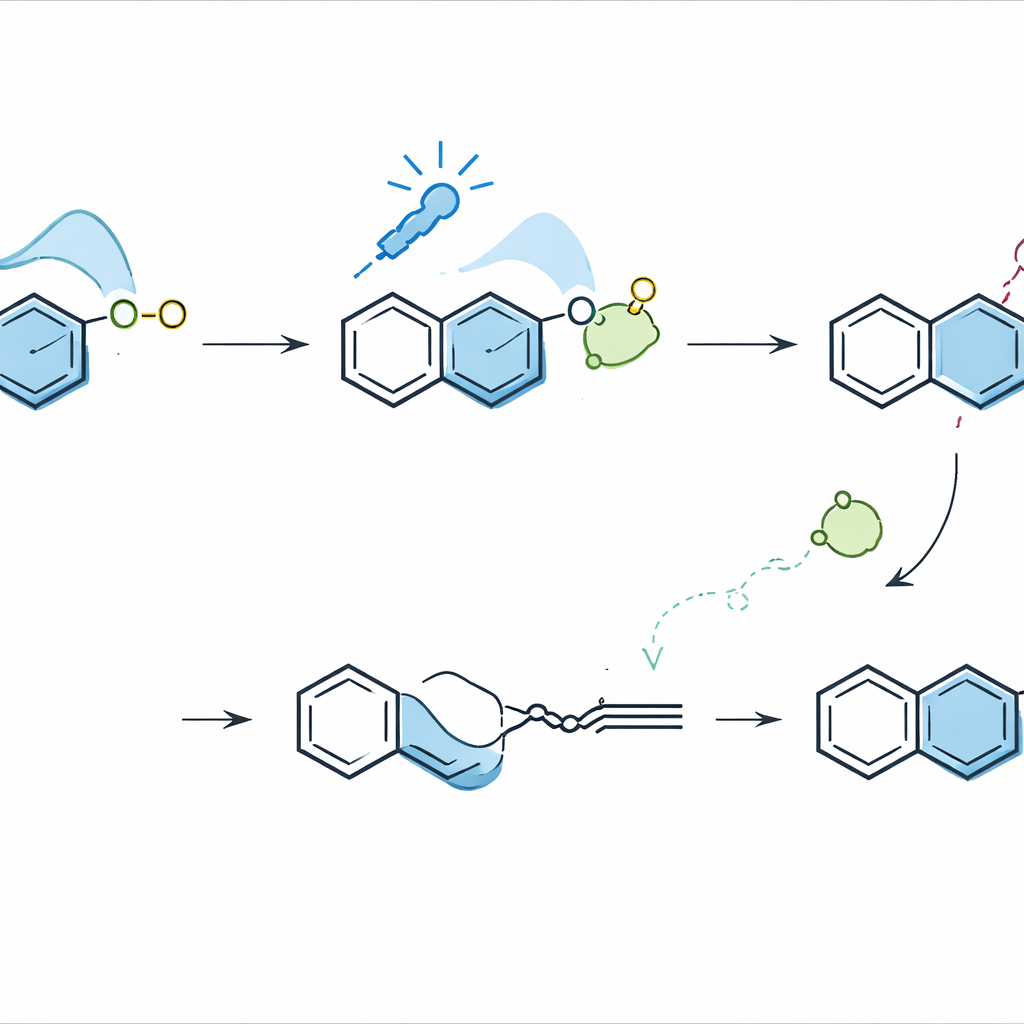
Construire des architectures plus grandes à partir des nouveaux anneaux
Les esters de naphthalène fraîchement obtenus ne sont pas de simples produits finaux ; ils servent de blocs de construction pour des structures plus élaborées. L’équipe a présenté une série de réactions de suivi qui convertissent ces esters en hydrocarbures aromatiques polycycliques et ligands chiraux de grande valeur, tels que des benzofluorénones, carbazoles, BINOL et QUINOL — des échafaudages largement utilisés en science des matériaux et en catalyse asymétrique. Dans une autre démonstration, ils ont utilisé la méthode comme étape clé pour préparer un analogue de l’adapalène, un médicament dermatologique, à partir d’un précurseur isoquinoline facilement assemblé.
Ce que cela signifie pour l’avenir
En utilisant la lumière visible pour inverser le caractère électronique d’un anneau contenant de l’azote, ce travail transforme une réaction auparavant défavorable en un outil puissant d’édition squelettique. Les chimistes peuvent désormais convertir des isoquinolines abondantes directement en naphthalenes richement fonctionnalisés, évitant des voies synthétiques longues et préservant des chaînes latérales délicates. Pour le grand public, la conclusion est que le « recyclage » de molécules existantes en nouveaux cœurs devient plus pratique, ce qui pourrait accélérer la recherche de meilleurs médicaments et matériaux avancés tout en réduisant les coûts et les déchets.
Citation: Zhang, C., Zhang, J., Lan, Y. et al. Photoinduced polarity-mismatched transformations of isoquinolines into naphthalenes. Nat Commun 17, 2547 (2026). https://doi.org/10.1038/s41467-026-68969-1
Mots-clés: édition squelettique, photochimie, isoquinoline, naphthalène, découverte de médicaments