Clear Sky Science · fr
Le repliement induit par association gouverne l’assemblage du chaînon léger substitut et du récepteur pré‑B
Comment notre organisme teste les nouveaux anticorps
Avant qu’un jeune lymphocyte B dans la moelle osseuse soit autorisé à rejoindre le système immunitaire, il doit réussir une épreuve sévère : peut‑il construire un noyau d’anticorps fonctionnel ? Cet article explore comment une version « d’essai » spéciale d’une partie de l’anticorps, appelée chaînon léger substitut, aide à réaliser ce test. En observant comment ces protéines se replient et s’emboîtent, les auteurs révèlent un système de contrôle qualité caché qui décide quels futurs anticorps sont assez bons pour être conservés — et lesquels sont éliminés.
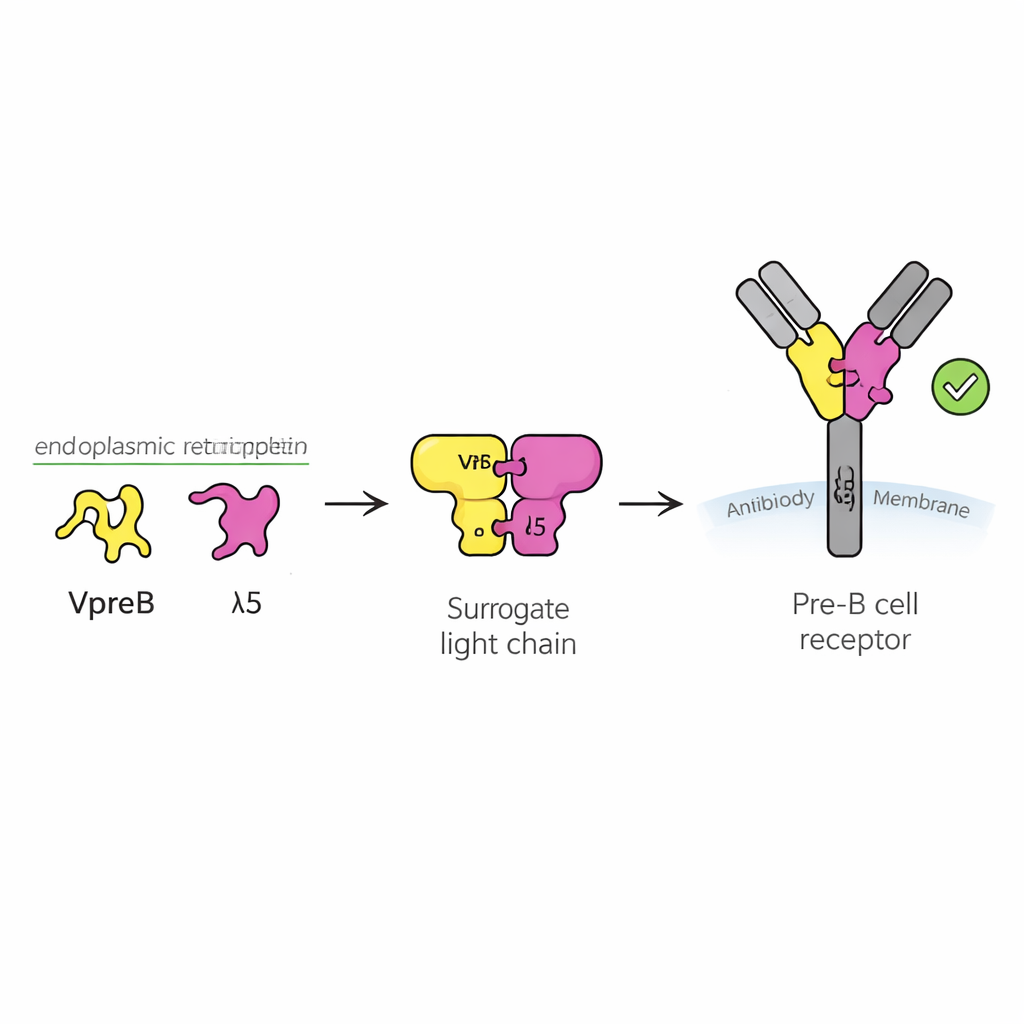
Un point de contrôle de sécurité pour les jeunes cellules immunitaires
Les anticorps sont des protéines en forme de Y qui reconnaissent les agents infectieux. Ils sont constitués de deux parties principales : des chaînes lourdes et des chaînes légères. Pendant le développement des lymphocytes B, la chaîne lourde est synthétisée en premier, et la cellule doit déterminer si cette nouvelle chaîne lourde est utile avant d’investir de l’énergie pour produire une chaîne légère assortie. Pour cela, la cellule utilise un remplaçant temporaire appelé chaînon léger substitut, composé de deux protéines nommées VpreB et λ5. Ensemble avec la chaîne lourde, elles forment le récepteur pré‑B, un senseur à la surface cellulaire qui envoie un signal « go » ou « stop ». Environ la moitié des chaînes lourdes nouvellement réarrangées échouent à ce test, si bien que comprendre le fonctionnement du chaînon léger substitut est essentiel pour saisir comment un répertoire d’anticorps sain est constitué.
Repliement par association : aider un partenaire instable
Les auteurs ont constaté qu’un des composants, VpreB, est en grande partie non replié et instable lorsqu’il est isolé. À l’aide de techniques biophysiques, ils ont montré qu’il n’adopte sa conformation tridimensionnelle correcte que lorsqu’il se lie à λ5. Un court segment de λ5, en forme de feuillet β, s’insère dans VpreB et complète sa structure, comme l’insertion d’une dent manquante dans un engrenage. Ce « repliement induit par association » stabilise non seulement VpreB, mais crée aussi un partenariat très serré entre les deux protéines, avec une affinité de l’ordre du nanomolaire inférieur. Dans les cellules, ce n’est que lorsque VpreB et λ5 s’assemblent en ce chaînon léger substitut qu’ils échappent à la rétention dans le réticulum endoplasmique pour être sécrétés ou exportés, soulignant à quel point repliement et contrôle qualité sont étroitement couplés.
Finaliser la chaîne lourde et passer l’inspection
L’histoire ne s’arrête pas à VpreB et λ5. Une région cruciale de la chaîne lourde, appelée CH1, est initialement non structurée et retenue à l’intérieur de la cellule. Les chercheurs ont montré que λ5, agissant quelque peu comme une chaperonne, peut déclencher le repliement du CH1 lorsqu’elles se lient. Cette seconde étape de repliement induit par association est essentielle pour construire le récepteur pré‑B complet et lui permettre de quitter le réticulum endoplasmique pour atteindre la surface cellulaire. Fait intéressant, les deux parties du chaînon léger substitut — VpreB et λ5 — peuvent contacter la chaîne lourde, mais seule λ5 est capable de conduire CH1 vers son état final et compétent pour le repliement. Lorsqu’il n’en est pas ainsi, le récepteur partiel est retenu et la cellule rejette effectivement cette chaîne lourde.
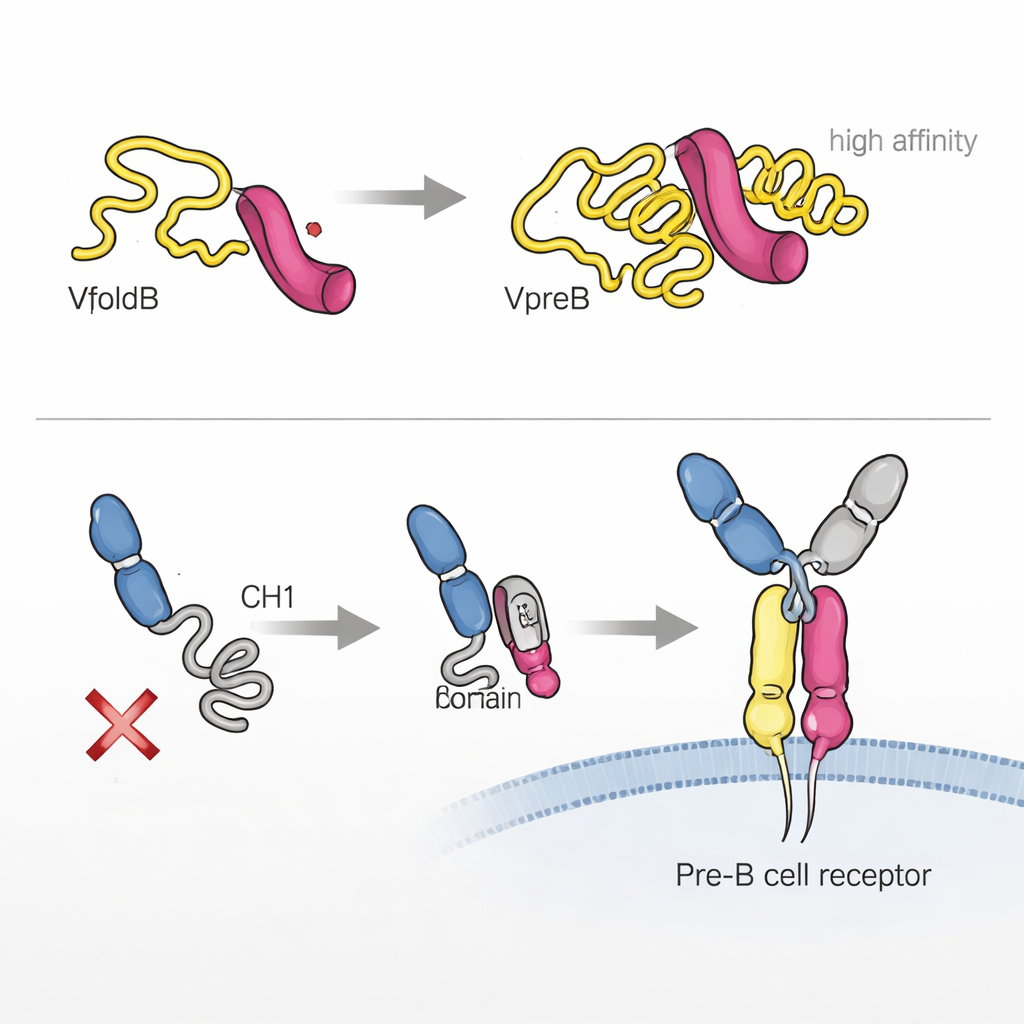
Queues flexibles qui ajustent la liaison et la signalisation
Tant VpreB que λ5 portent des segments mous et non structurés connus sous le nom de régions uniques, qui ne ressemblent à aucune séquence protéique connue. Bien que ces queues ne soient pas strictement nécessaires à l’assemblage des deux protéines in vitro, l’équipe a constaté qu’elles influencent fortement la vitesse de formation du chaînon léger substitut, sa stabilité et son affinité pour des segments de la chaîne lourde. Dans les cellules, la suppression de ces régions réduisait l’efficacité de la sécrétion des complexes assemblés. La queue de λ5 en particulier apparaît comme multifonction : elle accélère l’assemblage, est essentielle pour certains contacts avec la région variable de la chaîne lourde, et contribue largement à la manière dont le récepteur pré‑B interagit avec les antigènes et autres ligands. Dans certains cas, l’affinité de liaison d’une combinaison chaînon léger substitut–chaîne lourde approchait celle d’un fragment d’anticorps normal.
Pourquoi cela compte pour la diversité des anticorps
En cartographiant ces événements progressifs de repliement et d’assemblage, les auteurs proposent que le chaînon léger substitut ne se contente pas de maintenir la chaîne lourde en place. Il agit comme un inspecteur dynamique, utilisant son noyau structuré et ses queues flexibles pour détecter si une chaîne lourde peut se replier correctement et interagir de manière productive avec des cibles potentielles. Les combinaisons réussies sont repliées, stabilisées et autorisées à atteindre la surface cellulaire, où elles envoient des signaux permettant au lymphocyte B de poursuivre sa maturation. Les combinaisons défectueuses sont piégées puis éliminées. Pour le non‑spécialiste, la conclusion est que votre système immunitaire exécute un « banc d’essai » sophistiqué pour les futurs anticorps, composé de protéines qui se replient mutuellement, garantissant que seuls des noyaux d’anticorps bien comportés progressent pour vous défendre.
Citation: König, J., Sarmiento Alam, N.C., He, R. et al. Association-induced folding governs surrogate light chain and pre-B cell receptor core assembly. Nat Commun 17, 1202 (2026). https://doi.org/10.1038/s41467-026-68965-5
Mots-clés: développement des lymphocytes B, repliement des anticorps, chaînon léger substitut, contrôle de qualité des protéines, récepteur pré‑B