Clear Sky Science · fr
Déverrouiller la déracémisation enzymatique d’allènes structurellement diversifiés par des photoenzymes conçus
Pourquoi l’association de molécules compte
Beaucoup de médicaments ne sont actifs que lorsque leurs atomes sont disposés d’une façon tridimensionnelle très précise, un peu comme une main gauche qui n’entre que dans un gant gauche et pas dans un gant droit. Les chimistes savent souvent produire ces molécules « à main unique », mais il est difficile de le faire proprement lorsque les blocs de construction sont complexes. Cet article relève ce défi pour une catégorie délicate de structures torsadées appelées allènes en utilisant des enzymes photo‑activées conçues sur mesure. Le travail montre comment la biologie et la photochimie peuvent être combinées pour trier la « main » moléculaire désirée à partir d’un mélange brouillé, ouvrant la voie à des routes plus rapides et plus propres vers de futurs médicaments et matériaux.
Des briques tournées qui rapportent gros
Les allènes sont des chaînes linéaires de trois atomes de carbone avec deux doubles liaisons adjacentes, mais cette simple disposition tord l’espace d’une manière qui confère à la molécule une chiralité. Ces torsions axiales apparaissent dans des produits naturels, des agents de protection des cultures et des catalyseurs avancés. Malheureusement, les méthodes traditionnelles pour fabriquer des allènes chiraux ont tendance à être très spécialisées : un catalyseur qui fonctionne parfaitement pour un allène échoue souvent pour un autre présentant de petites différences structurelles. Même les catalyseurs chimiques activés par la lumière développés récemment peinent à surmonter ce problème. En conséquence, les chimistes doivent souvent repenser des catalyseurs de zéro à chaque nouvel allène étudié, ralentissant la découverte et augmentant les déchets.
Emprunter la sélectivité de la nature et y ajouter la lumière
Les enzymes des systèmes vivants excellent à reconnaître et transformer des formes spécifiques avec une précision remarquable, mais elles ont évolué pour des cibles naturelles, pas pour des allènes artificiels. Les auteurs se sont donné pour objectif de créer une « photoenzyme » qui combine la sélectivité d’une enzyme et la capacité à exploiter la lumière comme source d’énergie. Ils sont partis d’un échafaudage protéique appelé CTB10 et l’ont reconfiguré génétiquement pour intégrer un acide aminé non naturel qui joue le rôle d’une petite antenne lumineuse intégrée. Quand ce bloc spécial absorbe des rayons ultraviolets, il peut transférer de l’énergie à un allène voisin, l’excitant temporairement et permettant que sa torsion soit brouillée. En répétant ce processus de nombreuses fois, l’enzyme peut sélectionner et éliminer une « main » d’un mélange 50:50 et laisser en grande partie l’autre.
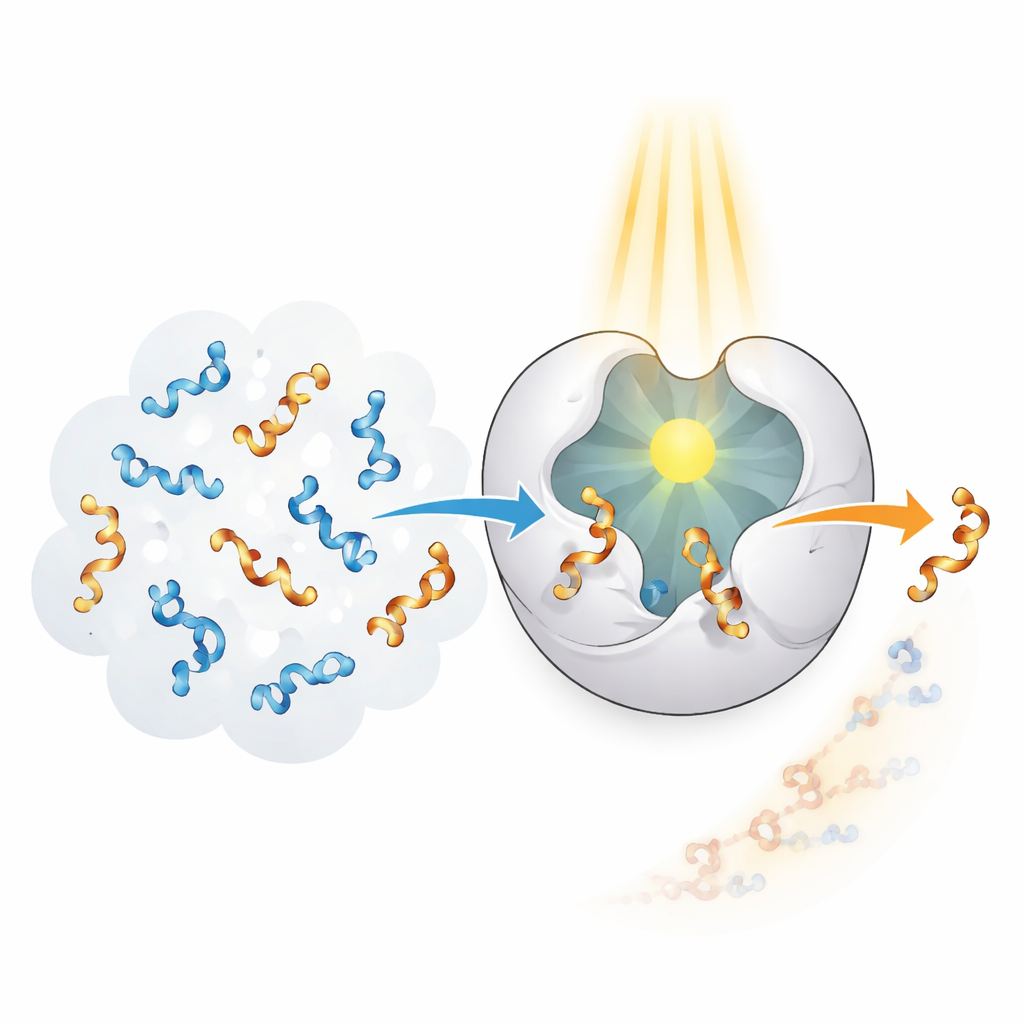
Sculpter des poches ajustées pour de nombreux invités
Concevoir un tel système n’est pas aussi simple que d’éclairer une protéine. L’équipe a utilisé la modélisation informatique, des mutations ciblées et des clichés par rayons X pour sculpter plusieurs versions de la photoenzyme, chacune avec une poche interne légèrement différente. Ces poches maintiennent l’allène dans une pose définie à côté de l’antenne lumineuse et stabilisent des parties clés de la molécule par des liaisons hydrogène et des interactions d’empilement subtiles. Pas à pas, les chercheurs ont amélioré à la fois l’affinité de liaison et l’alignement entre l’enzyme et l’allène, éléments cruciaux pour un transfert d’énergie efficace. Les variantes finales ont montré des performances impressionnantes, convertissant des acides carboxyliques, esters et amides d’allènes en produits majoritairement d’une seule main avec une pureté très élevée, souvent supérieure à 99 % d’un seul sens de chiralité, et ce en présence d’air sans conditions délicates.
Observer le mécanisme à résolution atomique
Pour comprendre pourquoi les nouvelles photoenzymes préfèrent une main plutôt qu’une autre, les auteurs ont cristallisé des paires enzyme–substrat et les ont examinées à résolution atomique. Ils ont constaté que la main d’allène favorisée se place plus près du groupe collecteur de lumière et peut adopter plusieurs conformations légèrement différentes, toutes compatibles avec un transfert d’énergie efficace. La main défavorisée se lie soit faiblement, soit se situe plus éloignée, la rendant beaucoup moins susceptible d’être excitée. Des expériences supplémentaires avec des matériaux de départ purement droits ou gauches ont confirmé ce biais : l’enzyme convertit rapidement la main préférée en un intermédiaire réactif, qui se relâche ensuite en solution pour reformer un mélange où l’autre main s’accumule. En essence, la protéine agit comme un tourniquet moléculaire, excitant et consommant de façon répétée une main tout en laissant l’autre s’accumuler.
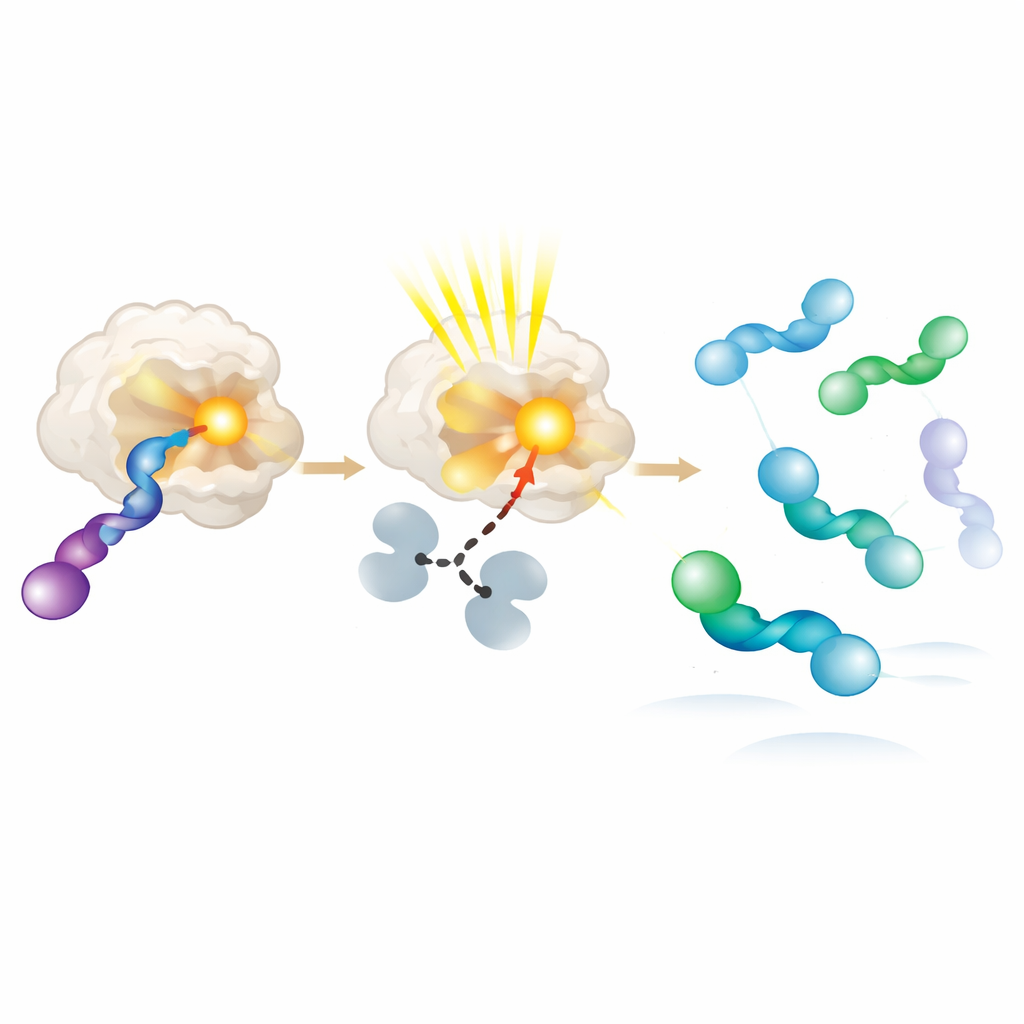
Ce que cela signifie pour la chimie de demain
Pour les non‑spécialistes, le message principal est que l’équipe a créé une machine protéique programmable qui utilise la lumière pour trier et améliorer des molécules torsadées avec une polyvalence sans précédent. Au lieu de concevoir un catalyseur chimique entièrement nouveau pour chaque cible, les chercheurs peuvent désormais partir de cette plate‑forme de photoenzyme et ajuster sa poche interne pour accepter de nombreux allènes différents. Cette approche réduit l’écart entre le contrôle exquis de la nature et le besoin de l’industrie chimique pour des méthodes larges et robustes. À long terme, de telles enzymes actionnées par la lumière pourraient aider les chimistes à préparer des blocs de construction complexes et homogènes pour les médicaments et les matériaux de manière plus efficace, avec moins d’étapes et moins de déchets.
Citation: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
Mots-clés: photoenzyme, déracémisation, allène chiral, biocatalyse, transfert d’énergie triplet