Clear Sky Science · fr
Synthèse de poly(ester disulfide)s par polymérisation par addition à croissance par étapes impliquant S8 à température ambiante
Transformer le soufre de déchet en plastiques intelligents
La vie moderne repose sur les plastiques, mais la plupart sont fabriqués à partir d’ingrédients coûteux et sont difficiles à recycler ou à décomposer en toute sécurité. Cette étude montre comment un déchet industriel — le soufre élémentaire jaune issu du raffinage du pétrole — peut être transformé à température ambiante en une nouvelle famille de plastiques intelligents. Ces matériaux sont non seulement résistants et extensibles, mais peuvent aussi être décomposés sur commande, ouvrant des perspectives pour des emballages plus verts, des dispositifs médicaux et des outils de dépollution.
Des résidus de raffinerie à des matériaux utiles
Chaque année, les raffineries produisent quelque 80 millions de tonnes de soufre élémentaire qui restent souvent inutilisées dans d’immenses stocks. Les chimistes savent depuis longtemps que le soufre peut former des polymères, ces longues chaînes qui constituent les plastiques, mais le faire réagir a exigé de fortes températures, des conditions agressives ou des précurseurs compliqués. Les méthodes antérieures produisaient des solides cassants et vitreux ou reposaient sur des composés sulfurés cycliques difficiles à synthétiser en grande quantité. Le défi consistait à trouver une manière simple et douce de transformer cet élément abondant et peu coûteux en matériaux modulables offrant des performances adaptées au monde réel.
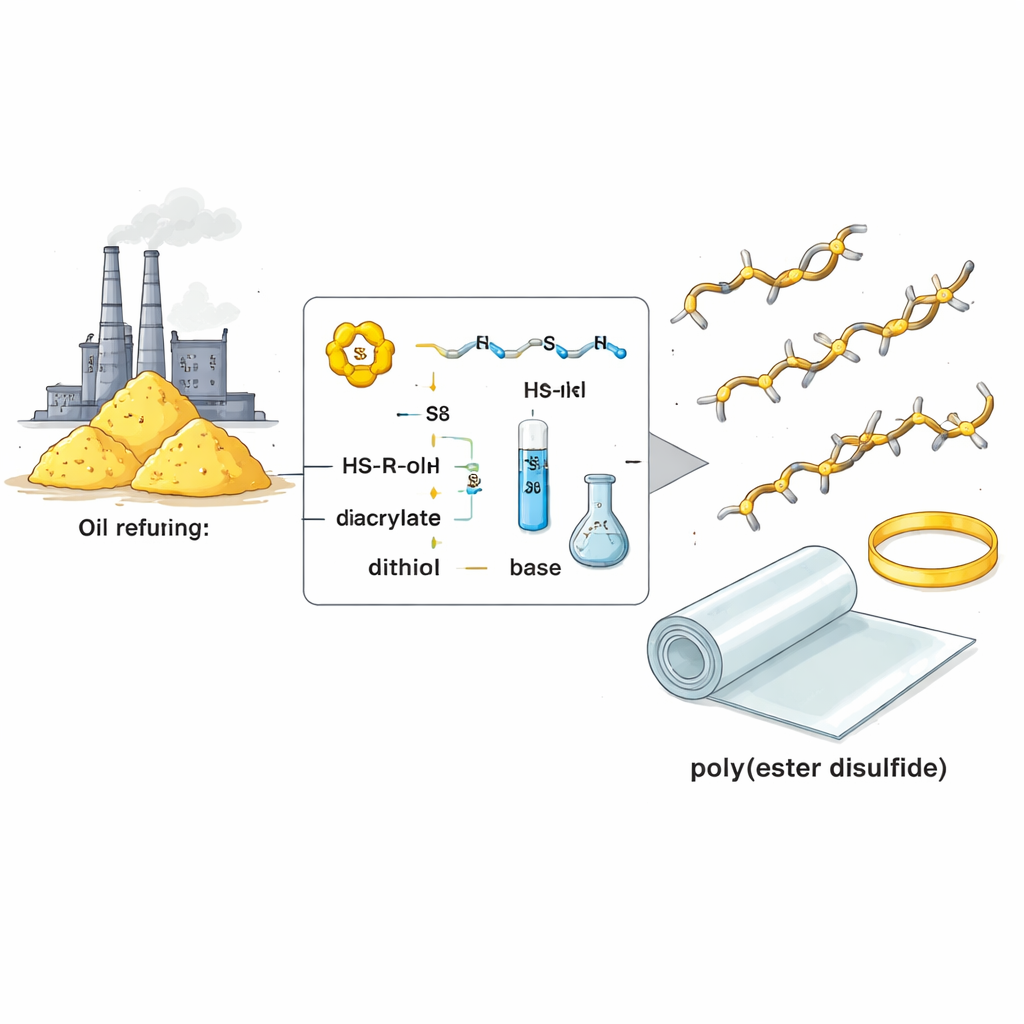
Une assemblage chimique doux en trois étapes
Les chercheurs ont mis au point une recette à température ambiante qui combine trois ingrédients largement disponibles : du soufre élémentaire, de petites molécules portant deux groupes soufre–hydrogène (dithiols), et de petites molécules comportant deux doubles liaisons carbone–carbone adjacentes à des groupes ester (diacrylates). Avec une toute petite quantité d’une base organique comme catalyseur, les cycles de soufre s’ouvrent et se lient aux dithiols, puis s’additionnent proprement aux diacrylates. Le résultat est une chaîne polymère composée d’unités ester alternant avec des liaisons soufre–soufre. Des analyses approfondies ont montré que cette réaction est très sélective : elle évite les sous-produits courants et convertit les réactifs en blocs constructeurs souhaités avec un rendement supérieur à 95 %.
Comment la réaction choisit sa voie
Pour comprendre pourquoi la chimie fonctionne de manière si fiable à température ambiante, l’équipe a utilisé des calculs quantum-chimiques pour cartographier les étapes réactionnelles. La base arrache d’abord un proton au dithiol, créant une espèce sulfurée réactive qui attaque l’anneau de soufre (S8) et l’ouvre. Cette courte chaîne de soufre se lie ensuite rapidement à la double liaison de l’acrylate par une addition de type Michael. Un échange rapide entre liaisons soufre–soufre redistribue les atomes en trois produits étroitement liés qui ont tous des énergies presque identiques, ce qui explique leur formation en proportions voisines. Des expériences par résonance magnétique nucléaire, spectrométrie de masse, spectroscopie Raman et spectroscopie photoélectronique X confirment que les polymères finaux contiennent le mélange prévu d’unités ester et de liaisons disulfure sans soufre élémentaire résiduel ni longues chaînes de polysulfures.
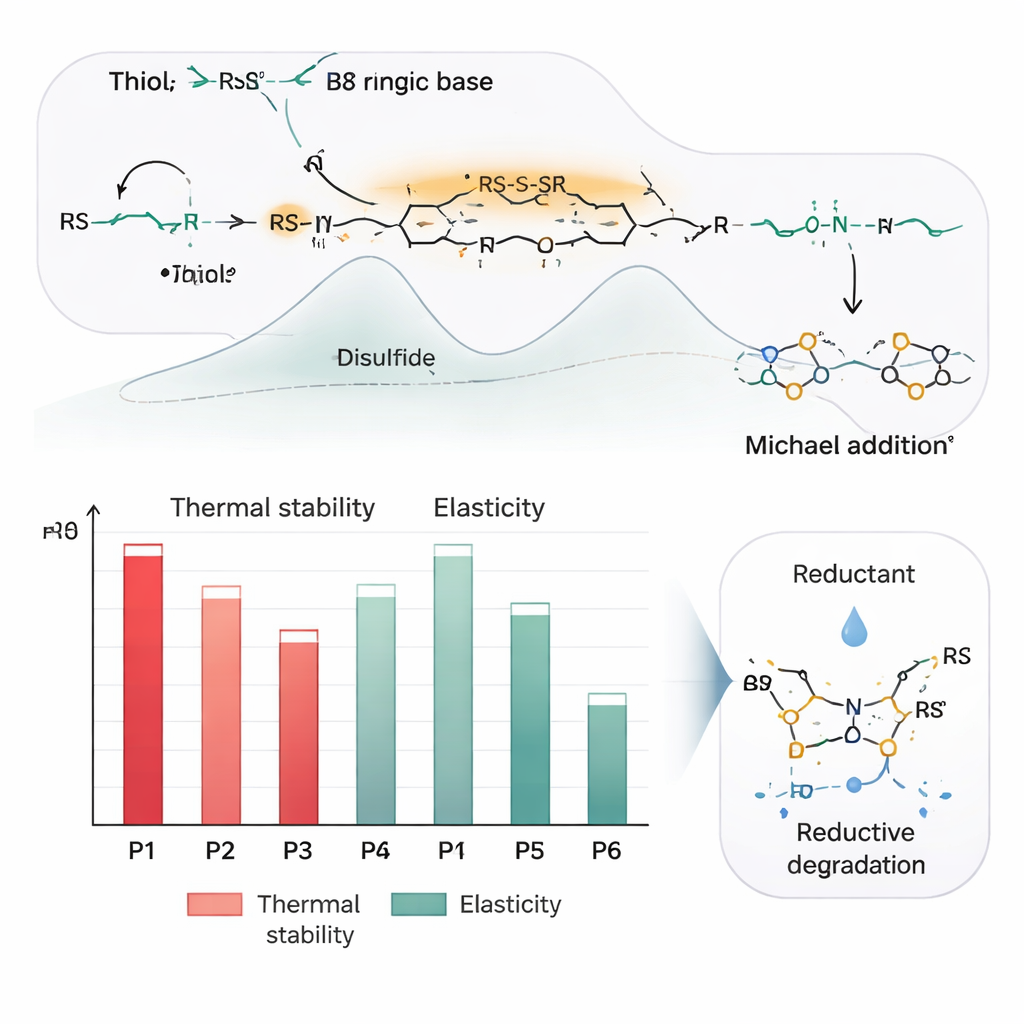
Des plastiques avec souplesse intégrée et bouton d’autodestruction
En choisissant différents dithiols et diacrylates, les scientifiques ont pu obtenir une gamme de comportements physiques. Certaines combinaisons ont donné des matériaux mous et caoutchouteux avec des températures de transition vitreuse très basses — si flexibles qu’un échantillon pouvait s’étirer à plus de vingt fois sa longueur initiale et revenir comme un élastique. D’autres, contenant des unités rigides en anneau ou des groupes supplémentaires formant des liaisons hydrogène, sont devenus plus résistants et plus cristallins, avec des points de fusion au-dessus du point d’ébullition de l’eau et des résistances à la rupture plus élevées. Tous ces polymères supportent des températures d’environ 250 °C avant de commencer à se décomposer, ce qui les rend suffisamment robustes pour des usages exigeants. Pourtant, leurs liaisons soufre–soufre restent sensibles à des agents réducteurs doux, tels que le dithiothréitol, qui peuvent scinder les chaînes en petites molécules en quelques heures. Cette dégradabilité activable ouvre la voie à un cycle de vie circulaire, dans lequel les produits peuvent être démontés pour recyclage ou élimination sécurisée.
Ce que cela signifie pour les plastiques de demain
En termes simples, ce travail transforme un flux de déchets problématique en une boîte à outils pour les plastiques de nouvelle génération. En n’utilisant que la température ambiante, des solvants courants et de petites quantités de catalyseurs organiques, les auteurs ont créé des polymères riches en soufre avec une résistance, une extensibilité et une capacité de désassemblage programmables. Parce que la chimie est modulaire, les concepteurs futurs pourront combiner les blocs de construction pour programmer le comportement de ces matériaux dans le corps, dans l’environnement ou en milieu industriel. Pour les non-spécialistes, le message principal est que le sous-produit des raffineries d’hier peut devenir le plastique intelligent et dégradable de demain — aidant à rapprocher performance et durabilité.
Citation: Sun, Y., Cao, Y., Liu, X. et al. Synthesis of poly(ester disulfide)s from S8-involved step-growth addition polymerization at ambient temperature. Nat Commun 17, 2066 (2026). https://doi.org/10.1038/s41467-026-68963-7
Mots-clés: polymères de soufre, plastiques à liaisons covalentes dynamiques, matériaux biodégradables, élastomères recyclables, chimie des polymères verte