Clear Sky Science · fr
L’infection par le HCMV perturbe les fonctions de barrière et favorise la transition épithélio–mésenchymateuse dans un modèle d’organoïde de cholangiocytes
Pourquoi cette histoire de virus dans le foie compte
Le cytomégalovirus humain est un virus très fréquent que la plupart d’entre nous portent sans le savoir. Pourtant, chez les nouveau-nés et les personnes immunodéprimées, il peut être associé à des problèmes hépatiques et biliaires graves, y compris une maladie infantile rare mais dévastatrice appelée atrésie des voies biliaires. Cette étude utilise de petits conduits biliaires humains cultivés en laboratoire pour montrer comment le virus peut directement endommager ces tubes fragiles et déclencher des modifications cicatricielles qui pourraient aider à expliquer les liens, longtemps débattus, entre infection et maladie hépatique chronique.
Un regard plus attentif sur un virus courant mais discret
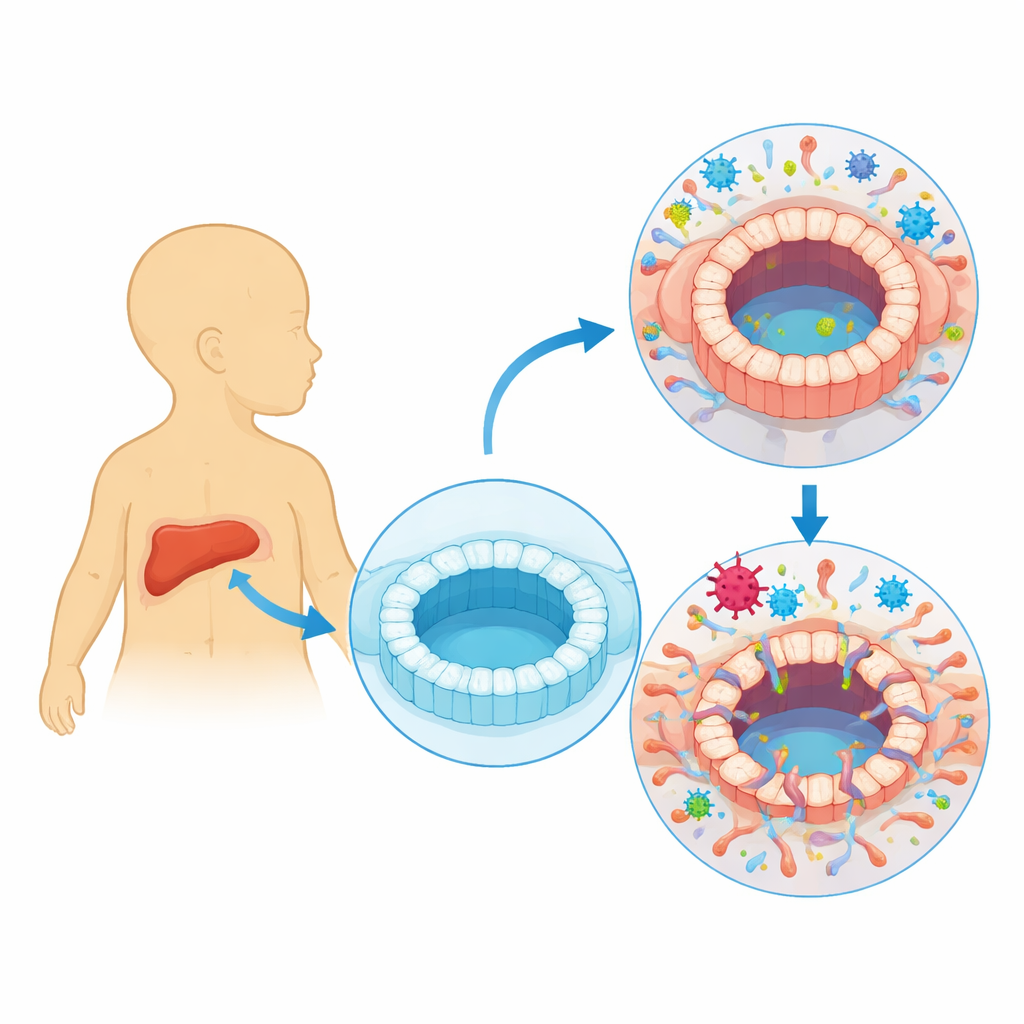
Le cytomégalovirus humain (HCMV) vit généralement de façon silencieuse dans notre organisme, alternant entre une phase active, où il produit de nouvelles particules virales, et une phase latente, où il se dissimule dans certains globules sanguins. Les cliniciens ont depuis longtemps observé que des personnes présentant une infection manifeste par le HCMV peuvent développer des lésions des voies biliaires et une cholestase, dans laquelle la bile ne s’écoule pas correctement. De nombreux nourrissons atteints d’atrésie des voies biliaires — une affection où les voies biliaires se bouchent et se cicatrisent peu après la naissance — présentent aussi des signes d’infection récente par le HCMV. Il restait cependant incertain si le virus infectait réellement les cellules qui tapissent les voies biliaires ou s’il était simplement présent comme un témoin lors de la maladie.
Construire de minuscules voies biliaires en laboratoire
Pour répondre à cette question, les chercheurs ont créé des « organoïdes » tridimensionnels reproduisant des voies biliaires humaines. Ils ont commencé à partir de cellules souches pluripotentes induites, reprogrammées à partir de sang humain, et les ont orientées pour former des cellules de type cholangiocyte — le type cellulaire qui tapisse les voies biliaires. Ces cellules se sont auto-organisées en sphères creuses avec une cavité centrale et des jonctions cellule–cellule serrées, ressemblant à un mini-conduit biliaire. L’équipe a ensuite exposé ces organoïdes à une souche de HCMV marquée par un traceur fluorescent qui s’allume lorsque le virus réplique activement. Cela leur a permis de suivre les cellules infectées et de mesurer les modifications des organoïdes au fil du temps.
Comment l’infection déforme la structure et affaiblit la barrière
Une fois infectés, les organoïdes ont cessé de croître normalement et sont devenus déformés, avec des parois épaissies et irrégulières. Certaines cellules brillaient intensément, montrant une activité virale complète et la production de nouvelles particules ; d’autres contenaient du matériel génétique viral à des niveaux plus faibles, suggérant un état plus dormant, proche de la latence. Des tests fonctionnels ont révélé que les organoïdes infectés avaient perdu des fonctions clés des voies biliaires. Ils ne gonflaient plus correctement en réponse à un stimulus dépendant des canaux de transport d’ions, et ils fuyaient davantage dans un essai de résistance électrique mesurant l’étanchéité de la barrière. Les protéines qui scellent normalement les espaces entre les cellules, comme les composants des jonctions serrées, étaient réduites, et le transport d’un colorant test vers et depuis la cavité interne était anormal. Ensemble, ces changements montrent que le HCMV peut compromettre directement la paroi des voies biliaires, la rendant perméable et dysfonctionnelle.
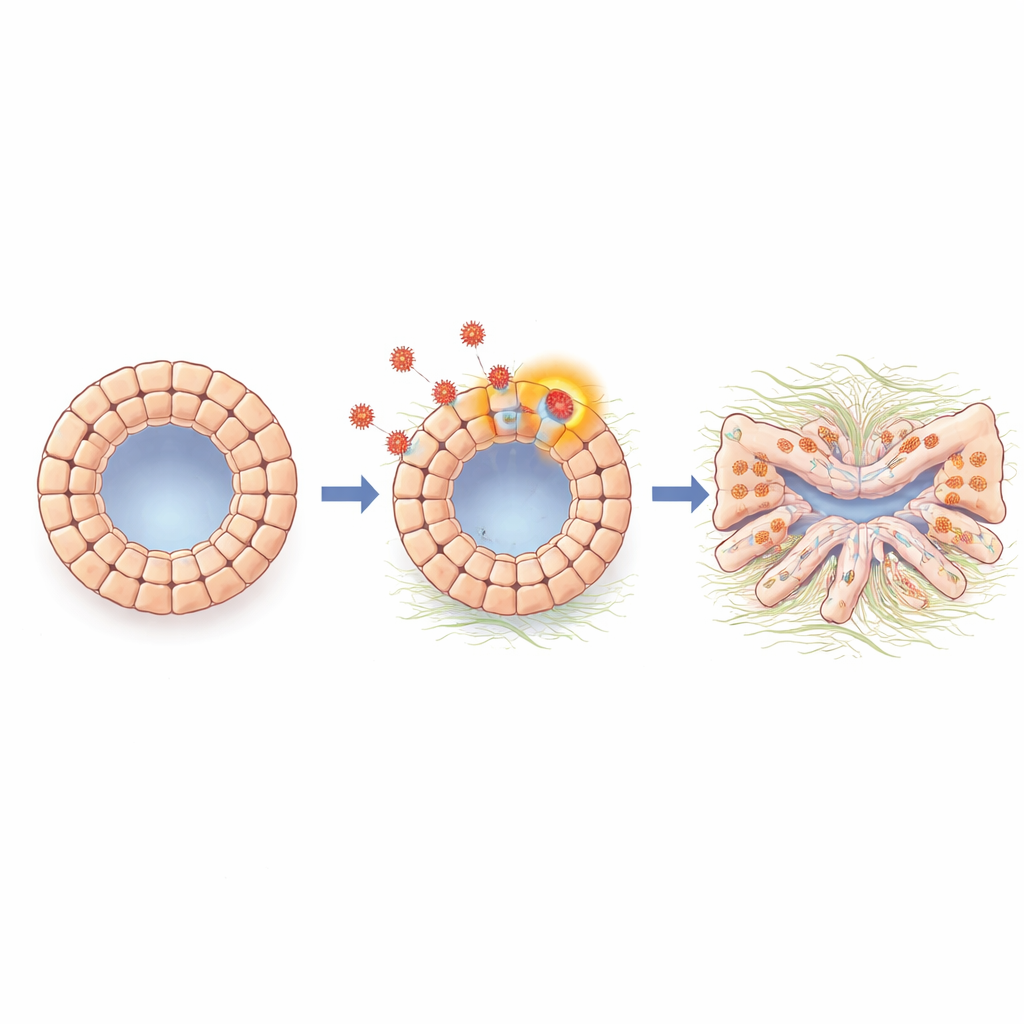
Les cellules changent d’identité vers un état cicatriciel
En approfondissant l’analyse, les scientifiques ont étudié l’activité génique des organoïdes en masse et à la résolution d’une seule cellule. Ils ont observé une forte activation d’un programme ressemblant à la transition épithélio–mésenchymateuse, un processus par lequel des cellules de surface étroitement connectées assouplissent leurs liens, adoptent un caractère plus mobile et fibreux, et commencent à produire des molécules associées à la cicatrisation tissulaire. Les organoïdes infectés présentaient des niveaux accrus de N-cadhérine et d’autres marqueurs liés à ce basculement, ainsi que des gènes impliqués dans la fibrose et la production de matrice. Une molécule de signalisation appelée TGF-bêta, bien connue pour stimuler la cicatrisation dans de nombreux organes, était renforcée pendant l’infection. Lorsque l’équipe a bloqué la signalisation TGF-bêta avec un inhibiteur petit-moléculaire ou un anticorps, les organoïdes ont repris une forme plus normale et beaucoup des gènes associés à la cicatrisation et à la transition sont revenus vers les niveaux de base, indiquant que le TGF-bêta est un intermédiaire clé reliant la présence virale aux changements cellulaires délétères.
Des tubes cultivés en laboratoire aux enfants malades
Pour savoir si ces observations de laboratoire se rapportent à la maladie réelle, les chercheurs ont examiné des tissus hépatiques d’enfants atteints d’atrésie des voies biliaires et d’autres affections hépatiques pédiatriques. À l’aide de sondes sensibles, ils ont détecté de l’ADN du HCMV dans les cholangiocytes — les cellules des voies biliaires — dans environ les deux tiers des échantillons d’atrésie des voies biliaires, mais beaucoup moins fréquemment dans les foies non atteints par l’atrésie. Dans les mêmes régions où l’ADN viral était présent, les cellules biliaires présentaient des niveaux plus élevés de TGF-bêta et de N-cadhérine, correspondant au profil de transition et de cicatrisation observé dans les organoïdes. Cela suggère que, dans au moins une sous-partie des enfants, le HCMV infecte directement les cellules des voies biliaires et les incline vers un état fibrotiques en activant des voies dépendantes du TGF-bêta.
Ce que cela implique pour la compréhension et le traitement des maladies des voies biliaires
En termes simples, ce travail montre qu’un virus fréquent peut envahir les cellules qui tapissent les voies biliaires, assouplir leurs jonctions serrées et les pousser vers une identité cicatricielle et moins spécialisée via une signalisation basée sur le TGF-bêta. Ces changements affaiblissent les fonctions de barrière et de transport des conduits et peuvent contribuer aux voies biliaires obstruées et fibreuses observées dans des maladies comme l’atrésie des voies biliaires. Si tous les cas de maladies biliaires ne sont pas causés par le HCMV, l’étude renforce l’idée que, chez les nourrissons vulnérables, l’infection virale pourrait être un élément important du puzzle — et que cibler les voies liées au TGF-bêta pourrait un jour aider à protéger ou restaurer des voies biliaires fragiles.
Citation: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
Mots-clés: cytomégalovirus, atrésie des voies biliaires, organoïdes de voies biliaires, transition épithélio-mésenchymateuse, signalisation TGF-bêta