Clear Sky Science · fr
Alkylation N énantioconvergente catalysée par le cuivre des hydrazines avec des α‑haloamides racémiques pour accéder à des hydrazines enrichies en énantiomères
Pourquoi ces petites molécules comptent
De nombreux médicaments modernes et composés candidates dans le domaine pharmaceutique contiennent une petite mais puissante unité appelée hydrazine. Lorsque cette unité est « orientée » — c’est‑à‑dire qu’elle existe principalement sous une forme image‑miroir plutôt que sous un mélange 50:50 — cela peut modifier profondément le comportement d’une molécule dans l’organisme. L’étude à l’origine de cet article présente une nouvelle voie efficace pour obtenir de telles hydrazines en configuration unique (chiralité) à partir de matières premières bon marché et largement disponibles, ce qui pourrait simplifier la conception de nouveaux médicaments et de molécules bioactives.
Des ingrédients simples à des produits précis
Les auteurs se concentrent sur deux types de blocs de construction simples : les hydrazines et les α‑haloamides racémiques. Les hydrazines possèdent une paire azote–azote et sont fréquentes en pharmacologie, dans des structures proches des peptides et dans des systèmes cycliques riches en azote. Les α‑haloamides racémiques sont des composés faciles à préparer où un carbone réactif est adjacent à la fois à un halogène (comme le chlore ou le brome) et à un groupe amide. Si l’on pouvait lier ces deux partenaires de manière contrôlée, cela offrirait un accès direct à des hydrazines chirales sans devoir préassembler des intermédiaires plus complexes. Jusqu’à présent, les méthodes existantes nécessitaient souvent plusieurs étapes, des réactifs oxydés instables ou étaient limitées à des partenaires particuliers peu représentatifs des molécules réelles.
Un nouveau rôle pour le cuivre comme guide moléculaire
Pour résoudre ce problème, l’équipe a conçu un catalyseur à base de cuivre capable de transformer un mélange racémique d’α‑haloamides en un produit préférentiel d’une seule configuration lorsqu’il est associé à des hydrazines. Plutôt que la voie classique de formation de liaison en deux électrons, qui peine face à des hydrazines nucléophiles et susceptibles d’empoisonner le catalyseur, ils exploitent un mécanisme de crossover radical‑polaire. Dans la première phase, le complexe cuivre intervient par chimie à électron unique pour arracher un atome d’halogène à l’α‑haloamide, générant un radical transitoire lié au métal. Ce radical recombine alors au sein du centre en cuivre pour donner un complexe cuivre hautement réactif et polarisé positivement. Dans la seconde phase, l’hydrazine attaque ce partenaire activé depuis un côté contrôlé, de sorte qu’une seule image‑miroir est formée avec une grande sélectivité.
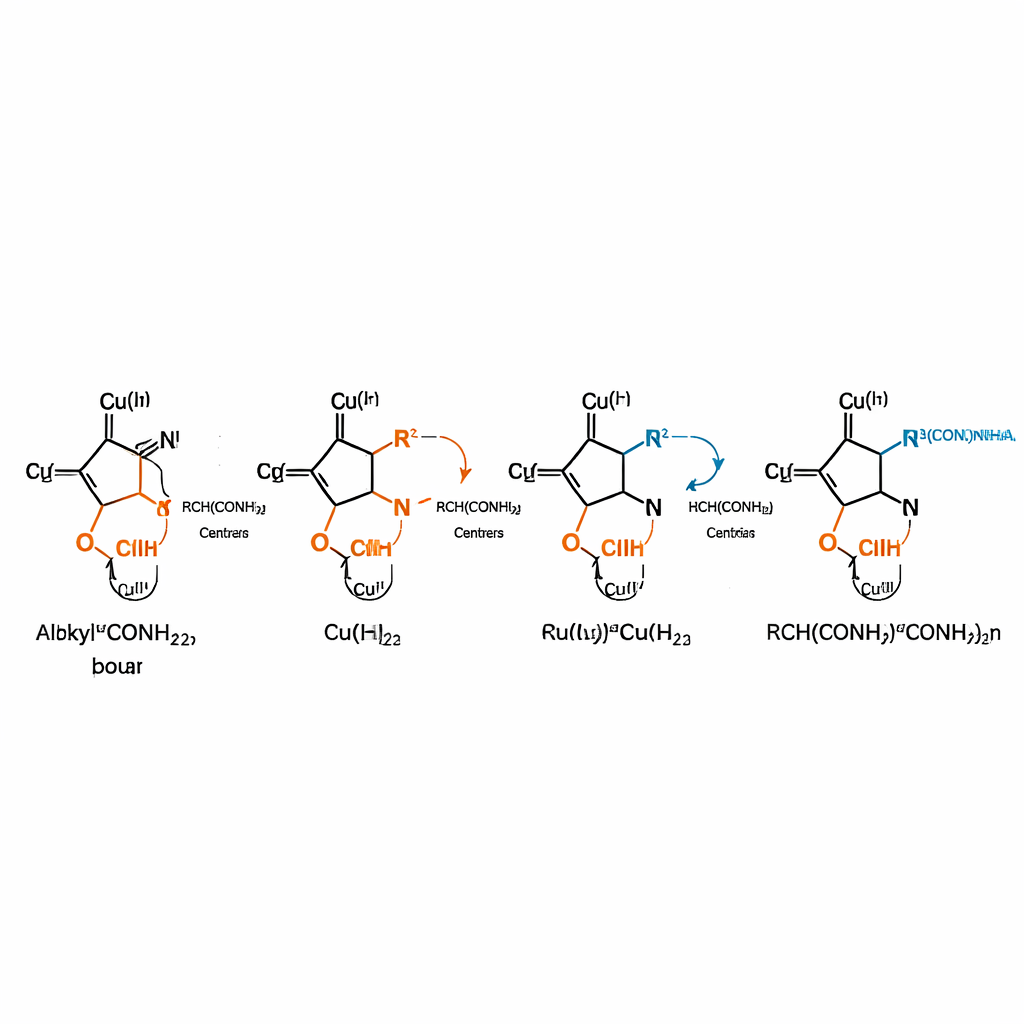
Ajuster la recette pour une utilisation large et pratique
Un élément clé de cette avancée réside dans la conception du ligand chiral qui enrobe l’atome de cuivre. Les chercheurs ont découvert qu’un ligand N,N,N tridentate, chargé négativement — un échafaudage à trois branches riche en azote — est crucial. Il se lie fermement, augmente la puissance réductrice du cuivre pour favoriser la formation rapide des radicaux et stabilise l’étape hautement énergique du cuivre(III) où la sélectivité se fixe. En testant systématiquement différents groupes protecteurs sur l’hydrazine, ils ont identifié la N,N‑bis‑Boc comme partenaire idéale : elle dirige la réaction vers un seul site azoté, résiste aux conditions de transformation et peut ensuite être délicatement retirée pour révéler l’hydrazine chirale libre. Dans des conditions optimisées et douces, ce système convertit des dizaines d’α‑haloamides racémiques en hydrazines chirales avec de bons rendements et d’excellentes puretés énantiomériques, que le carbone de départ soit lié à des cycles aromatiques ou à des chaînes alkyle simples.
Construire des peptides et des cycles à forme précise
La puissance de cette plate‑forme devient évidente lorsqu’on l’applique à des blocs de construction plus complexes. En utilisant des α‑haloamides dérivés d’acides aminés naturels, l’équipe a préparé des N‑amino dipeptides — courts fragments de type peptide dans lesquels un azote est remplacé par une hydrazine. Ces unités N‑amino sont connues pour stabiliser des conformations peptidiques inhabituelles et résister à la dégradation enzymatique, ce qui les rend attractives en conception de médicaments. Remarquablement, en associant soit la version normale soit l’image‑miroir du ligand chiral avec des matières premières issues d’acides aminés de l’une ou l’autre configuration, les chimistes ont pu accéder aux quatre stéréoisomères possibles d’un dipeptide N‑amino donné. Ce contrôle « stéréodivergent » signifie qu’à partir des mêmes entrées simples, on peut obtenir un panel complet de variantes de forme pour des tests biologiques.
Des blocs de construction à des structures complexes
Une fois les hydrazines protégées formées, leurs groupes protecteurs peuvent être ôtés pour donner des hydrazines chirales libres sous forme de sels stables. Celles‑ci réagissent ensuite aisément avec de simples composés carbonylés pour former une gamme de systèmes cycliques riches en azote — comme des pyrazoles, des phthalazinones et des hybrides peptides‑cycles fusionnés — tout en préservant leur caractère énantiomérique. Les auteurs montrent également que la chimie peut être montée en échelle sans perte d’efficacité, une étape importante vers une utilisation concrète. Dans l’ensemble, ce travail fournit une voie modulaire et directe, à partir de matériaux disponibles, vers des hydrazines chirales finement ajustées et leurs dérivés.
Ce que cela implique pour l’avenir
Pour un non‑spécialiste, le message principal est que les chercheurs ont appris à un catalyseur métallique peu coûteux, le cuivre, à prendre un mélange désordonné de pièces de départ et à les assembler en un produit « orienté » précis, sur demande. Parce que ces hydrazines chirales peuvent être facilement transformées en peptides et en cycles riches en azote — éléments centraux de nombreux médicaments — cette méthode offre un raccourci puissant pour les chimistes médicinaux et les biologistes chimiques. Elle devrait faciliter et accélérer l’exploration de l’effet de la forme moléculaire sur l’activité biologique, aidant en fin de compte à identifier de nouveaux candidats thérapeutiques et matériaux fonctionnels.
Citation: Li, N., He, SY., Wang, PF. et al. Copper-catalysed enantioconvergent N-alkylation of hydrazines with racemic α-haloamides to access enantioenriched hydrazines. Nat Commun 17, 2070 (2026). https://doi.org/10.1038/s41467-026-68961-9
Mots-clés: hydrazines chirales, catalyse au cuivre, crossover radical‑polaire, synthèse énantiosélective, N‑amino peptides