Clear Sky Science · fr
Comprendre la promotion par les métaux alcalins en catalyse d’hydrogénation via l’interaction forte métal‑base
Pourquoi ajuster les catalyseurs compte dans la vie quotidienne
Transformer des molécules simples comme le dioxyde de carbone et l’hydrogène en combustibles et produits chimiques utiles est au cœur d’une énergie plus propre et d’une industrie plus verte. De nombreux catalyseurs métalliques qui pilotent ces réactions contiennent déjà de faibles quantités de métaux alcalins tels que le sodium ou le potassium comme « promoteurs », mais leur rôle réel est resté étonnamment flou. Cette étude met au jour un principe unificateur expliquant le fonctionnement de ces additifs, offrant une voie pour concevoir des catalyseurs plus intelligents capables d’orienter les réactions vers des produits désirés et d’éviter les déchets.
Un regard plus précis sur les catalyseurs renforcés
Les catalyseurs constitués de métaux de transition comme le rhodium et le nickel reposent sur des supports solides et aident à briser et reformer des liaisons chimiques. Depuis des décennies, l’industrie ajoute des métaux alcalins pour rendre ces catalyseurs plus actifs, plus sélectifs ou plus durables. Les explications habituelles mettaient l’accent sur des effets géométriques simples (modification de la forme et de la taille des particules) ou sur un don direct d’électrons de l’alcali vers le métal actif. Cependant, dans des conditions réelles de fonctionnement, ces promoteurs existent principalement sous forme d’oxydes, et non comme atomes métalliques nus, ce qui rend l’idée d’un transfert électronique direct incomplète.
Découverte d’un partenariat fort à la surface
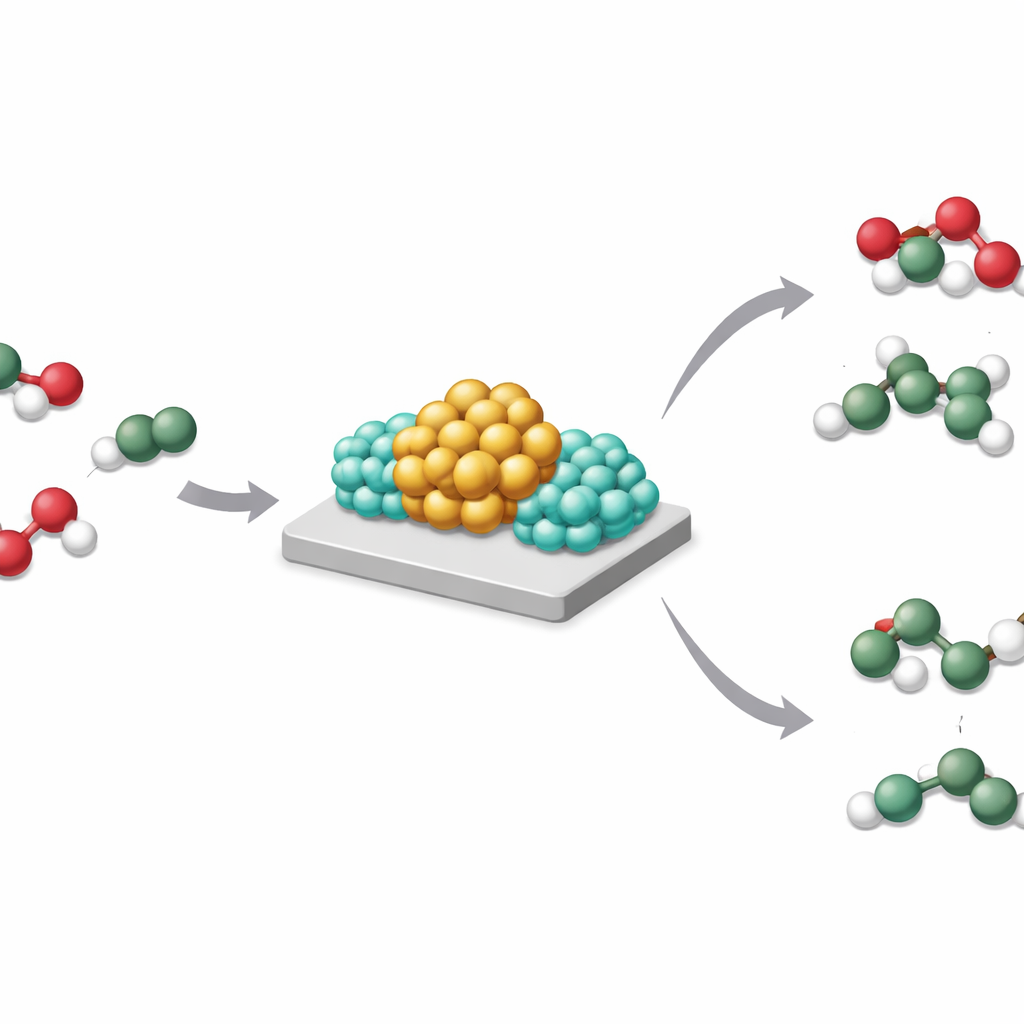
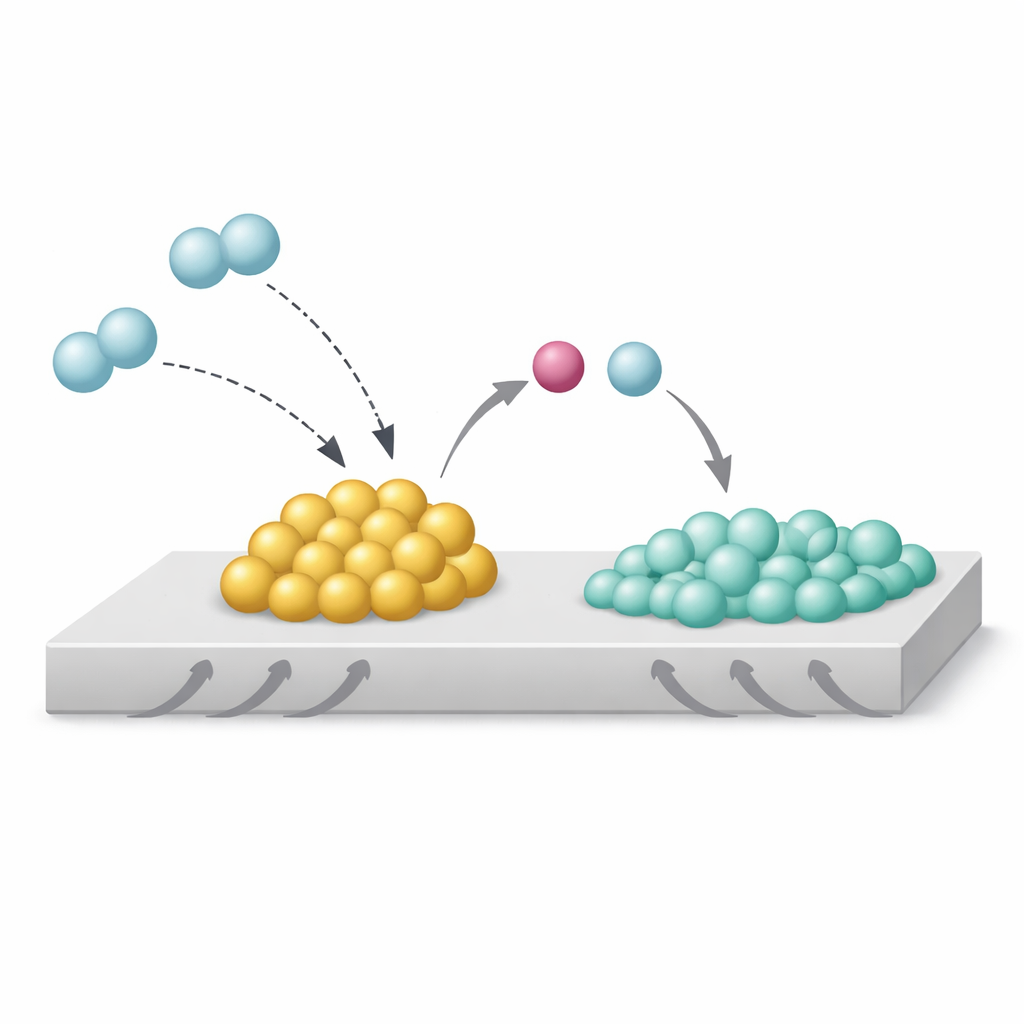
Les auteurs ont étudié un système modèle : des nanoparticules de rhodium sur du dioxyde de titane, avec et sans ajout de sodium. À l’aide de microscopie électronique avancée, de spectroscopies aux rayons X et de simulations informatiques, ils ont observé que le sodium se présente sous forme d’oxyde, Na₂O, précisément à la frontière où les particules de rhodium touchent le support. Sous hydrogène, cette configuration crée ce qu’ils appellent une Interaction Forte Métal‑Base, ou IFMB (SMBI en anglais). À ces points de contact particuliers, les molécules d’hydrogène se scindent de manière hétérogène : le Na₂O, plus basique, s’empare de la partie protons‑comme, tandis que le rhodium retient la partie riche en électrons. Cette coupure « hétérolytique » laisse la surface de rhodium exceptionnellement chargée en électrons et empêche l’hydrogène de se répandre, ou de « migrer », vers le support en dioxyde de titane.
Comment cet effet caché oriente les réactions
Cette réorganisation subtile de la localisation de l’hydrogène et des électrons a de grandes conséquences. Dans l’hydrogénation du dioxyde de carbone, le rhodium pur sur dioxyde de titane favorise une hydrogénation poussée jusqu’au méthane. Lorsqu’on ajoute du sodium, le même catalyseur produit principalement du monoxyde de carbone, un intermédiaire précieux, tout en générant beaucoup moins de méthane. Un comportement similaire apparaît avec du lithium ou du potassium, ou lorsque le rhodium est remplacé par du nickel. Les auteurs montrent que lorsque l’hydrogène peut librement migrer sur le support, l’hydrogénation profonde domine ; quand l’IFMB maintient l’hydrogène concentré à la frontière métal‑base et hors du support, des produits plus modérés sont favorisés.
Différentes doubles liaisons, différents résultats
L’équipe a ensuite étudié comment l’IFMB influence des réactions d’hydrogénation organique courantes impliquant des doubles liaisons carbone‑carbone, carbone‑oxygène et azote‑oxygène. Pour une double liaison carbone‑carbone dans l’acétate de vinyl, la promotion par le sodium rend le catalyseur plus rapide, probablement parce qu’un rhodium riche en électrons facilite l’affaiblissement de cette liaison tandis qu’un hydrogène plus faiblement lié s’y ajoute efficacement. En revanche, pour des molécules comme l’acétophénone et la nitrobenzène, dont les groupes réactifs préfèrent se fixer sur le support oxyde, le même ajout de sodium ralentit la réaction. Ici, la réduction du transfert d’hydrogène vers le support signifie que celui‑ci ne reçoit plus suffisamment d’hydrogène pour conduire ces transformations, montrant que toutes les doubles liaisons ne bénéficient pas de la même manière d’un même effet promoteur.
Concevoir des catalyseurs avec un contrôle intentionnel
En combinant expériences et théorie, les auteurs soutiennent que l’IFMB fournit une manière unifiée de comprendre comment les promoteurs alcalins reconfigurent les surfaces catalytiques. Plutôt que d’agir comme de simples donneurs d’électrons, les oxydes alcalins jouent le rôle de forts pièges à protons, forçant l’hydrogène à se scinder de façon polarisée et confinant l’hydrogène réactif près de l’interface métal‑base. Cette idée explique des tendances déroutantes observées sur de nombreuses réactions d’hydrogénation et différents métaux, et elle pointe vers une règle de conception pratique : en ajustant la quantité et la localisation des oxydes alcalins autour des particules métalliques, les chimistes peuvent consciemment orienter les réactions vers des produits spécifiques tout en optimisant l’activité et la stabilité pour des procédés chimiques plus propres.
Citation: Jung, M., Dickieson, M.P., Chen, P. et al. Understanding alkali metal promotion in hydrogenation catalysis through Strong Metal–Base Interaction. Nat Commun 17, 2465 (2026). https://doi.org/10.1038/s41467-026-68952-w
Mots-clés: catalyse d’hydrogénation, promoteurs métaux alcalins, conversion du CO2, catalyseurs hétérogènes, interfaces métal‑oxyde