Clear Sky Science · fr
RiboBright révèle des différences spécifiques aux types cellulaires dans l’organisation et le mouvement des ribosomes
Voir s’illuminer les usines à protéines de la cellule
Chaque seconde, chacune de nos cellules produit des milliers de nouvelles protéines à l’aide de petites machines appelées ribosomes. Jusqu’à présent, observer où ces machines se situent et comment elles se déplacent à l’intérieur des cellules vivantes était étonnamment difficile. Cette étude présente RiboBright, une petite molécule fluorescente qui se fixe aux ribosomes et les illumine, permettant aux scientifiques de suivre ces usines à protéines cellule par cellule. Le travail révèle que les ribosomes sont organisés et utilisés de manière très différente selon les types cellulaires, en particulier lorsque les cellules souches choisissent leur devenir.
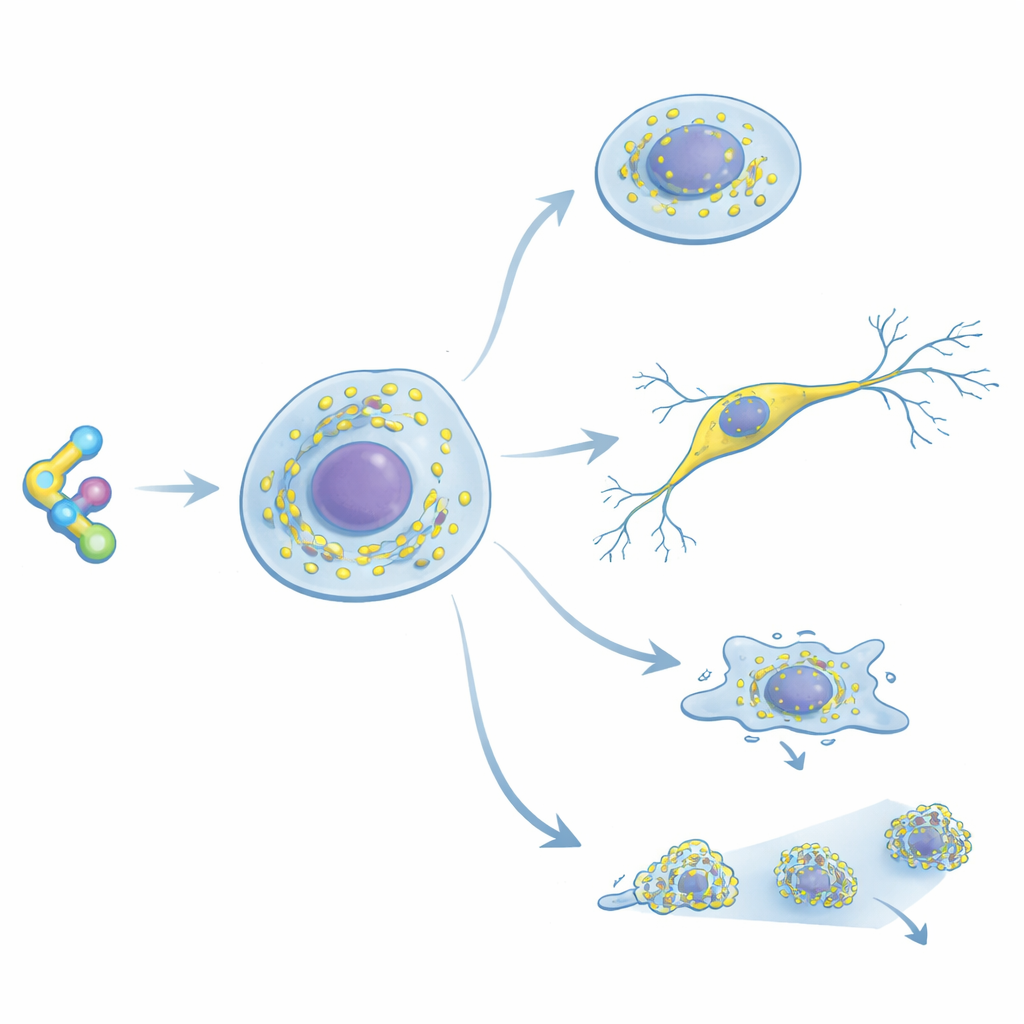
Une nouvelle façon de mettre en lumière les ribosomes
Les chercheurs ont conçu RiboBright en modifiant la cycloheximide, un médicament classique connu pour se lier de façon forte et sélective aux ribosomes chez les animaux et les humains. Ils ont attaché une teinture « rotor moléculaire » spéciale en un point du médicament qui n’affaiblit pas son ancrage au ribosome. Cette teinture scintille à peine lorsqu’elle tourne librement en solution, mais devient brillante lorsque son mouvement est restreint — comme lorsque la sonde s’insère dans le ribosome. Des tests en éprouvette ont montré que les molécules modifiées inhibent toujours la production de protéines à des doses presque identiques à celles du médicament d’origine, confirmant une bonne affinité. Dans les cellules vivantes, une version en particulier a produit des taches nettes et lumineuses, indiquant qu’elle trouvait le bon équilibre entre liaison étroite au ribosome et forte émission lumineuse ; cette sonde optimisée a été nommée RiboBright.
Prouver que la sonde cible de vrais ribosomes
Pour s’assurer que RiboBright marque réellement les ribosomes, l’équipe a combiné plusieurs approches complémentaires. Lorsque les cellules étaient prétraitées soit avec la cycloheximide elle-même, soit avec un autre composé bloquant les ribosomes sans lien apparent, le signal RiboBright disparaissait presque complètement, ce qui implique que les trois composés entrent en compétition pour le même site de liaison. Des sondages chimiques de l’ARN ribosomal ont en outre montré que RiboBright protège le même nucléotide que la cycloheximide, cohérent avec un site d’ancrage identique. La microscopie à haute résolution a révélé que le signal RiboBright chevauche fortement les marqueurs de la grande sous-unité ribosomique et des structures comme le réticulum endoplasmique et les mitochondries, où beaucoup de ribosomes résident. En même temps, certaines taches lumineuses flottent librement dans le cytoplasme, représentant probablement des ribosomes mobiles non attachés aux membranes.
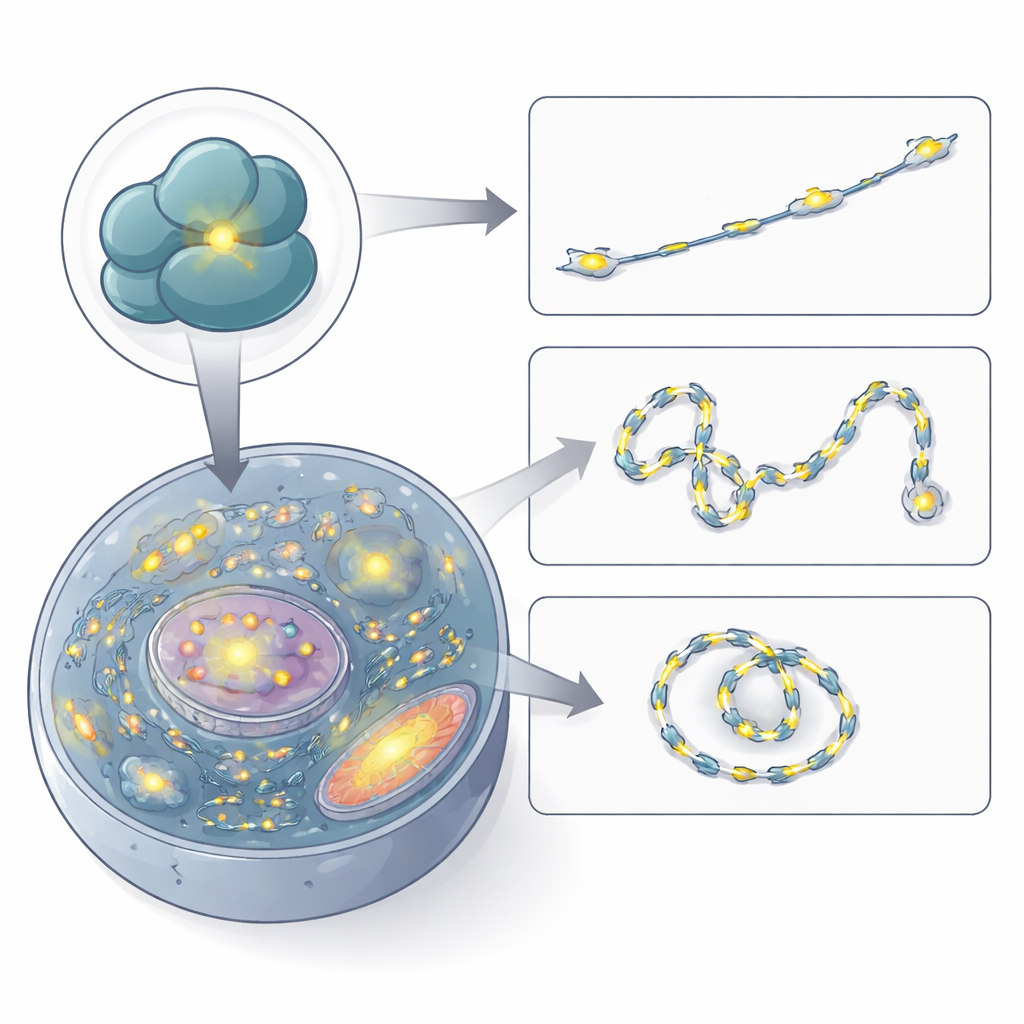
Observer les ribosomes en mouvement dans les cellules vivantes
Confiants dans sa spécificité, les auteurs ont utilisé RiboBright pour filmer les ribosomes en action. En enregistrant des images toutes les quelques centaines de millisecondes, ils ont retracé les trajectoires de taches fluorescentes individuelles à travers la cellule. Beaucoup d’entre elles bougeaient à peine ou restaient confinées à de petites régions, ce qui suggère des ribosomes traduisant sur place sur des ARNm ancrés ou sur le réticulum endoplasmique. D’autres erraient de manière aléatoire et diffusante, et une plus petite fraction montrait un mouvement dirigé net, évoquant un transport actif le long de voies cellulaires. Les vitesses mesurées correspondent à des estimations antérieures pour les ARNm et les amas de ribosomes, confirmant que RiboBright peut capturer en temps réel des dynamiques ribosomiques réalistes.
Différents types cellulaires, différentes stratégies ribosomiques
RiboBright a également révélé à quel point le contenu et l’organisation des ribosomes dépendent de l’identité cellulaire. Sur dix lignées cellulaires humaines et murines, y compris des cellules souches, des cellules cancéreuses et des cellules non cancéreuses, le motif et la luminosité des taches ribosomiques variaient de façon spectaculaire. Certaines cellules contenaient de grands amas lumineux qui peuvent correspondre à des régions de production protéique intense, tandis que d’autres présentaient principalement de petites taches dispersées. De manière surprenante, le simple nombre de ribosomes dans une cellule ne prédisait pas de manière fiable la quantité de protéines produites : dans la plupart des types cellulaires, la production protéique et le contenu en ribosomes montraient peu de corrélation. Les cellules souches embryonnaires se distinguaient par une faible productivité par ribosome et une traduction relativement uniforme entre cellules individuelles, suggérant qu’elles conservent de larges réserves de ribosomes peu utilisés tout en maintenant un faible bruit dans la production protéique.
Les ribosomes lors des premières décisions de destin cellulaire
L’équipe a ensuite suivi des cellules souches embryonnaires de souris au début de leur différenciation vers deux lignées précoces : une branche de type ectoderme et une branche de type endoderme extra-embryonnaire (XEN). En utilisant RiboBright conjointement avec des marqueurs de surface cellulaire, ils ont constaté que les deux lignées émergentes acquéraient légèrement plus de ribosomes totaux que les cellules indifférenciées, mais arrangeaient ces ribosomes différemment. Les cellules de type XEN, qui développent de longues protrusions, montraient des mouvements ribosomiques plus lents et plus confinés, cohérent avec une synthèse protéique localisée dans des régions spécialisées. En revanche, les cellules de type ectoderme présentaient des ribosomes plus mobiles et, après environ deux jours, développaient des « hubs translationnels » marquants où le signal ribosomal et la nouvelle synthèse protéique atteignaient un pic. Au cours des 72 premières heures de différenciation, la production protéique globale et les niveaux de ribosomes ont légèrement diminué, mais les ribosomes restants sont devenus un peu plus efficaces, en particulier dans les cellules en cours de différenciation.
Ce que cela signifie pour la compréhension des cellules
Ensemble, ces résultats dressent un tableau plus riche des ribosomes comme des machines dynamiques et dépendantes du contexte, plutôt que comme de simples ouvriers uniformes. RiboBright offre aux chercheurs un outil pratique pour visualiser et compter les ribosomes à travers de nombreux types cellulaires, dans des échantillons fixés comme vivants, et pour relier la position et le mouvement des ribosomes à la quantité de protéines réellement produite par une cellule. Pour les non-spécialistes, l’idée clé est que les cellules ajustent non seulement combien d’usines à protéines elles construisent, mais aussi où elles les placent et à quel point elles les font fonctionner, de façons dépendant du type cellulaire et de l’état développemental. Cette nouvelle sonde fluorescente rend visibles ces logistiques cachées, ouvrant la voie à l’étude de la contribution du comportement ribosomique au développement, aux maladies et aux réponses aux thérapies.
Citation: Poulladofonou, G., Grandi, C., Hu, X. et al. RiboBright reveals cell-type-specific differences in ribosome organization and movement. Nat Commun 17, 2734 (2026). https://doi.org/10.1038/s41467-026-68947-7
Mots-clés: ribosomes, sondes fluorescentes, imagerie unicellulaire, différenciation des cellules souches, synthèse des protéines