Clear Sky Science · fr
FCHo2, et non talin, permet l’activation intramembranaire de l’intégrine ɑvβ5 dans les adhésions courbées
Comment les cellules perçoivent la forme de leur environnement
Nos corps sont constitués de cellules qui s’accrochent en permanence à leur environnement, tirant et poussant pour se déplacer, se diviser ou rester en place. Cet article montre que les cellules ne perçoivent pas seulement la rigidité de leur milieu — elles en lisent aussi la forme. En découvrant un système d’adhésion spécifique qui ne s’active que là où la membrane cellulaire est fortement courbée, les auteurs démontrent que les cellules utilisent des « prises » internes différentes selon que le milieu est plat ou fibreux, avec des implications importantes pour la formation des tissus et la dissémination des cancers.
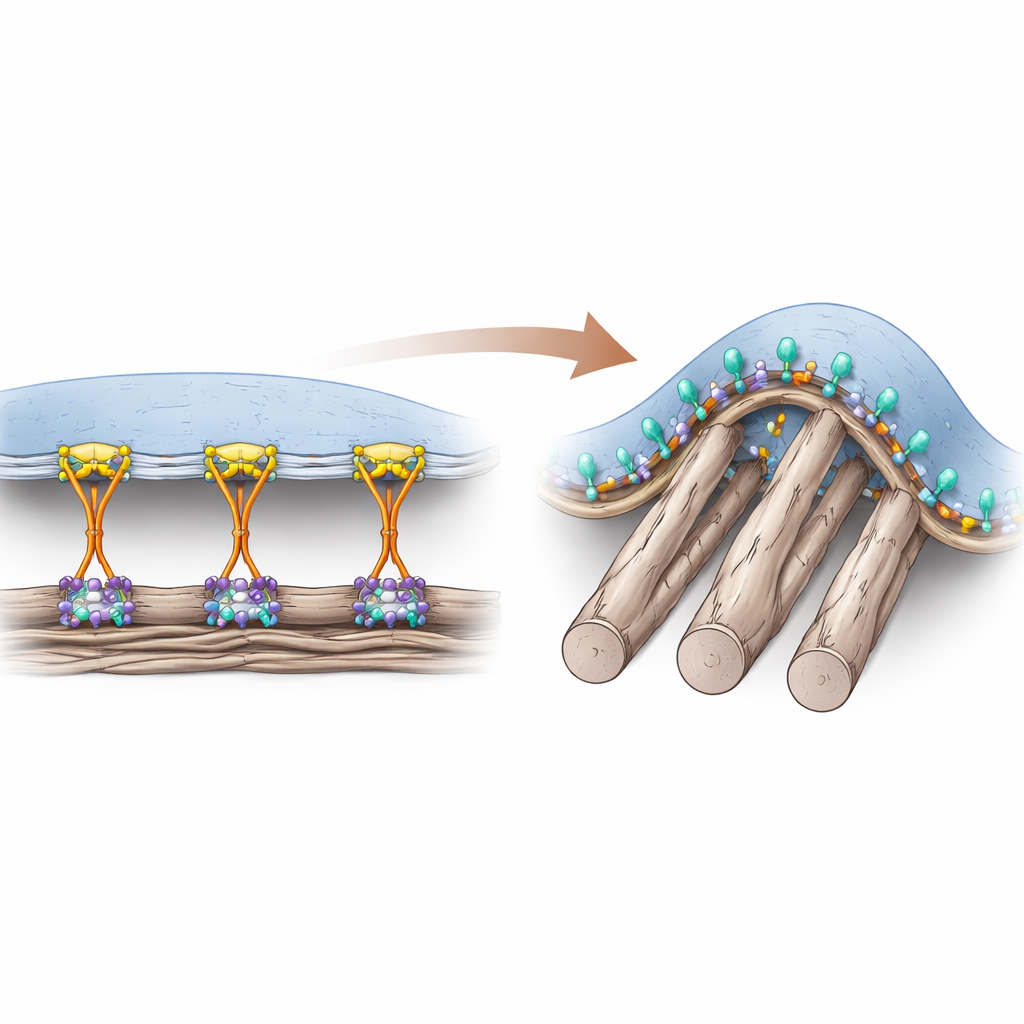
Deux manières pour la cellule de s’accrocher
Les cellules se fixent au matériau riche en protéines qui les entoure via des récepteurs de surface appelés intégrines. Pendant des années, les chercheurs ont pensé qu’une protéine auxiliaire nommée talin était absolument essentielle pour activer les intégrines « de l’intérieur » de la cellule, permettant une fixation solide dans des sites d’ancrage classiques appelés adhésions focales. Ces adhésions se forment principalement sur des surfaces plates et rigides et transmettent de fortes forces de traction via le cytosquelette. Toutefois, dans les tissus vivants, de nombreuses fibres environnantes sont souples et cylindriques, créant des points de contact courbés qui ne supportent pas facilement ces structures à forte contrainte. Les auteurs avaient précédemment identifié un type d’adhésion différent, appelé adhésion courbée, qui apparaît précisément là où la membrane s’enroule autour de fines fibres et qui dépend d’une intégrine spécifique, αvβ5.
Les prises courbées utilisent un auxiliaire différent
Dans la nouvelle étude, l’équipe montre que talin, bien que toujours présent, n’est pas l’activateur clé de l’intégrine αvβ5 dans les adhésions courbées. À la place, une protéine détectrice de courbure appelée FCHo2 prend ce rôle. En utilisant des barres et des piliers nanométriques conçus avec précision pour plier les membranes cellulaires de manière contrôlée, ils ont observé que αvβ5 se regroupe fortement dans les régions courbées, mais seulement lorsque FCHo2 peut se lier à une très courte séquence — un motif HDRRE — juste à l’intérieur de la cellule sur la queue β5. Lorsque ce motif est perturbé, l’intégrine fonctionne encore dans les adhésions focales mais ne peut plus former d’adhésions courbées. L’inhibition de FCHo2 laisse les adhésions focales classiques largement intactes tout en éliminant les adhésions courbées, alors que la suppression de talin affaiblit fortement les adhésions focales mais laisse les adhésions courbées essentiellement inchangées.
Un unique acide aminé qui fait office de sélecteur de forme
Un mystère était pourquoi une intégrine étroitement apparentée, αvβ3, ne peut pas former d’adhésions courbées alors que sa queue intracellulaire ressemble beaucoup à celle de β5. En échangeant des domaines entre les deux intégrines et en introduisant des mutations ponctuelles, les auteurs ont identifié une position pivot proche du site de liaison à talin : la plupart des intégrines β possèdent un tryptophane (W), mais β5 a de manière unique une tyrosine (Y766). Lorsque la tyrosine de β5 a été remplacée par un tryptophane, l’intégrine a perdu sa capacité à participer aux adhésions courbées et s’est comportée davantage comme β3, ne favorisant que les adhésions focales. L’inverse — introduire une tyrosine dans le chimère de type β3 — a restauré la sensibilité à la courbure. Des expériences supplémentaires avec des variants mimant les états phosphorylés ou non phosphorylés de cette tyrosine suggèrent que sa modification chimique peut orienter l’intégrine vers des adhésions focales plates et à haute force ou vers des adhésions courbées à faible force.
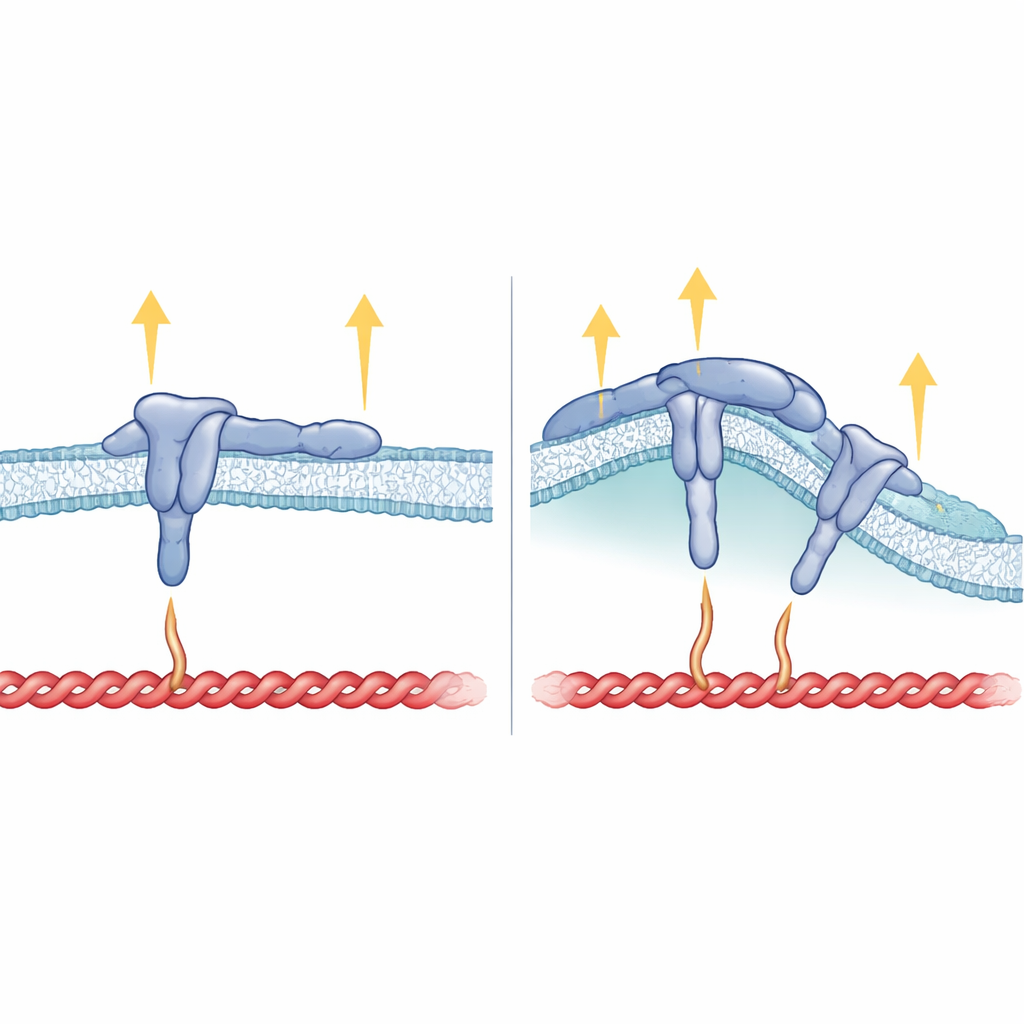
Comment la forme de la membrane, la structure de l’intégrine et la force s’emboîtent
Au-delà de la queue intracellulaire, le segment de β5 qui traverse la membrane s’est aussi avéré critique. Lorsque les chercheurs ont remplacé le segment transmembranaire de β5 par celui de β3, l’intégrine résultante pouvait encore former des adhésions focales mais ne favorisait plus les sites courbés et ne suivait plus FCHo2. Cela suggère que la manière dont l’intégrine s’insère dans la membrane aide à orienter le motif HDRRE pour que FCHo2 puisse s’y accrocher dans les régions courbées et stabiliser αvβ5 liée au ligand et active. Dans les adhésions courbées, il semble que talin ne touche qu’une partie plus éloignée de la queue de l’intégrine et ne supporte pas de fortes tensions, ce qui explique pourquoi d’autres composants gourmands en force tels que vinculine, tensine et kindline y sont largement absents. En revanche, dans les adhésions focales, talin s’accroche à la fois aux sites proches et lointains de la queue et de la membrane, soutenant de fortes forces de traction mais empêchant FCHo2 d’accéder à la même région.
Ce que cela implique pour le comportement cellulaire
Pour un observateur non spécialiste, le message de ce travail est que les cellules disposent de deux « modes de prise » distincts pour s’attacher à leur environnement. Sur des zones plates et rigides, elles utilisent des adhésions focales pilotées par talin, conçues pour tirer fortement. Sur des structures souples, fibreuses et courbées, elles basculent vers des adhésions courbées pilotées par FCHo2 qui stabilisent l’intégrine αvβ5 avec une force beaucoup plus faible. Un petit changement dans la séquence de l’intégrine — et l’état chimique de ce site — aide à décider quel mode est employé. Ce système double permet aux cellules d’interpréter à la fois la rigidité et la forme dans des environnements tridimensionnels, influençant leur migration, l’organisation des tissus et potentiellement leur invasion en cas de maladie.
Citation: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Mots-clés: intégrines, adhésion cellulaire, courbure de la membrane, FCHo2, cytosquelette