Clear Sky Science · fr
Formation d’indazole déclenchée par une nitroreductase
Transformer des ingrédients simples en médicaments précieux
De nombreux médicaments modernes reposent sur quelques « cadres » moléculaires répandus qui s’insèrent efficacement dans les cibles biologiques. L’un de ces cadres, appelé indazole, apparaît dans des médicaments utilisés contre le cancer et les nausées sévères. Jusqu’à présent, la synthèse des indazoles nécessitait le plus souvent des réactifs agressifs, des températures élevées et des métaux peu respectueux de l’environnement. Cette étude montre comment des scientifiques peuvent inciter des enzymes naturelles à construire des indazoles en douceur, en milieu aqueux, ouvrant la voie à des méthodes de production de médicaments plus écologiques.
Pourquoi ces molécules en anneau sont importantes
Les concepteurs de médicaments réutilisent souvent certaines structures cycliques parce qu’elles interagissent de manière fiable avec les protéines de l’organisme. Les indazoles sont l’une de ces structures prisées et se retrouvent dans des médicaments approuvés pour le cancer et les nausées liées à la chimiothérapie. Les chimistes connaissent déjà plusieurs voies de synthèse des indazoles, mais les routes standard reposent sur des blocs de construction réactifs, des bases ou des acides forts et des catalyseurs métalliques comme le cuivre ou le palladium. Ces méthodes fonctionnent, mais elles génèrent des déchets, consomment de l’énergie et présentent des risques de sécurité, en contradiction avec la volonté croissante d’une fabrication pharmaceutique durable.
Les enzymes, des ouvriers de construction délicats
Plutôt que de forcer l’assemblage des atomes par la chaleur et des réactifs agressifs, les auteurs ont recours à la biocatalyse — l’utilisation d’enzymes, catalyseurs naturels, pour mener des réactions en eau à température ambiante. Ils se concentrent sur des enzymes appelées nitroreductases, qui aident normalement les cellules à détoxifier des composés contenant un groupe nitro par réduction par étapes. L’équipe a émis l’hypothèse que si un intermédiaire particulier de cette voie de réduction pouvait être relâché au bon moment, il se refermerait spontanément pour former le système d’anneau caractéristique de l’indazole. En utilisant deux nitroreductases différentes, ils démontrent que des matières premières simples, des 2-nitrobenzylamines, sont converties avec aisance en indazoles avec une excellente efficacité, souvent au-delà de 99 % de conversion, dans des conditions aqueuses et douces.
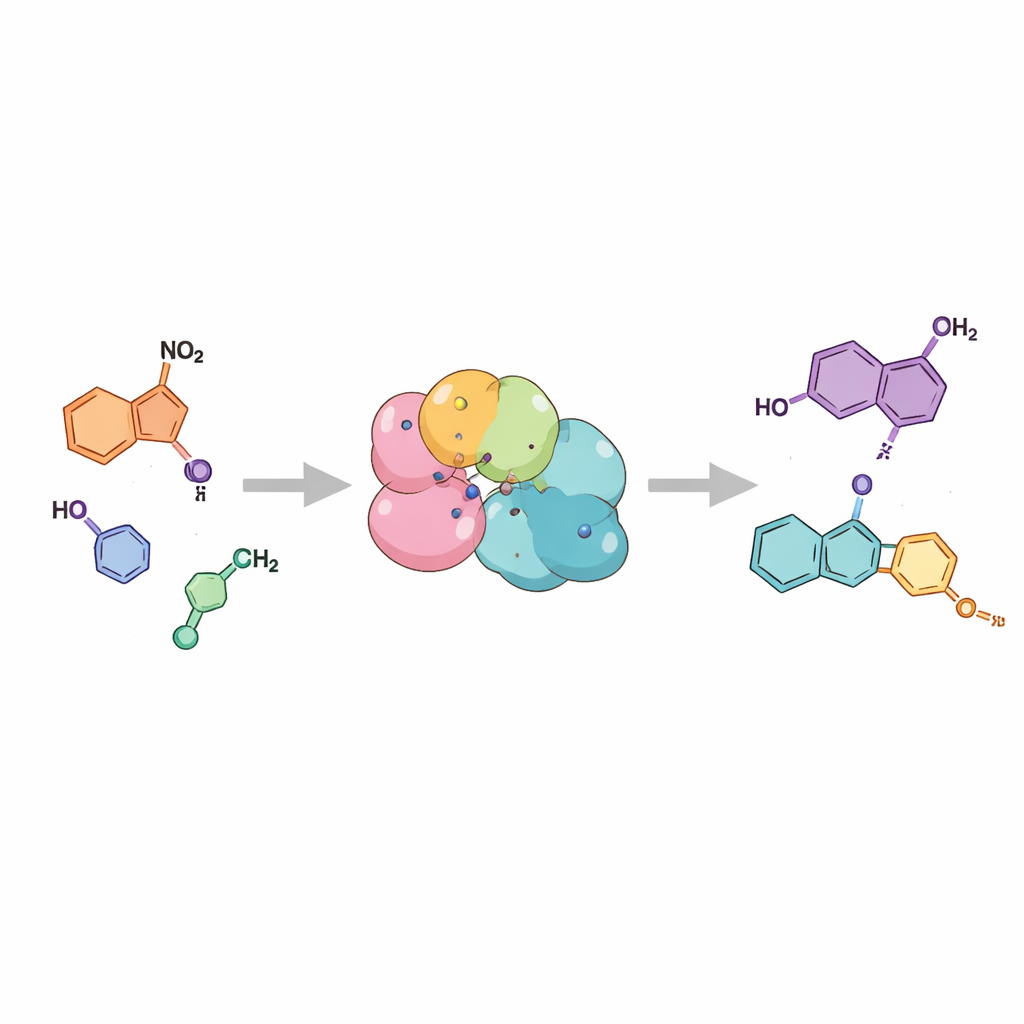
Cartographier les capacités des enzymes
Pour tester la généralité de la stratégie, les chercheurs ont soumis aux enzymes une famille de précurseurs apparentés portant différents substituants et positions sur le noyau aromatique. Ils ont constaté que les deux enzymes toléraient une large gamme de décorations chimiques, des petits groupes comme le méthyle à des systèmes d’anneaux plus volumineux ainsi que diverses substitutions chlore, brome et méthoxy. Dans de nombreux cas, les réactions ont mené proprement à l’indazole désiré, avec des rendements isolés suffisamment élevés pour être pratiques. La nature des substituants sur le matériau de départ contrôlait aussi quelle des deux formes proches d’indazole apparaissait, un aspect important car les deux formes peuvent avoir de l’importance en conception de médicaments. Le même concept a même été étendu pour produire un parent plus grand des indazoles, appelé cinnoline, soulignant la polyvalence de l’approche.
Assembler une chaîne de fabrication enzymatique en deux étapes
Les indazoles obtenus dans ce travail ne proviennent pas directement de précurseurs spécialisés ; l’équipe a plutôt construit une courte chaîne enzymatique à partir de blocs de départ peu coûteux. Dans la première étape, une autre classe d’enzymes, des imine réductases, assemble une aldéhyde simple et une amine pour former la 2-nitrobenzylamine nécessaire. Dans la seconde étape, la nitroreductase convertit cet intermédiaire en anneau d’indazole. En ajustant soigneusement les quantités d’enzymes et le système de recyclage de leurs cofacteurs, les auteurs ont réalisé cette cascade à deux enzymes à l’échelle préparative, à partir de 50 milligrammes d’aldéhyde en milieu aqueux. Ils ont obtenu plusieurs produits indazole en bons rendements globaux, y compris des exemples avec différentes chaînes latérales susceptibles d’être modifiées ensuite pour la découverte de médicaments.
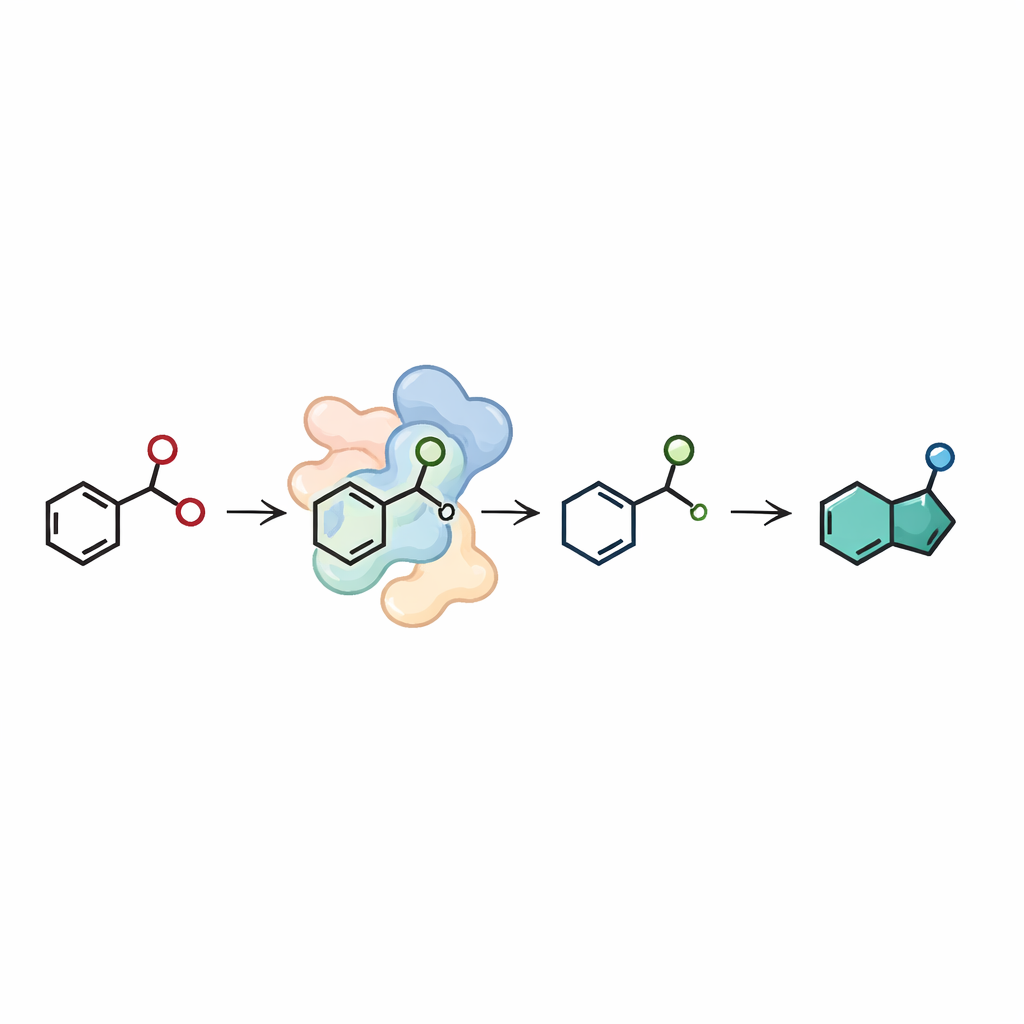
Une voie plus propre vers des blocs de construction pharmaceutiques complexes
Pour le lecteur non spécialiste, le message clé est que les chercheurs ont appris à des catalyseurs naturels à assembler un système d’anneau d’intérêt médical d’une manière plus douce pour les opérateurs et pour l’environnement. Leur voie enzymatique évite les réactifs nitrogène–azote dangereux et les catalyseurs métalliques précieux, fonctionne en eau à températures modérées et peut être combinée avec d’autres enzymes pour former une mini-usine efficace. Ce travail apporte un nouvel outil puissant à la boîte à outils du chimiste, rapprochant la fabrication durable tout en fournissant au monde pharmaceutique des blocs d’indazole polyvalents pour les médicaments de demain.
Citation: Terholsen, H., Medema, L., Chernyshova, E. et al. Nitroreductase-triggered indazole formation. Nat Commun 17, 2261 (2026). https://doi.org/10.1038/s41467-026-68926-y
Mots-clés: biocatalyse, synthèse d’indazole, nitroreductase, chimie verte, cascades enzymatiques