Clear Sky Science · fr
Les protéines TMEM63 agissent comme des scramblases lipidiques activés mécaniquement et modulés par le cholestérol, contribuant à la méca-résilience membranaire
Comment les cellules restent intactes sous contrainte physique
Les cellules de notre corps sont constamment comprimées, étirées et secouées, que ce soit dans un cœur qui bat, des muscles en activité ou des tumeurs poussant à travers les tissus. Cette étude révèle comment une famille de protéines membranaires, nommée OSCA/TMEM63, aide les cellules à survivre à de telles forces mécaniques en réorganisant les lipides de leur enveloppe externe. Comprendre ce système amortisseur intégré pourrait offrir de nouvelles perspectives sur des troubles de l’audition, la gaine des nerfs et même la dissémination du cancer.
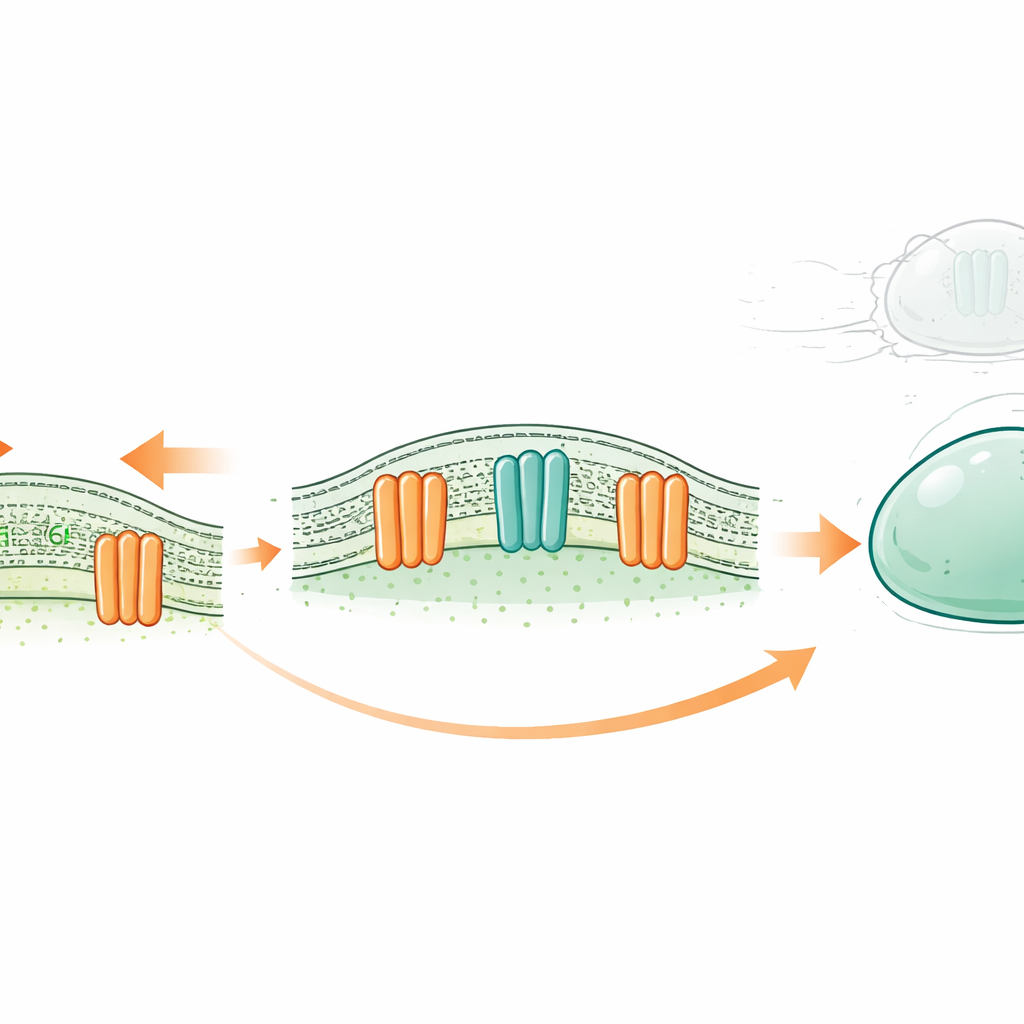
Un nouveau type d’amortisseur cellulaire
Chaque cellule est entourée d’une fine membrane huileuse composée de deux couches de molécules lipidiques. Traditionnellement, certaines protéines membranaires étaient considérées principalement comme des canaux ioniques — de minuscules valves permettant à des particules chargées d’entrer ou de sortir en réponse à des stimuli tels que l’étirement. La famille OSCA/TMEM63, présente des plantes jusqu’aux humains, est connue pour s’ouvrir en réponse à la tension membranaire. Des travaux structuraux antérieurs laissaient entrevoir que, contrairement aux canaux classiques, leurs pore étaient en partie bordés par des lipides eux-mêmes. Cela a soulevé une possibilité provocante : ces canaux pourraient-ils aussi agir comme des « scramblases », faisant basculer les lipides entre les couches interne et externe de la membrane lorsque la cellule est soumise à une force ?
Observer les lipides basculer à travers la membrane
Pour tester cette idée, les auteurs ont combiné simulations informatiques et systèmes d’étude réductionnistes construits à partir de composants purifiés. Dans les simulations, des versions ouvertes de plusieurs protéines OSCA et TMEM63 ont été insérées dans des membranes modèles. Des molécules lipidiques ont spontanément traversé un sillon dans ces protéines, passant d’un feuillet de la bicouche à l’autre, formant une sorte de ceinture reliant les deux feuillets tout en laissant un passage rempli d’eau pour les ions. En parallèle, l’équipe a construit de grosses « bulles » artificielles (vésicules) contenant des lipides fluorescents et des protéines spécifiques. Lorsqu’un agent externe éteignait la fluorescence à la surface externe, toute baisse supplémentaire du signal ne pouvait s’expliquer que par des lipides basculant du feuillet interne vers l’extérieur. Les vésicules contenant OSCA1.1, OSCA1.2, OSCA2.2 ou TMEM63A/B ont montré cette perte supplémentaire de fluorescence, indiquant un scrambling actif, tandis que des canaux témoins qui ne renversent pas les lipides n’en ont pas présenté.
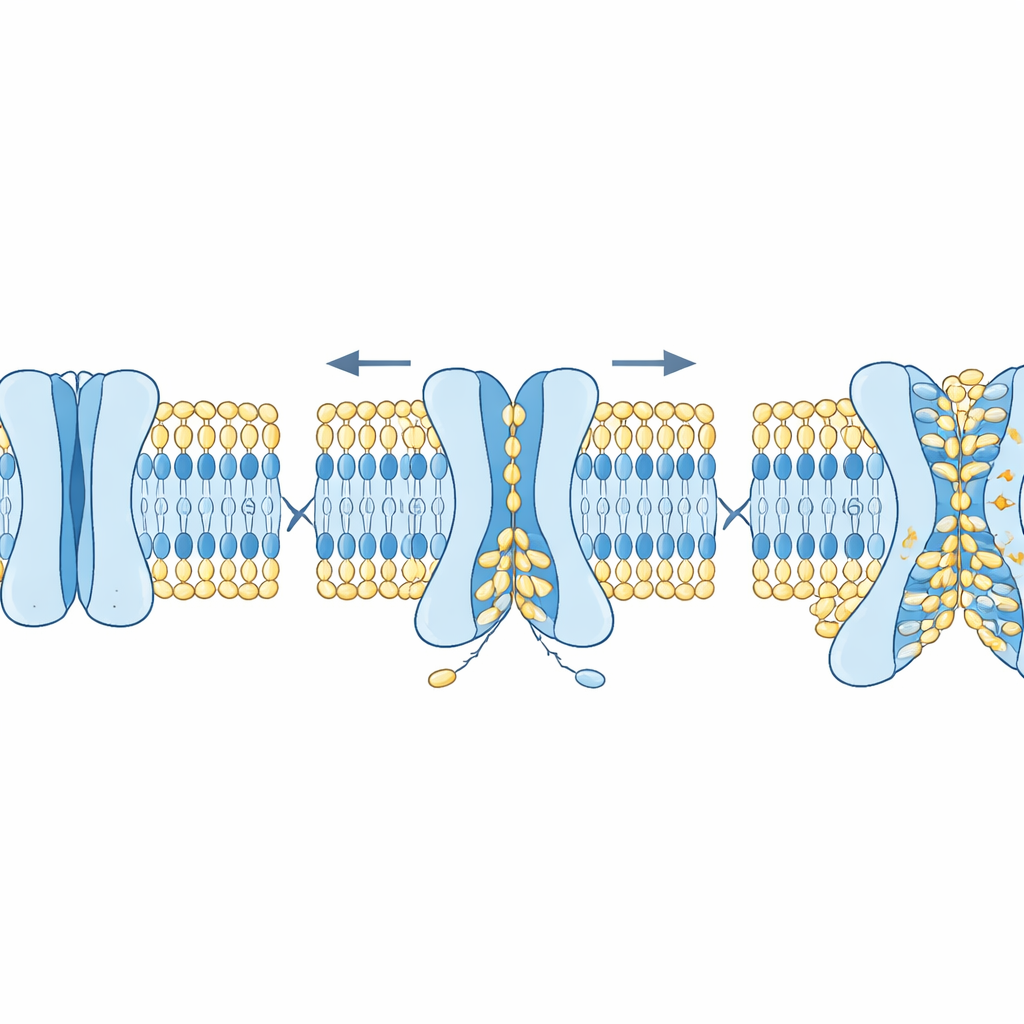
Comment la structure et le cholestérol règlent le processus
Les chercheurs ont ensuite cherché quels éléments des protéines TMEM63 contrôlent ce comportement double. En utilisant AlphaFold2, ils ont généré de nombreuses conformations plausibles des TMEM63 humains, allant d’un état fermé à des états de plus en plus ouverts. Les simulations ont révélé qu’un petit nombre d’acides aminés volumineux agissent comme des « goulots d’étranglement » dans le sillon. Une résidu limite principalement le flux ionique, tandis que d’autres bloquent le mouvement des lipides. La mutation de la barrière ionique augmentait la conductance électrique sans beaucoup modifier le scrambling lipidique, tandis que la mutation du verrou lipidique favorisait le basculement des lipides et provoquait même l’apparition de signaux « mangez-moi » à la surface des cellules sans autre stimulus. Un autre régulateur clé était le cholestérol, un composant rigidifiant des membranes. L’ajout de cholestérol aux membranes modèles ralentissait nettement le scrambling lipidique et stabilisait l’état fermé de TMEM63A, aussi bien dans les simulations que dans des structures obtenues par cryo‑microscopie électronique où le cholestérol s’insérait dans des sites spécifiques de la protéine.
La force mécanique comme interrupteur
Si le cholestérol maintient normalement le scrambling sous contrôle à l’intérieur des cellules, qu’est‑ce qui l’active au bon moment ? L’équipe a utilisé des molécules en anneau de sucres appelées cyclodextrines pour extraire sélectivement des lipides des membranes et ainsi augmenter la tension sans retirer le cholestérol. Dans des vésicules de taille cellulaire, l’ajout de cyclodextrine a activé le scrambling lipidique par TMEM63A uniquement lorsque la protéine était présente, démontrant que la contrainte mécanique seule peut déclencher le basculement. Des approches similaires dans des cellules vivantes ont montré qu’une simple réduction légère du cholestérol n’était pas suffisante ; un défi mécanique ultérieur était nécessaire pour observer un scrambling important. Lorsque des cellules modifiées pour exprimer TMEM63A étaient étirées à plusieurs reprises, elles exposaient rapidement certains lipides à leur surface externe, un signe caractéristique de scrambling, tandis que des cellules dépourvues de ces protéines montraient bien moins de changement.
Protection des cellules contre la rupture
Au‑delà du basculement des lipides, le scrambling activé mécaniquement modifiait le comportement physique des membranes sous stress extrême. Dans des vésicules artificielles exposées à de fortes forces, celles dépourvues de scramblases avaient tendance à éclater, alors que les vésicules contenant TMEM63A ou un scramblase connu se contractaient, formaient de fins tubules et restaient en grande partie intactes. Dans une lignée de cellules de gliome humain exprimant naturellement TMEM63A et TMEM63B, la réduction des niveaux de l’une ou l’autre protéine augmentait la probabilité de rupture sous stress mécanique intense. Ensemble, ces résultats soutiennent un modèle dans lequel les protéines OSCA/TMEM63 agissent comme des soupapes qui s’ouvrent sous tension et estompent temporairement la différence habituelle entre les faces interne et externe de la membrane. En permettant aux lipides de se redistribuer rapidement, elles contribuent à égaliser les contraintes et à prévenir des déchirures catastrophiques.
Ce que cela signifie pour la santé et la maladie
En termes clairs, ce travail montre que certains canaux sensibles à l’étirement font plus que conduire des signaux électriques : ils réorganisent aussi la « peau » externe de la cellule pour l’aider à survivre à la compression. Les protéines TMEM63 apparaissent comme des scramblases lipidiques activées mécaniquement dont l’activité est finement modulée par la composition membranaire, en particulier le cholestérol. Ce mécanisme de méca‑résilience peut être important partout où les cellules subissent de fortes forces, des fibres nerveuses isolantes et des cellules sensorielles de l’oreille jusqu’aux cellules cancéreuses traversant des tissus denses. Comprendre et, éventuellement, manipuler cette double fonction canal ionique–scramblase pourrait ouvrir de nouvelles voies pour protéger des tissus vulnérables — ou, à l’inverse, rendre des cellules cancéreuses difficiles à éliminer plus fragiles.
Citation: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
Mots-clés: canaux ioniques mécanosensibles, renversement des lipides, mécanique de la membrane cellulaire, régulation par le cholestérol, protéines OSCA/TMEM63