Clear Sky Science · fr
Des protéines FOX antagonistes contrôlent épigénétiquement l’équilibre lytique‑latent des herpèsvirus
Pourquoi les virus herpétiques cachés comptent
De nombreuses personnes hébergent des virus herpès simplex à vie, souvent sans le savoir. Ces virus peuvent rester silencieux à l’intérieur des cellules nerveuses pendant des années, puis flamber soudainement, provoquant des boutons de fièvre, des atteintes oculaires ou des problèmes plus graves chez les personnes immunodéprimées. Ce qui maintient le virus endormi la plupart du temps, et ce qui le réactive, a longtemps été un mystère. Cette étude révèle une pièce clé de ce système de contrôle : une lutte d’influence entre deux groupes opposés de protéines humaines qui remodèlent l’ADN viral et déterminent si l’herpès reste silencieux ou commence à produire de nouveaux virus.
Deux équipes cellulaires tirant en sens opposé
Les auteurs se sont concentrés sur une grande famille de protéines humaines liant l’ADN appelées protéines FOX, qui contrôlent normalement nos propres gènes lors du développement et du métabolisme. En testant de nombreux membres de la famille FOX dans des cellules de type neuronal, ils ont identifié deux camps distincts. Un groupe (incluant des protéines comme FOXF1) stimulait fortement la réplication du virus herpès simplex de type 1 (HSV‑1) et de plusieurs alphaherpèsvirus apparentés. Un autre groupe (FOXK1 et FOXK2) faisait l’inverse, réprimant puissamment la croissance virale. Cet équilibre n’était pas identique selon les types cellulaires : les cellules non neuronales et les neurones sous stress avaient tendance à produire davantage les FOX activateurs, tandis que les neurones sensoriels au repos produisaient très peu d’activateurs mais des niveaux élevés des FOXK répressifs.
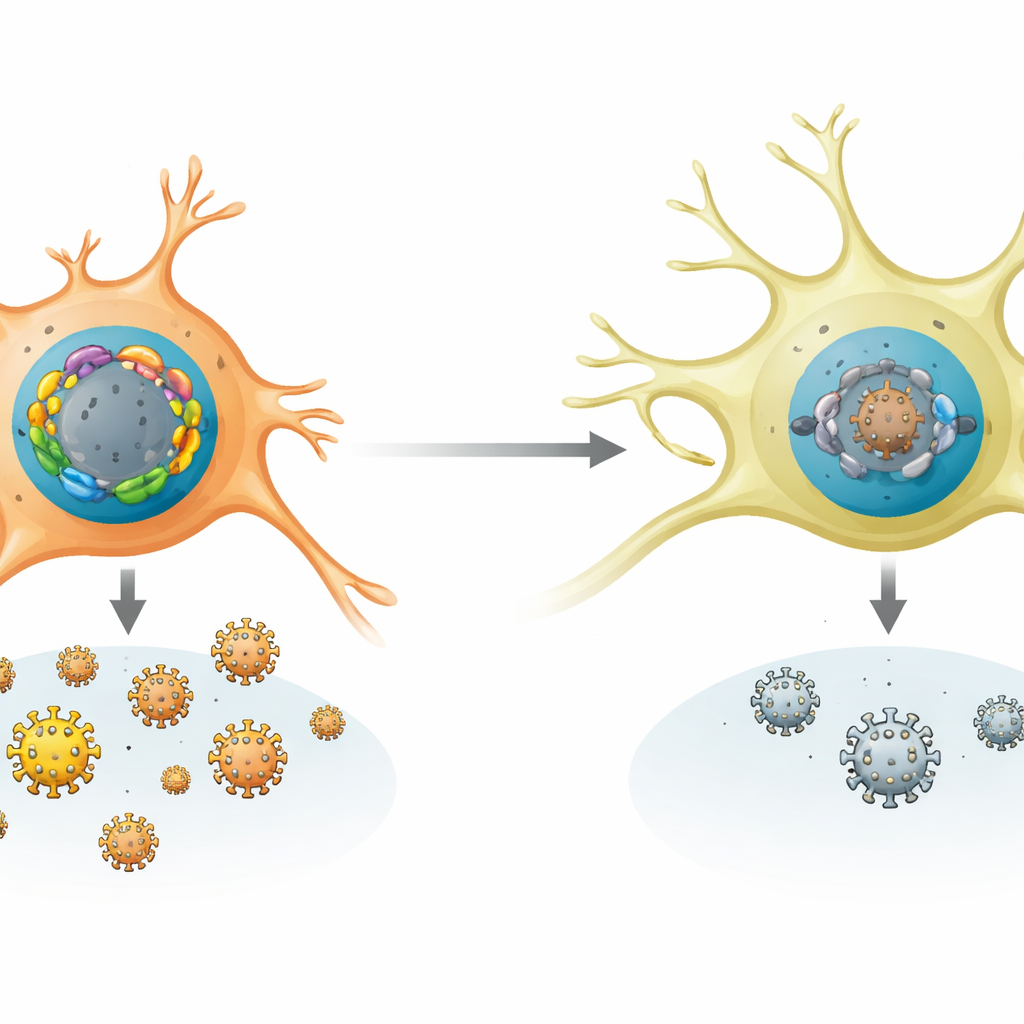
Comment les cellules nerveuses favorisent l’état silencieux
L’équipe a comparé l’activité des gènes FOX dans de nombreux types cellulaires humains et murins et chez des animaux infectés. Les neurones sensoriels, lieu naturel de la latence du HSV‑1, présentaient un profil favorable au silence : forte expression de FOXK1 et FOXK2, et faible expression de la plupart des FOX activateurs. Chez la souris, l’infection initiale et des signaux de stress ultérieurs tels que la chaleur ou une lésion tissulaire augmentaient sélectivement les niveaux de plusieurs gènes Fox activateurs sans réduire les répressifs. Dans des neurones murins en culture et chez la souris vivante, la suppression ou la délétion des protéines FOXK facilitait la réplication du HSV‑1 et sa réapparition depuis la latence. À l’inverse, forcer les neurones à produire des FOX activateurs suffisait à déclencher la réactivation même en l’absence de déclencheurs chimiques, montrant à quel point l’état viral est sensible à cet équilibre FOX.
Saisir l’ADN viral et l’ouvrir ou le refermer
Pour comprendre le mécanisme sous‑jacent, les chercheurs ont cartographié où les protéines FOX se placent sur le génome viral. Ils ont constaté que tant l’activateur FOXF1 que le répresseur FOXK1 se lient largement à l’ADN du HSV‑1, et pas seulement à quelques motifs séquentiels précis. Cette liaison dépend d’une région conservée des protéines FOX qui saisit l’épine dorsale de l’ADN plutôt que des bases individuelles, leur permettant de s’attacher presque n’importe où. Une fois en place, les deux camps protéiques recrutent des partenaires moléculaires différents qui remodèlent la chromatine, l’ensemble formé par l’ADN et ses protéines de conditionnement. Les FOX activateurs, en particulier FOXF1, s’associent à CBP et P300, des enzymes qui ajoutent des groupes acétyle aux histones et relâchent la chromatine. Cela rend l’ADN viral plus accessible et stimule l’expression des gènes viraux précoces, intermédiaires et tardifs. FOXK1, en revanche, travaille avec des facteurs tels que SIN3A et MAX liés à la désacétylation des histones et à la répression génique, resserrant la chromatine virale et maintenant les gènes éteints.
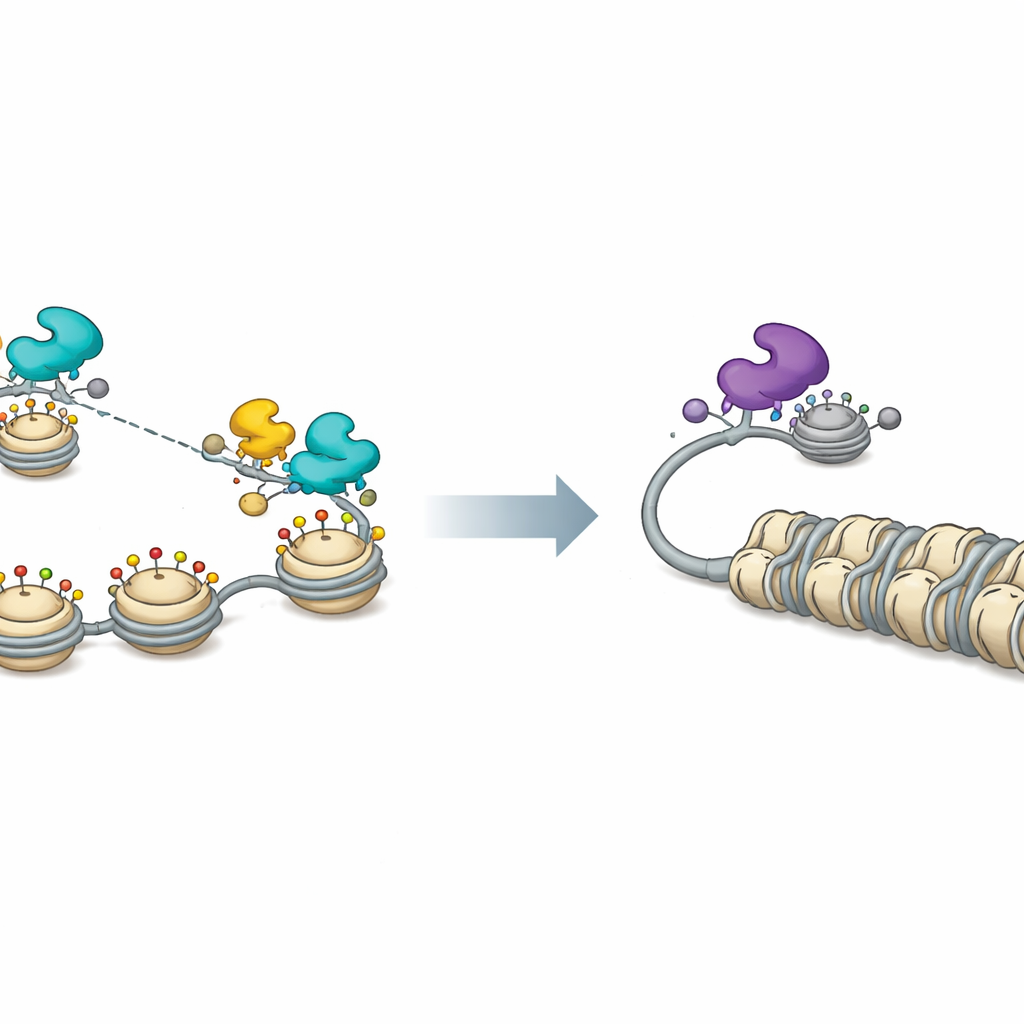
Un interrupteur chromatine pour le sommeil et l’éveil viraux
Les mesures sur la chromatine virale ont confirmé ce tableau. En présence de FOXF1, les histones sur l’ADN viral étaient dégarnis ou marqués chimiquement de façon associée à une chromatine ouverte et active, et l’accessibilité globale des promoteurs viraux augmentait à l’échelle du génome. L’expression de FOXF1 dispersait aussi de petites structures nucléaires appelées corps nucléaires PML qui contribuent normalement à réprimer l’ADN viral. Le blocage de CBP et P300 annulait beaucoup de ces effets activateurs et réduisait l’expression des gènes viraux induite par FOXF1. Du côté répressif, les chercheurs ont montré que les partenaires associés à FOXK1 et l’activité des histones désacétylases étaient importants pour maintenir une réplication faible du HSV‑1 ; l’inhibition chimique des désacétylases augmentait à la fois la production virale et affaiblissait la suppression médiée par FOXK1.
Ce que cela signifie pour contrôler l’infection à vie
En somme, le travail suggère que l’activité ou la dormance du HSV‑1 dépend largement du mélange de protéines FOX présentes dans le neurone hôte. Les neurones sensoriels au repos favorisent naturellement l’état répressif dominé par FOXK, poussant le virus vers une forme profondément silencieuse et compactée en chromatine. Des stress ou d’autres conditions qui augmentent les FOX activateurs peuvent faire basculer cet équilibre, ouvrir la chromatine virale et permettre la reprise du cycle lytique. En révélant cette lutte épigénétique, l’étude met en lumière de nouvelles façons dont les scientifiques pourraient, un jour, pousser les virus herpétiques plus fermement vers une latence inoffensive ou, inversement, les forcer à sortir de leur cachette dans des conditions contrôlées afin de les éliminer.
Citation: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
Mots-clés: latence du virus herpès simplex, facteurs de transcription FOX, chromatine virale, régulation épigénétique, réactivation virale