Clear Sky Science · fr
Étendre le potentiel d’altération de l’ADN des métallo-nucléases artificielles grâce à la chimie click
Construire des ciseaux moléculaires plus intelligents
La chimiothérapie agit souvent en endommageant l’ADN des cellules cancéreuses, mais les médicaments actuels peuvent être des outils grossiers qui blessent aussi les tissus sains. Cette étude explore une nouvelle classe de « ciseaux moléculaires » hautement programmables, constitués de cuivre et de petits éléments organiques assemblés par chimie click. En ajustant leur forme et leur manière d’agripper l’ADN, les chercheurs cherchent à créer des agents qui coupent le matériel génétique avec plus de précision, ouvrant des pistes vers de futurs traitements anticancéreux et antibactériens.
Assembler un coupeur à trois bras
L’équipe utilise la chimie click catalysée par le cuivre, une méthode récompensée par un prix Nobel et reconnue pour sa fiabilité, pour assembler une famille de molécules appelées ligands Tri-Click (TC). Chaque molécule TC est un noyau à trois bras capable de coordonner trois ions cuivre à la fois, formant un cluster compact susceptible d’attaquer l’ADN. En échangeant différents groupes « donneurs » chimiques à l’extrémité de chaque bras — à base d’azote, d’oxygène ou de soufre — les scientifiques ont testé de façon systématique comment de subtiles modifications structurelles influencent la liaison du cuivre, la reconnaissance de l’ADN et l’activité biologique. Parmi plusieurs nouveaux dessins, les versions portant des donneurs azotés plats et cycliques se sont révélées particulièrement prometteuses pour une fixation serrée de l’ADN.
Trouver une molécule leader qui aime les sillons de l’ADN
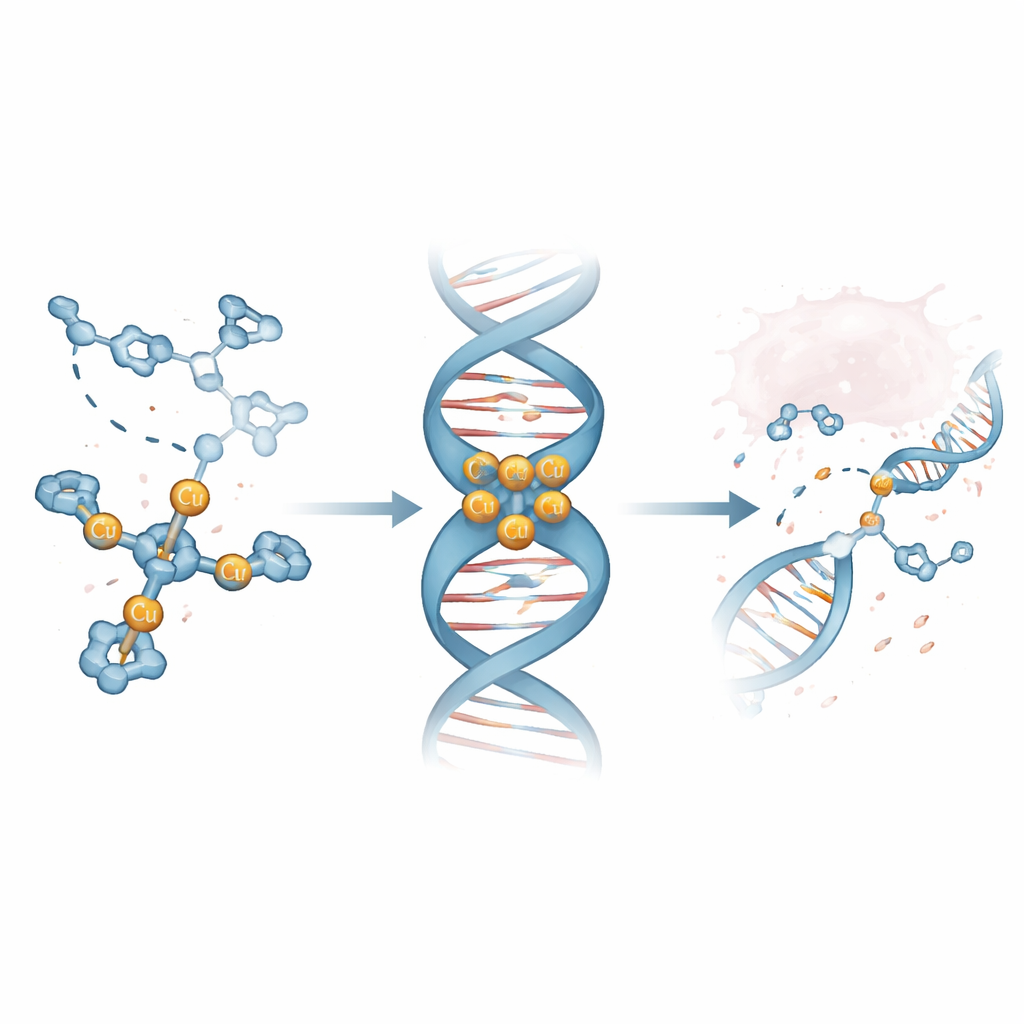
Grâce à la spectrométrie de masse et à des méthodes optiques, les chercheurs ont montré qu’un complexe, nommé Cu3-TC-Py, forme de façon fiable un cluster à trois cuivres stable en solution. Des expériences de compétition avec des colorants fluorescents liés à l’ADN de thymus de veau ont révélé que Cu3-TC-Py déloge ces colorants à de très faibles concentrations, témoignant d’une forte affinité pour l’ADN. Des tests complémentaires sur de courts segments d’ADN en épingle ont indiqué que ce complexe préfère se nicher dans le sillon mineur — la vallée plus étroite qui entoure la double hélice — et qu’il favorise tout particulièrement les régions riches en appariements G–C. Des simulations informatiques haute résolution ont confirmé ce tableau, montrant le complexe tripode installé dans le sillon, ses charges positives serrant l’ADN chargé négativement et compactant subtilement l’hélice.
De la liaison forte à l’effondrement et à la rupture de l’ADN
Au niveau d’une seule molécule, l’équipe a observé de longues brins d’ADN confinés dans des canaux nano‑dimensionnés interagissant avec Cu3-TC-Py. À faibles doses, le complexe se substituait à un colorant d’allongement, le délogeant au fur et à mesure qu’il se liait dans les sillons. À doses plus élevées, l’ADN commençait à se raccourcir puis à se condenser complètement, cohérent avec une forte attraction électrostatique entre le cluster de cuivre et l’épine dorsale de l’ADN. Lorsqu’on a exposé de l’ADN plasmidique au complexe en présence d’un agent réducteur, les brins sont passés de leur forme enroulée native à des formes relâchées puis complètement linéaires, un schéma indiquant la formation de coupures mono- et bicaténaires. Des tests complémentaires avec des pièges à radicaux ont impliqué des espèces d’oxygène à vie courte — telles que le superoxyde, l’oxygène singulet et les radicaux hydroxyle — comme les véritables outils de coupure générés à proximité du complexe fixé.
Attaquer l’ADN dans les cellules cancéreuses et bactériennes
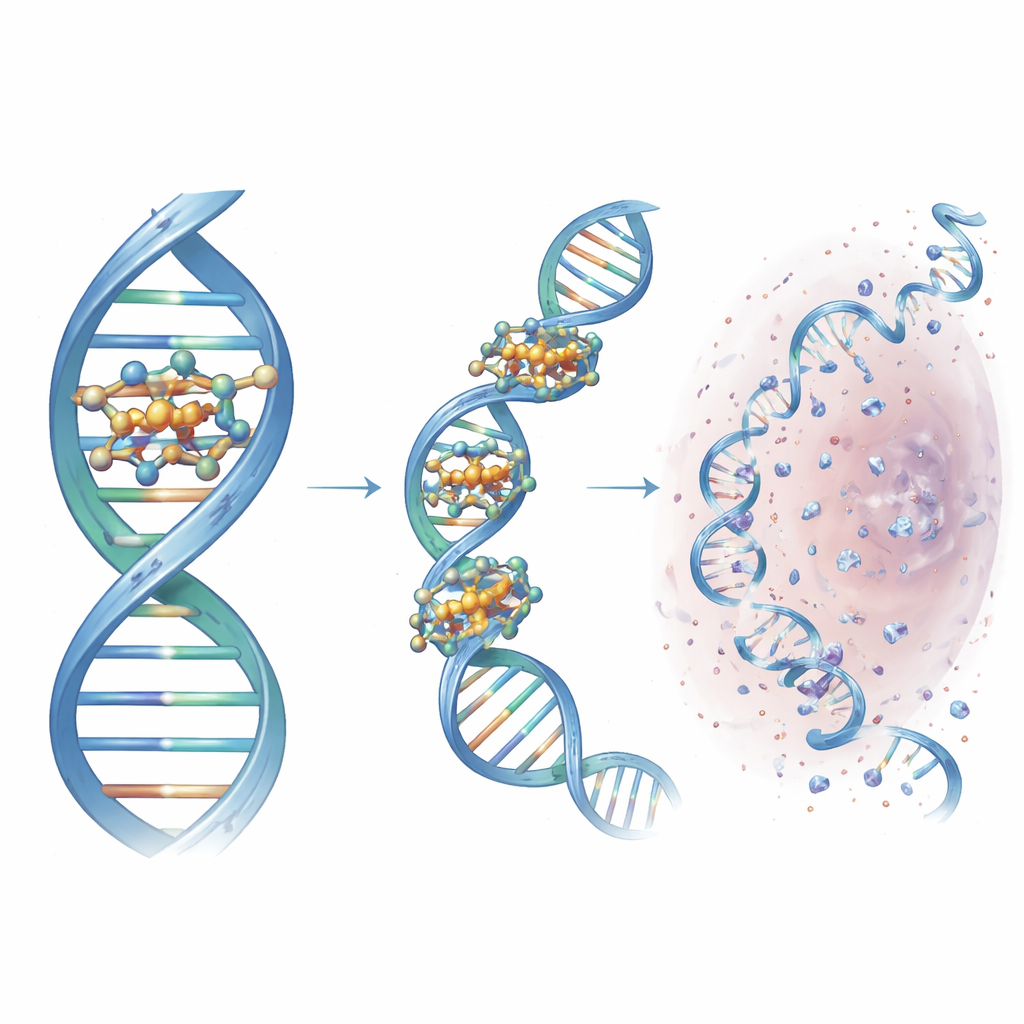
Allant au‑delà de l’ADN purifié, les chercheurs ont examiné le comportement de Cu3-TC-Py à l’intérieur des cellules vivantes. Dans des panels de cellules cancéreuses, les ligands libres contenant des groupes aromatiques riches en azote ont montré une inhibition de croissance bien plus forte que les conceptions antérieures, et le complexe cuivre pleinement formé s’est avéré encore plus puissant, tuant plusieurs lignées cancéreuses à des concentrations micromolaires. Des mesures du cuivre intracellulaire ont révélé que Cu3-TC-Py transporte efficacement le cuivre dans les cellules et déclenche une accumulation d’ADN endommagé, détectée par une méthode d’imagerie assistée par réparation qui marque les lésions le long de brins génomiques étirés. Chez les bactéries, la microscopie a montré qu’un traitement perturbe rapidement le chromosome bactérien compact, dispersant l’ADN dans toute la cellule et reproduisant la fragmentation sévère observée avec un antibiotique fortement endommageant l’ADN, cohérent avec une destruction génétique étendue.
Pourquoi ces ciseaux sur mesure sont importants
Pour le non-spécialiste, le message clé est que les chercheurs ont transformé un échafaudage simple et modulaire issu de la chimie click en une machine de coupe de l’ADN finement réglée. En choisissant les bons groupes azotés cycliques, ils ont créé un cluster de cuivre compact qui s’ancre dans un sillon spécifique de l’ADN, rapproche les brins et génère localement des espèces réactives de l’oxygène qui tranchent la double hélice. Ce composé principal, Cu3-TC-Py, endommage efficacement l’ADN tant dans les cellules cancéreuses que bactériennes et montre comment la conception rationnelle peut affiner l’action des médicaments à base de métal. Bien qu’il reste beaucoup de travail avant une utilisation clinique, l’étude établit des règles de conception pour la prochaine génération de ciseaux moléculaires qui pourraient un jour offrir des thérapies anticancéreuses plus ciblées et de nouvelles stratégies antimicrobiennes.
Citation: Gibney, A., Sidarta, M., Delahunt, E. et al. Expanding the DNA damaging potential of artificial metallo-nucleases with click chemistry. Nat Commun 17, 2309 (2026). https://doi.org/10.1038/s41467-026-68911-5
Mots-clés: chimie click, lésions de l’ADN, complexes de cuivre, agents anticancéreux, nucléases artificielles