Clear Sky Science · fr
Réaffectation évolutive d’un complexe thiolase métabolique permettant la biosynthèse d’un antibiotique
Comment des microbes quotidiens réinventent leur chimie
Nombre des antibiotiques et médicaments sur lesquels nous comptons sont discrètement synthétisés par des bactéries. Ces petits chimistes utilisent des enzymes — des machines moléculaires — pour assembler des composés défensifs complexes. Cette étude révèle comment un complexe enzymatique central du métabolisme, autrefois consacré à l’entretien cellulaire de base, a été réorienté par évolution chez des bactéries buccales pour fabriquer un antibiotique puissant. Comprendre cette transformation montre non seulement comment la nature invente de nouvelles réactions chimiques, mais donne aussi des pistes pour concevoir des médicaments et des biocatalyseurs de nouvelle génération.
Du métabolisme de base à l’armement chimique
Toutes les cellules vivantes dépendent d’un ensemble d’enzymes conservées qui gèrent leur métabolisme central, par exemple la dégradation des lipides et la synthèse de molécules essentielles. Un de ces groupes, la superfamille des thiolases, aide habituellement à traiter de petits vecteurs d’énergie comme l’acétyl-CoA et soutient des voies vitales pour la fabrication des lipides et d’autres composants cellulaires. Les auteurs ont découvert que, chez plusieurs espèces orales de Streptococcus, un complexe à trois composantes basé sur une thiolase — composé de protéines apparentées à HMGS, ACAT et d’un troisième protéine auxiliaire — a abandonné son rôle métabolique ancestral. Ce complexe achève désormais la biosynthèse d’un antibiotique nommé reutericycline A, qui aide ces bactéries à rivaliser dans l’environnement encombré de la bouche.
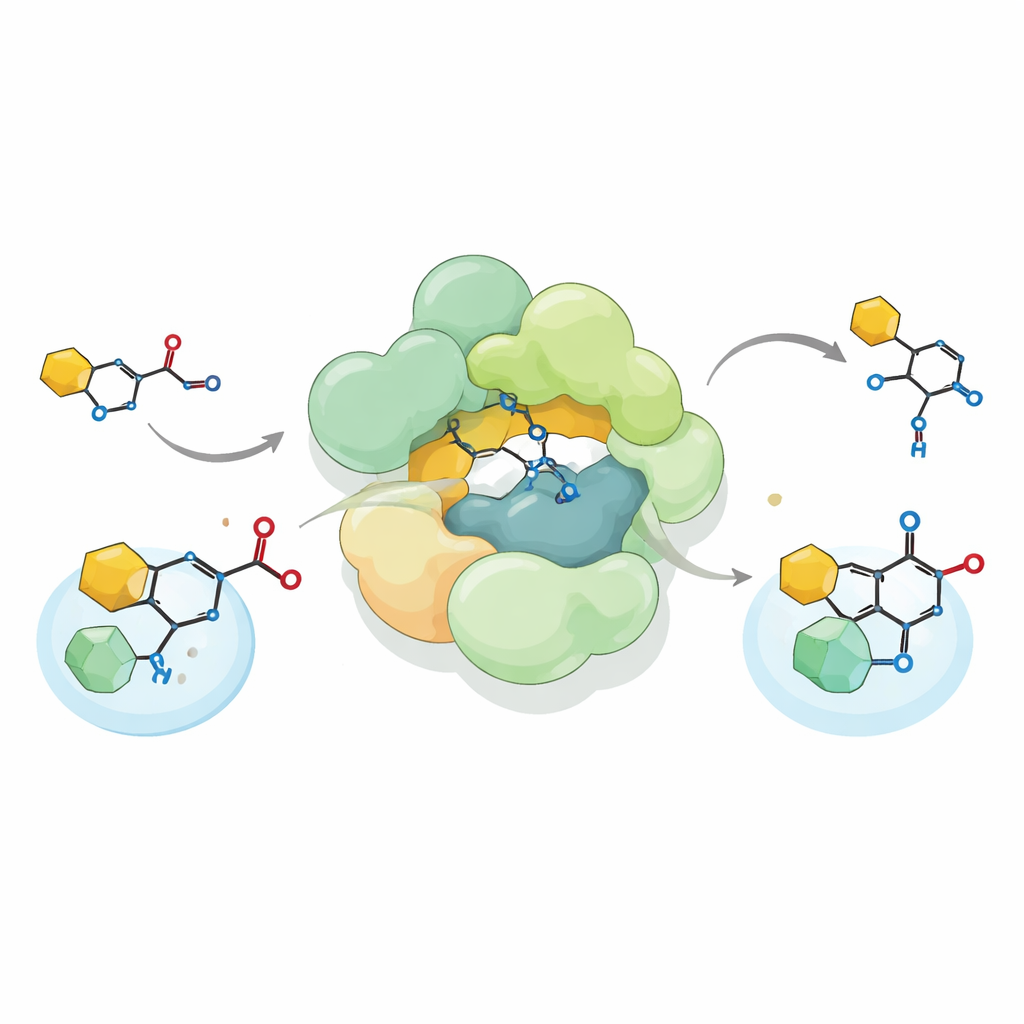
Un nouveau type de réaction enzymatique sur un échafaudage antibiotique
En reconstituant le complexe de Streptococcus en laboratoire et en lui fournissant un précurseur synthétique de la reutericycline A, les chercheurs ont montré que le complexe réalise une réaction inhabituelle de formation de liaison carbone–carbone connue sous le nom d’acylation de Friedel–Crafts en C. Plutôt que d’attacher un groupe acétyle sur un oxygène, comme le font nombre d’enzymes, il installe ce groupe directement sur un atome de carbone d’un noyau pyrrolidine-2,4-dione — une partie importante de l’ossature de la reutericycline. Le complexe accepte à la fois des donneurs d’acétyle naturels tels que l’acétyl-CoA et plusieurs donneurs artificiels, et peut même effectuer la réaction en sens inverse, rompant la liaison qu’il a formée. Cette flexibilité élargit le répertoire connu des acyltransférases biologiques et suggère comment de telles enzymes pourraient être adaptées pour construire des produits chimiques divers.
Réaffecter un échafaudage protéique conservé
À l’aide de cryo-microscopie électronique à haute résolution, l’équipe a résolu la structure tridimensionnelle du complexe de Streptococcus, nommé SmaATase. Malgré sa nouvelle fonction, SmaATase conserve une ressemblance architecturale frappante avec un complexe apparenté chez les archées qui participe à la voie du mévalonate pour la synthèse des lipides isoprénoïdes. Les deux sont de grandes assemblées multimériques construites à partir de modules répétitifs et présentent une cavité commune où le cofacteur CoA peut se lier et se déplacer entre des sites actifs. Cependant, des résidus catalytiques clés, essentiels pour la réaction métabolique originale, sont absents ou altérés dans la version bactérienne. Des tests biochimiques confirment que SmaATase ne peut plus fabriquer le produit ancestral HMG-CoA et utilise désormais l’acétyl-CoA uniquement comme donneur pour ses nouveaux substrats de faible masse moléculaire.
Une piste évolutive du métabolisme aux antibiotiques
Pour comprendre comment une telle réaffectation a pu se produire, les auteurs ont comparé les séquences et les activités de complexes apparentés chez de nombreuses bactéries et archées. Ils ont identifié plus d’un millier de clusters géniques contenant le même trio de types d’enzymes. Certains soutiennent encore la chimie thiolase classique ; d’autres, comme ceux de Pseudomonas, alimentent la production de différents antibiotiques de faible masse moléculaire. Un complexe représentatif de Pseudomonas fluorescens semble se situer à mi-chemin de ce parcours évolutif : son domaine de type HMGS est désactivé, mais son unité de type ACAT réalise encore une réaction plus conventionnelle sur des substrats liés au CoA. Dans SmaATase et son homologue de Pseudomonas qui produit le composé protecteur des cultures DAPG, des modifications supplémentaires autour du site actif ont adapté les enzymes à reconnaître des accepteurs non standards tels que des noyaux aromatiques ou des cœurs d’acide tétramique.
Pourquoi un petit groupe acétyle change tout
Au final, l’intérêt biologique de cette métamorphose moléculaire est évident. Lorsque l’équipe a testé les antibiotiques acétylés reutericycline A et DAPG sur un panel de bactéries à Gram positif, ces molécules ont montré une forte activité létale, alors que leurs précurseurs non acétylés étaient beaucoup moins actifs, voire presque inactifs. Ce petit groupe acétyle, placé au bon endroit par le complexe enzymatique réaffecté, transforme un échafaudage modeste en une arme puissante, permettant à Streptococcus dans la bouche ou à Pseudomonas autour des racines des plantes de éliminer leurs concurrents. Ce travail illustre comment l’évolution peut recycler des architectures enzymatiques existantes par des mutations minimes mais stratégiques, convertissant des machines métaboliques routinières en outils spécialisés de défense chimique — et fournit un modèle pour les ingénieurs qui veulent concevoir de nouveaux catalyseurs de formation de liaisons carbone–carbone pour la découverte de médicaments et la biologie synthétique.
Citation: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Mots-clés: évolution des enzymes, biosynthèse de produits naturels, chimie des antibiotiques, réaffectation métabolique, acylation de Friedel-Crafts