Clear Sky Science · fr
Conception de plasmides avec des origines de réplication synthétiques
Pourquoi réécrire l'ADN microbien compte
Beaucoup des outils derrière la biotechnologie moderne, de la production d'insuline aux circuits génétiques de pointe, reposent sur de petits cercles d'ADN appelés plasmides. Ces actifs génétiques transportent des gènes modifiés dans les bactéries, mais leur conception de base a peu évolué depuis des décennies. Cette étude montre que le cœur même des plasmides — les séquences qui indiquent aux cellules quand et à quelle fréquence les copier — peut être complètement repensé. En reconstruisant de zéro ce « moteur de copie », les auteurs créent des plasmides plus faciles à régler, combiner et programmer, ouvrant la voie à des diagnostics, une bioproduction et une biologie synthétique plus flexibles.
Des outils anciens aux limites cachées
Les plasmides ont évolué naturellement comme de l'ADN mobile, aidant les bactéries à partager des traits tels que la résistance aux antibiotiques ou de nouvelles capacités de digestion. Au laboratoire, les ingénieurs empruntent ces plasmides pour transporter des gènes utiles, mais la plupart reposent sur quelques modèles classiques découverts dans les années 1980. Ces conceptions anciennes cachent un enchevêtrement de parties génétiques qui contrôlent le nombre de copies d'un plasmide par cellule et la coexistence pacifique de plasmides différents. Parce que ces éléments sont fusionnés, modifier une caractéristique peut de façon imprévisible en casser une autre. En conséquence, les scientifiques restent limités à un choix restreint de plasmides avec des nombres de copies fixes et une compatibilité limitée, ce qui restreint la complexité des systèmes conçus.
Reconstruire le moteur de copie depuis zéro
Les chercheurs se sont concentrés sur une origine de réplication largement utilisée issue de la famille des plasmides pMB1. À l'état naturel, cette origine repose sur un équilibre délicat entre deux ARN — l'un qui déclenche la copie de l'ADN et l'autre qui l'arrête — pour maintenir le nombre de plasmides. L'équipe a d'abord « refactorisé » ce système : elle a séparé des gènes qui se chevaupaient, désactivé un promoteur enfoui et placé les éléments clés sur des cassettes génétiques propres et distinctes. Cela a montré que la fonction fondamentale de l'origine pouvait être préservée tout en simplifiant son architecture, transformant une pièce façonnée par l'évolution en quelque chose de plus modulaire, avec des composants accessibles.
Remplacer par des boutons de contrôle synthétiques
Avec la logique de contrôle exposée, les auteurs ont ensuite remplacé le système par des régulateurs entièrement synthétiques. Ils ont relié l'amorce de réplication à des interrupteurs ARN conçus qui fonctionnent comme des boutons de variateur : de petits ARN régulateurs peuvent activer ou bloquer la production de l'amorce et, par conséquent, la copie du plasmide. En choisissant différents variants d'interrupteurs et en les associant à des promoteurs de forces variées, ils ont réglé le nombre de copies sur plus de deux ordres de grandeur. Ils ont aussi exploré différentes configurations physiques des cassettes de contrôle sur l'ADN, découvrant des agencements qui améliorent la stabilité et qui leur ont permis de réduire la région de réplication à un noyau compact et fonctionnel tout en ajoutant des systèmes d'aide naturels pour prévenir les enchevêtrements problématiques entre plasmides.
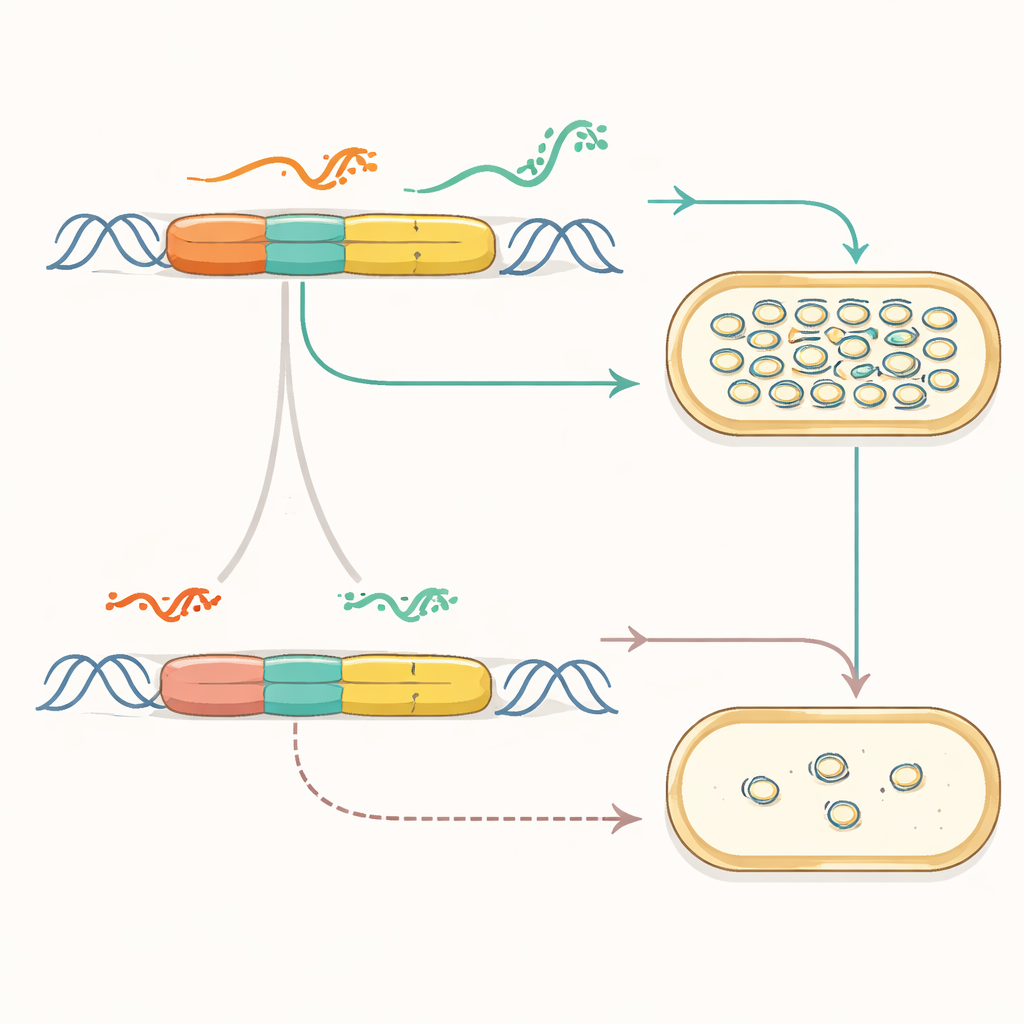
Transformer des signaux chimiques en nombres d'ADN
Une fois le moteur de copie rendu modulaire, l'équipe a montré qu'il pouvait être connecté pour détecter le milieu extérieur. Ils ont relié l'origine synthétique à des promoteurs inductibles et à des structures ARN appelées riboswitchs, qui changent de conformation en réponse à de petites molécules. Dans ces nouveaux plasmides, l'ajout d'un composé comme l'IPTG ou le cumate faisait augmenter ou diminuer le nombre de copies du plasmide — et donc le signal d'un témoin. Plusieurs signaux pouvaient être combinés, de sorte qu'une molécule stimule la copie tandis qu'une autre la freine. Les chercheurs ont même construit des paires de plasmides, chacun répondant à une molécule différente, et suivi leurs nombres de copies changeants dans la même cellule par séquençage de l'ADN, transformant ainsi les comptes de plasmides en un code-barres de l'histoire environnementale.
Plusieurs plasmides personnalisés dans une même cellule
Un test clé de cette approche était de savoir si plusieurs plasmides contrôlés indépendamment pouvaient coexister. En puisant dans une bibliothèque de régulateurs ARN orthogonaux, l'équipe a construit six plasmides différents, chacun avec sa propre origine synthétique et son marqueur antibiotique, et a introduit les six simultanément dans E. coli. Le séquençage des plasmides complets sur plusieurs jours a confirmé que les six restaient présents, même si leurs abondances relatives évoluaient. Les tentatives avec six plasmides conventionnels ont échoué, ce qui souligne comment la conception refactorisée et les systèmes de stabilité ajoutés rendent les nouveaux plasmides plus compatibles et robustes lorsqu'ils sont nombreux dans une même cellule.
Ce que cela signifie pour la biotechnologie future
Pour un non-spécialiste, la conclusion est simple : les auteurs ont transformé les plasmides d'outils rigides et universels en une plateforme personnalisable. Leurs origines de réplication synthétiques fonctionnent comme des moteurs modulaires dont la vitesse, la sensibilité et les entrées peuvent être choisies à la demande. Cela rend possible la construction de bactéries qui enregistrent des expositions chimiques sous forme de variations du nombre de copies d'ADN, le test parallèle de nombreuses voies génétiques en les répartissant sur plusieurs plasmides, ou l'équilibrage fin de croissance et de production dans des souches industrielles. Bien que certains compromis de stabilité subsistent, ce travail montre que les mécanismes fondamentaux de la réplication des plasmides ne sont plus hors de portée pour l'ingénierie, ouvrant de nouveaux espaces d'innovation en biologie synthétique.
Citation: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
Mots-clés: plasmides synthétiques, origine de réplication, régulateurs ARN, contrôle du nombre de copies, biologie synthétique