Clear Sky Science · fr
Le récepteur du succinate 1 limite l’hématopoïèse et empêche la progression de la leucémie myéloïde aiguë
Lorsque le carburant cellulaire déraille
Notre sang est constamment renouvelé par une petite population de cellules souches nichées dans la moelle osseuse. Cette étude examine comment un sous-produit métabolique courant, le succinate, et son capteur à la surface cellulaire jouent le rôle de frein sur ce système de renouvellement. Quand ce frein lâche, l’équilibre entre production sanguine saine et croissance cancéreuse peut basculer vers la leucémie myéloïde aiguë (LMA), un cancer du sang agressif. Comprendre cet interrupteur de contrôle caché pourrait conduire à des traitements plus précis qui maîtrisent la maladie en restaurant les mécanismes de protection de l’organisme.
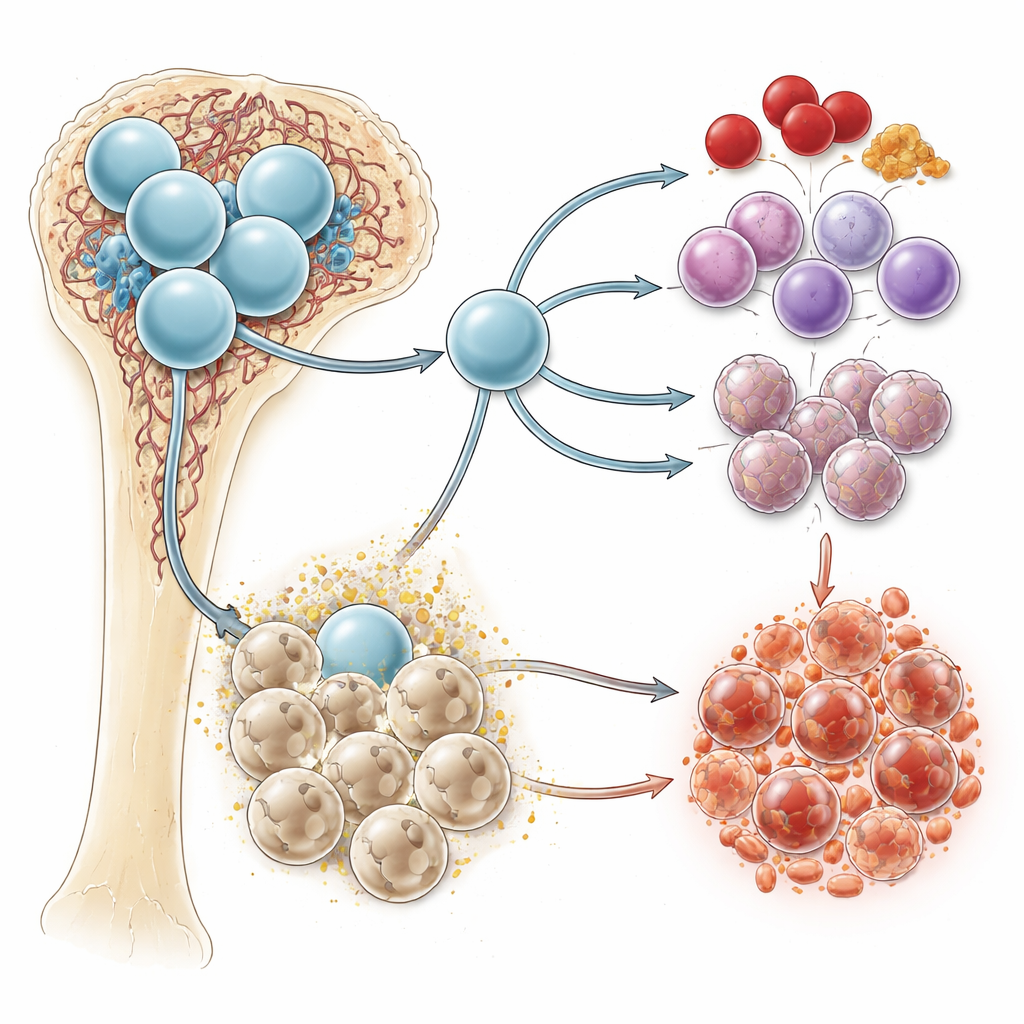
Un signal chimique à double visage
Le succinate est un sous-produit courant de la combustion du carburant cellulaire, en particulier dans les mitochondries, les centrales énergétiques de la cellule. En conditions de faible oxygénation — comme dans la moelle osseuse — le succinate tend à s’accumuler. Il peut agir à l’intérieur des cellules, modifiant le métabolisme et les réponses inflammatoires, et peut aussi être libéré à l’extérieur pour servir de signal. À la surface cellulaire, un récepteur appelé SUCNR1 détecte le succinate et transmet cette information vers l’intérieur. Des travaux antérieurs avaient lié le succinate et SUCNR1 à l’inflammation et à des environnements favorables au cancer, mais leur rôle direct dans la formation du sang et la leucémie restait flou.
Un signe d’alerte chez les patients leucémiques
Les chercheurs ont analysé des données d’expression génique provenant de centaines de patients atteints de LMA et ont découvert que les niveaux de SUCNR1 variaient largement d’un individu à l’autre. Les patients dont les cellules leucémiques produisaient peu de SUCNR1 présentaient une survie globale et sans progression plus courte, même après ajustement sur l’âge, le sexe et les sous-types cliniques usuels. Certains sous-groupes génétiques de LMA présentaient particulièrement de faibles niveaux de SUCNR1. Lorsque l’équipe a transplanté des cellules de LMA humaines dépourvues de SUCNR1 dans des souris immunodéficientes, puis injecté aux animaux de l’acide succinique (qui devient succinate dans l’organisme), la charge leucémique dans la moelle osseuse a augmenté. Cela suggère que, dans les cancers à faible SUCNR1, un excès de succinate peut en réalité alimenter la progression de la maladie plutôt que la freiner.
Le frein caché des cellules souches sanguines
Pour comprendre comment SUCNR1 agit dans l’hématopoïèse normale, les scientifiques se sont tournés vers des souris génétiquement modifiées. Lorsque SUCNR1 était supprimé, soit dans l’ensemble de l’animal soit seulement dans les cellules formatrices du sang, la moelle osseuse devenait hyperactive. Les cellules souches et progénitrices se sont accrues, et à la fois les cellules myéloïdes (telles que monocytes et granulocytes) et les cellules B ont augmenté dans le sang et la rate. Ces cellules aux caractéristiques de souches survivaient mieux et formaient davantage de colonies en culture, bien qu’elles aient été légèrement moins capables de rétablir la production sanguine lorsqu’elles étaient transplantées en compétition avec des cellules normales. Une lignée de souris rapporteur spéciale a montré qu’un sous-ensemble seulement des cellules souches et progénitrices exprime SUCNR1 ; ces cellules SUCNR1-positives avaient un potentiel d’implantation particulièrement limité. Dans l’ensemble, le récepteur agissait comme une contrainte sur la taille et l’activité du réservoir de cellules souches.
D’une défense équilibrée à l’emballement inflammatoire
Le profilage détaillé de l’expression génique des cellules souches et progénitrices dépourvues de SUCNR1 a révélé un basculement marquant. Les signatures des cellules souches primitives et au repos étaient atténuées, tandis que les gènes liés à l’inflammation, aux espèces réactives de l’oxygène et aux cellules sanguines matures étaient amplifiés. Deux molécules se détachaient : S100A8 et S100A9, une paire d’« alarmins » qui amplifient la signalisation inflammatoire. Ces facteurs étaient augmentés à la fois dans le compartiment des cellules souches et dans le liquide environnant de la moelle osseuse. Lorsque l’équipe a traité les souris dépourvues de SUCNR1 avec la tasquinimod, un médicament qui bloque la signalisation de S100A9, l’expansion excessive des cellules souches et progénitrices ainsi que la surproduction de cellules myéloïdes et B ont été largement inversées. Autrement dit, une grande partie des effets délétères de la perte de SUCNR1 pouvait être annulée en interrompant la boucle d’alarme S100A8/S100A9.
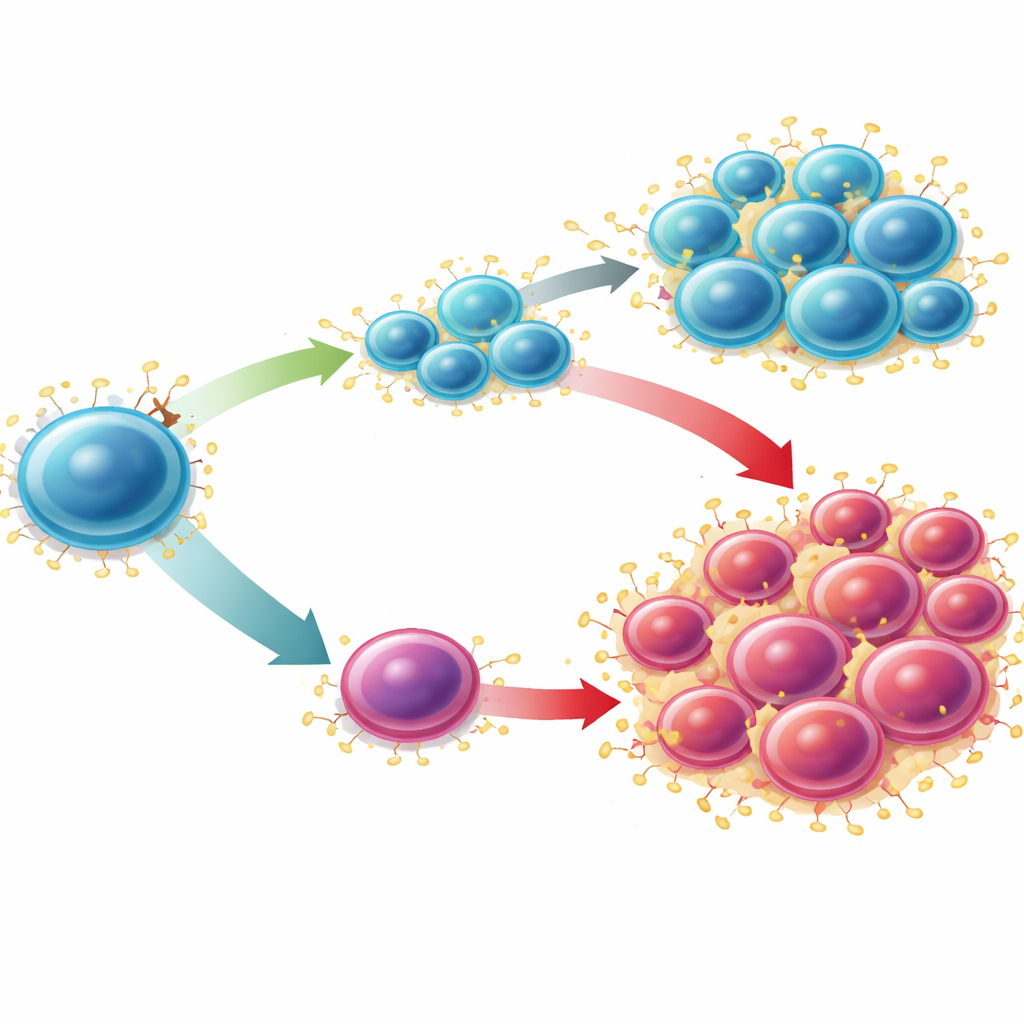
Transformer une vulnérabilité en stratégie thérapeutique
Les scientifiques ont ensuite cherché à savoir si cette voie pouvait être exploitée en thérapeutique pour la LMA. Dans une leucémie murine agressive pilotée par la mutation MLL-AF9 — où les niveaux de Sucnr1 sont très bas — le blocage de S100A9 avec la tasquinimod, surtout lorsqu’il était combiné à un composé activateur puissant de SUCNR1, a réduit les cellules souches leucémiques et allégé la charge tumorale dans la moelle osseuse et la rate. Les analyses de données d’ARN unicellulaire provenant de modèles humains de LMA traités par la chimiothérapie cytarabine ont montré que les grappes cellulaires résistantes étaient riches en S100A8 et S100A9, tandis que SUCNR1 était rare et associé à un sous-ensemble différent, métaboliquement actif, qui diminuait après le traitement. Dans des lignées cellulaires leucémiques humaines, l’activation de SUCNR1 augmentait la mort cellulaire induite par la chimiothérapie et pouvait déclencher l’apoptose à elle seule lorsque SUCNR1 était surproduit. Ensemble, ces résultats placent un faible SUCNR1 non seulement comme un marqueur de mauvais pronostic mais aussi comme une faiblesse : les cellules leucémiques qui ont perdu ce frein peuvent dépendre fortement de l’axe S100A8/S100A9 et être particulièrement sensibles aux stratégies qui réactivent la signalisation SUCNR1 ou bloquent l’alarme en aval.
Un nouveau levier pour maîtriser la leucémie
Pour le lecteur non spécialiste, le message central est qu’un sous-produit métabolique apparemment banal, le succinate, et son récepteur SUCNR1 forment un système de sécurité inattendu dans la formation du sang. Quand SUCNR1 est présent et actif, il maintient les cellules souches sous contrôle et empêche une prolifération incontrôlée. Quand SUCNR1 est perdu ou faible — fréquent chez certains patients atteints de LMA — le succinate et des alarmins inflammatoires comme S100A8 et S100A9 peuvent pousser les cellules souches et progénitrices vers une expansion excessive et la leucémie. En combinant des médicaments qui atténuent cette alarme inflammatoire avec des agents qui rétablissent ou miment la signalisation SUCNR1, il pourrait être possible de réorienter le système vers une production sanguine équilibrée et d’améliorer l’efficacité des chimiothérapies existantes.
Citation: Cuminetti, V., Boet, E., Heugel, M. et al. Succinate receptor 1 restricts hematopoiesis and prevents acute myeloid leukemia progression. Nat Commun 17, 2403 (2026). https://doi.org/10.1038/s41467-026-68906-2
Mots-clés: leucémie myéloïde aiguë, récepteur du succinate, cellules souches hématopoïétiques, métabolisme et cancer, signalisation inflammatoire