Clear Sky Science · fr
Des oxydases d’alcool conçues catalysent la transestérification en milieu aqueux sans hydrolyse concurrente
Pourquoi cette découverte enzymatique compte
De nombreux produits du quotidien, des médicaments et arômes alimentaires jusqu’au biodiesel, reposent sur un type simple de liaison chimique appelé ester. Produire et modifier ces esters de manière efficace, économique et respectueuse de l’environnement est un objectif majeur de la chimie verte. Le problème est que l’eau —solvant idéal du point de vue de la sécurité et de la durabilité— sabote généralement ces réactions en décomposant les esters aussi vite qu’ils sont formés. Cette étude met au jour une enzyme conçue qui peut synthétiser des esters en milieu aqueux tout en ignorant presque complètement l’eau environnante, ouvrant la voie à une chimie industrielle plus propre.
Transformer une enzyme connue pour une nouvelle fonction
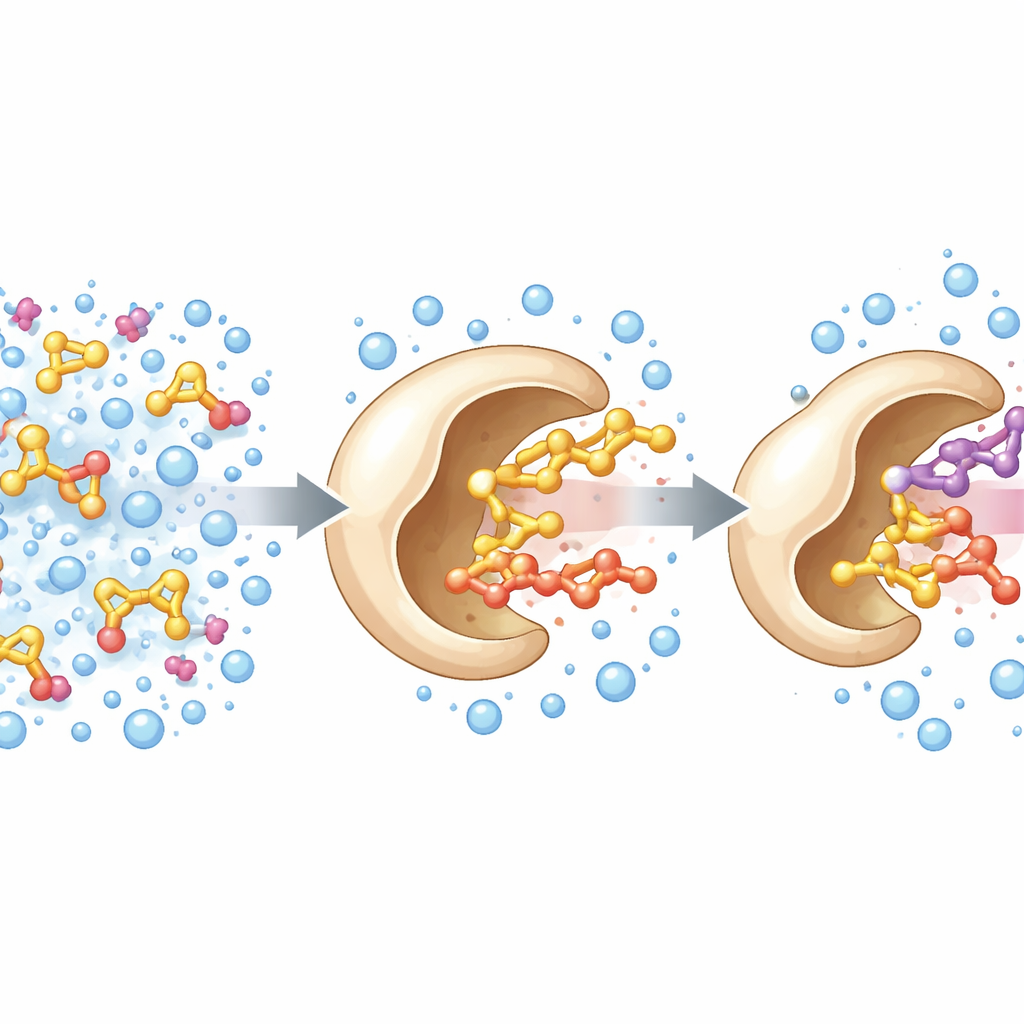
Les chercheurs sont partis d’une enzyme connue, une alcool oxydase issue d’un champignon saprophyte du bois. Dans la nature, cette enzyme utilise un cofacteur flavine pour arracher des électrons à de petits alcools comme le méthanol. L’équipe a cherché à en élargir la portée afin qu’elle accepte des alcools plus volumineux, plus pertinents pour les produits fins et les arômes. En s’appuyant sur la structure tridimensionnelle de l’enzyme comme feuille de route, ils ont ciblé trois acides aminés qui forment une sorte de passage d’accès au site actif. En randomisant ces positions et en criblant les variantes obtenues, ils ont découvert un triple mutant — nommé PcAOx‑VPN — capable de traiter efficacement des alcools plus gros comme le benzylalcool tout en perdant une grande partie de son activité originale envers de très petits alcools tels que le méthanol.
Talent inattendu : synthétiser des esters en eau
Lors des tests de PcAOx‑VPN dans des mélanges destinés à solubiliser des substrats huileux, l’équipe a observé des signaux supplémentaires dans leurs analyses. Il s’agissait d’acétates : l’enzyme transférait un groupe acyle d’un donneur d’ester activé vers des alcools, une réaction connue sous le nom de transestérification. Fait remarquable, cela se produisait dans un tampon aqueux, situation qui conduit habituellement à une hydrolyse concurrente intense où l’eau attaque et détruit l’ester. Ici, PcAOx‑VPN associait efficacement alcools et donneurs d’acyle comme l’acétate de vinyle pour former de nouveaux esters, souvent avec des rendements supérieurs à 80 % et avec seulement des réactions secondaires modestes. La même enzyme pouvait même agir sur une grande variété d’alcools — linéaires, aromatiques, chiraux et contenant du soufre — et montrait dans plusieurs cas une nette préférence pour l’un des énantiomères.
Écarter l’eau du mécanisme
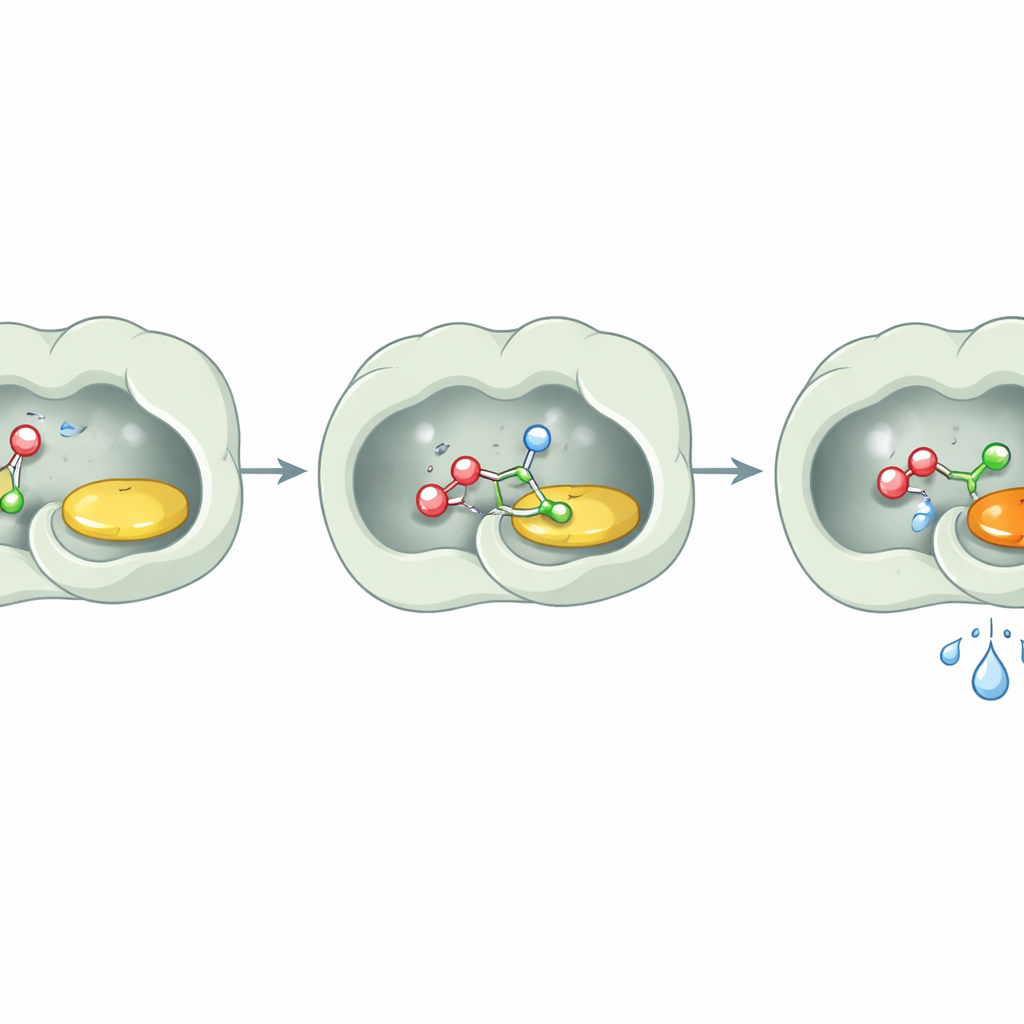
Une surprise clé fut ce que l’enzyme ne faisait pas : elle n’hydrolysait pas les esters de façon notable. Même après de longues incubations avec des substrats esters en présence d’eau, PcAOx‑VPN les laissait essentiellement intacts sauf si un donneur d’acyle supplémentaire était fourni. Les études structurales offrent une explication simple. Le site actif est bordé d’acides aminés majoritairement apolaires et aromatiques qui créent une poche très hydrophobe. Les analyses détaillées n’ont montré aucune molécule d’eau proche du cofacteur flavine, et les outils de modélisation ont confirmé que le canal menant au site actif est également peu accueillant pour l’eau. En substance, l’enzyme aménage une petite chambre sèche à l’intérieur d’un milieu aqueux. Les alcools et les esters activés peuvent y pénétrer et réagir, mais les molécules d’eau en sont tenues à distance et n’ont ainsi jamais l’occasion de détruire le produit.
Comment la réaction fonctionne probablement à l’intérieur
Des expériences mécanistiques et des analyses de mutations ont révélé que deux acides aminés, une histidine et une asparagine, sont centraux tant pour le rôle naturel d’oxydation de l’enzyme que pour sa nouvelle capacité de transestérification. L’histidine agit comme une base en aidant à arracher un proton à l’alcool entrant pour le rendre plus réactif, tandis que l’asparagine stabilise l’état chargé qui en résulte. Ensemble, ils favorisent l’attaque de l’alcool sur le donneur d’acyle pour former un intermédiaire de courte durée qui s’effondre en l’ester désiré. L’état oxydé du cofacteur flavine est également requis : en l’absence d’oxygène, lorsque la flavine est réduite, la transestérification s’arrête et ne reprend que lorsque l’air est réintroduit. Notamment, lorsque le même trio de mutations a été introduit dans des oxydases apparentées issues d’autres champignons, ces enzymes ont aussi acquis une activité de transestérification robuste, suggérant que ce comportement peut être généralisé.
Ce que cela signifie pour une chimie plus verte
Pour un public non spécialiste, le message central est que les auteurs ont appris à une enzyme connue un nouveau tour : synthétiser des esters utiles directement en eau, tout en neutralisant la tendance de l’eau à annuler la réaction. En aménageant une poche sèche, favorable aux composés huileux, à l’intérieur d’une protéine et en ajustant quelques acides aminés clés, ils ont créé un catalyseur qui privilégie les alcools plutôt que l’eau comme partenaire réactionnel. Puisque le même principe de conception fonctionne dans des enzymes apparentées, cette approche pourrait être étendue à une famille de catalyseurs pour la fabrication d’arômes, de parfums, de produits fins et éventuellement de biocarburants, dans des procédés plus sûrs et plus durables qui limitent l’usage de solvants organiques agressifs au profit de l’eau.
Citation: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
Mots-clés: ingénierie des enzymes, biocatalyse, chimie verte, synthèse d’esters, flavoprotéines