Clear Sky Science · fr
Une conception sans oxygène de réseau pour un reformage sec du méthane photothermique efficace et stable
Transformer les gaz à effet de serre en carburant utile
Le méthane et le dioxyde de carbone sont deux des gaz à effet de serre les plus puissants qui réchauffent notre planète, mais ils sont aussi de riches sources d’énergie chimique. Cette étude montre comment de minuscules particules métalliques finement conçues peuvent utiliser la lumière et la chaleur ensemble pour convertir ces gaz en gaz de synthèse — un mélange polyvalent d’hydrogène et de monoxyde de carbone — tout en évitant les problèmes habituels qui rendent ces procédés inefficaces et de courte durée.
Pourquoi éliminer le méthane est si difficile
Le reformage sec du méthane est une réaction qui transforme le méthane et le dioxyde de carbone en gaz de synthèse. En industrie, elle exige généralement des températures de four de 700–1000 °C pour avancer assez rapidement. À ces températures, les catalyseurs courants à base de nickel et de cobalt ont tendance à s’agglomérer et à accumuler des dépôts de carbone, perdant ainsi leur activité au fil du temps. Les approches « photothermiques » récentes visent à utiliser une lumière concentrée pour chauffer les catalyseurs de façon plus ciblée et induire des effets électroniques supplémentaires, mais les matériaux actuels gaspillent la majeure partie de la lumière incidente et souffrent encore d’accumulation de carbone et de dégradation du catalyseur.
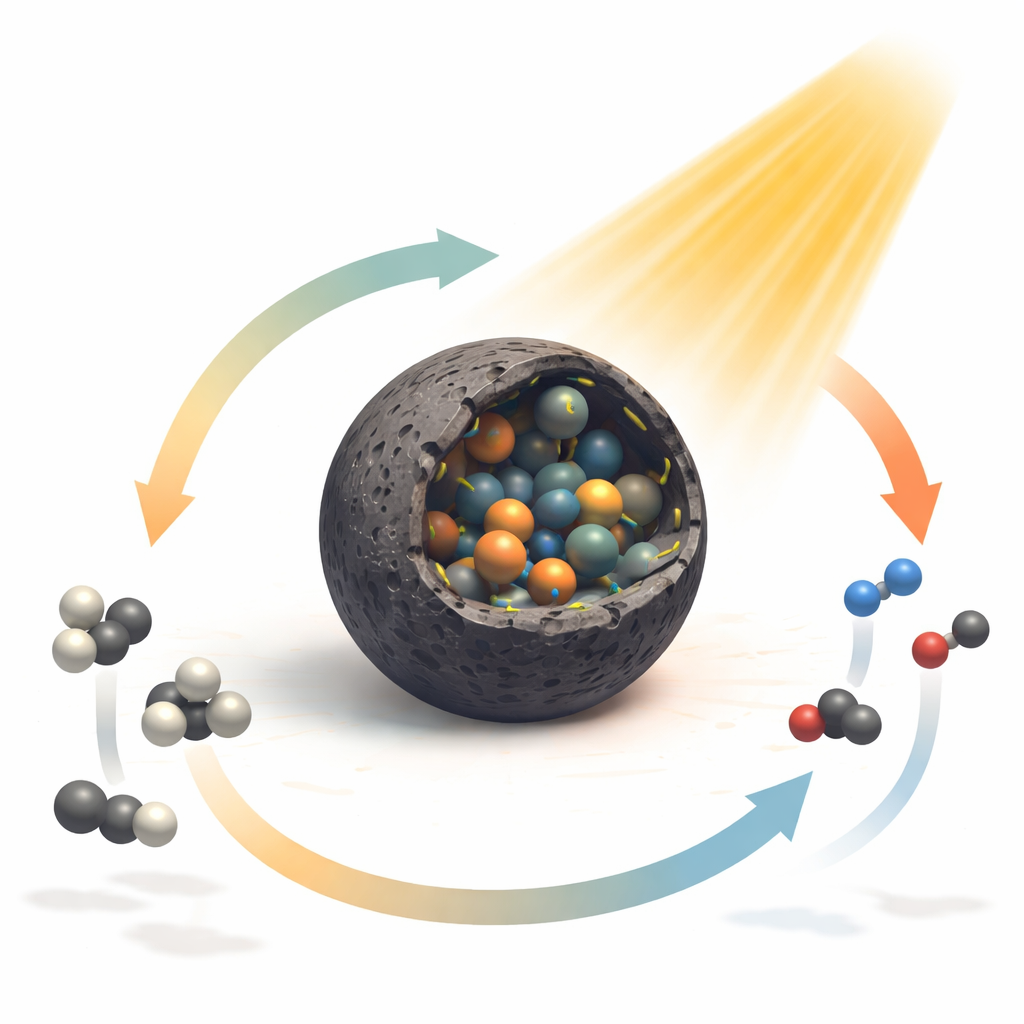
Conception d’un nouveau type d’enveloppe catalytique
Les chercheurs ont relevé ce défi en construisant un catalyseur à partir d’un cadre métal‑organique — un échafaudage cristallin qui arrange des atomes métalliques et des ligands organiques selon un motif régulier. Après un traitement thermique adapté, ce cadre se transforme en particules sphériques recouvertes d’une fine couche de carbone graphitique, à l’intérieur desquelles se logent de très petites nanoparticules d’un alliage nickel‑cobalt. Fait crucial, des atomes d’azote sont intégrés dans la coque carbonée et liés au nickel, formant ce que les auteurs appellent des sites C–N–Ni. Ces liaisons azote‑nickel remodèlent la manière dont les électrons sont partagés entre le nickel et le cobalt et entre les métaux et la couche de carbone, induisant une contrainte subtile du réseau cristallin et transformant la surface en un environnement plus réactif pour les molécules entrantes.
Confier le travail lourd à l’oxygène réactif
Dans les catalyseurs traditionnels pour cette réaction, l’oxygène incorporé dans le réseau solide joue un rôle clé pour briser les liaisons C–H fortes du méthane et nettoyer les fragments de carbone. Mais l’oxygène de réseau est difficile à mobiliser, et son utilisation excessive finit par endommager le catalyseur. Ici, l’équipe a mis au point une voie complètement différente : au lieu de compter sur l’oxygène intrinsèque, ils exploitent des espèces oxygénées et hydroxyles hautement réactives générées directement à partir du dioxyde de carbone durant la réaction. Des expériences et des simulations montrent que la surface nickel‑cobalt modifiée par l’azote adsorbe fortement à la fois le méthane et le dioxyde de carbone, tout en les orientant vers des atomes métalliques différents — le nickel se spécialise dans la rupture du méthane, tandis que le cobalt se concentre sur l’activation du dioxyde de carbone. Les espèces oxygénées réactives formées à partir du dioxyde de carbone oxydent ensuite rapidement les fragments riches en carbone issus du méthane en intermédiaires tels que le formaldéhyde, puis en monoxyde de carbone et dioxyde de carbone, empêchant l’accumulation de carbone solide.
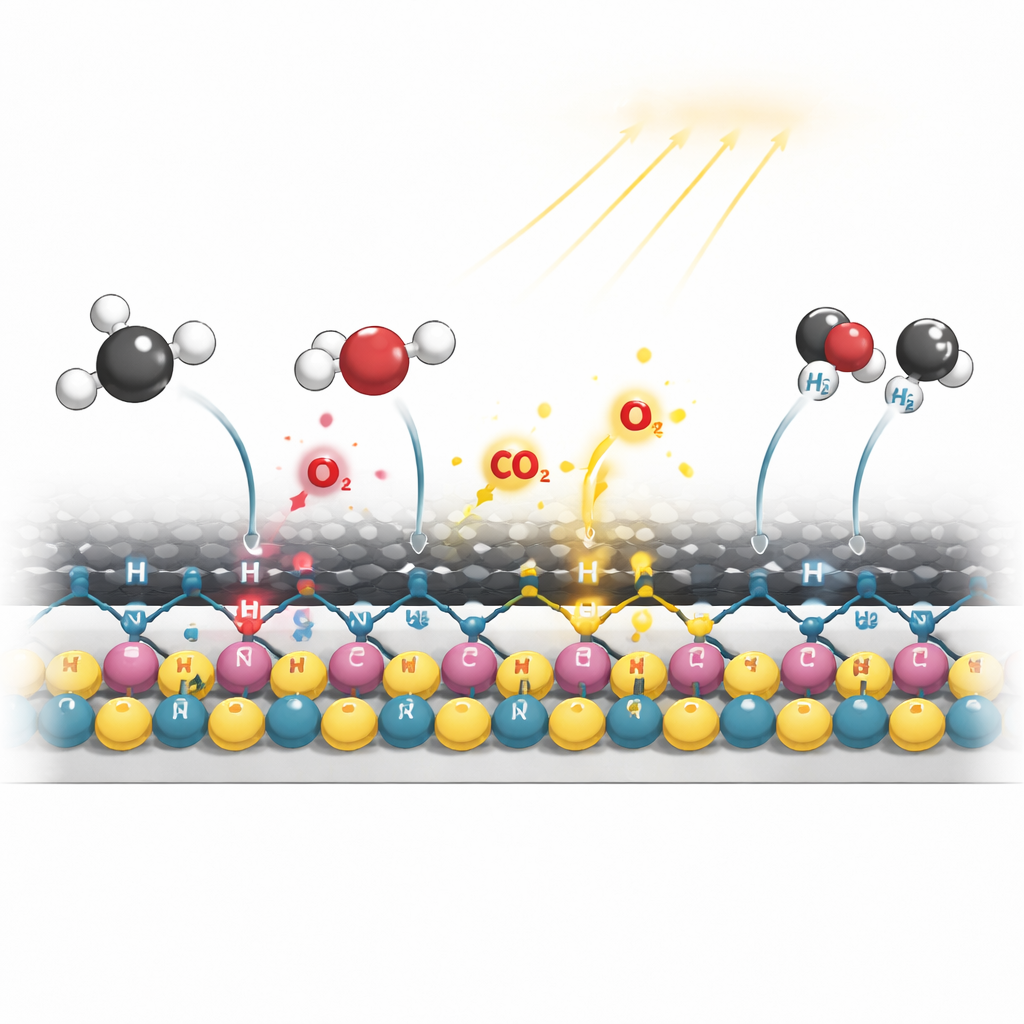
Comment la lumière rend le catalyseur plus intelligent
À l’aide de spectroscopies in situ, les auteurs ont observé ce qui arrive au catalyseur lorsqu’il fonctionne en conditions obscures et illuminées. Sans lumière, les surfaces de nickel et de cobalt ont tendance à s’oxyder, et des réactions secondaires formant de l’eau deviennent plus prononcées, affaiblissant progressivement la performance. Sous illumination, cependant, des électrons excités dans le revêtement carboné sont canalisés le long des voies C–N–Ni vers les sites métalliques. Cette densité électronique supplémentaire aide à maintenir le nickel et le cobalt dans leur état métallique actif, supprime les réactions secondaires indésirables et renforce la formation d’intermédiaires clés tels qu’une espèce COOH liée à la surface qui se scinde en monoxyde de carbone et en radicaux hydroxyles sans attaquer le métal. Des calculs quantiques détaillés confirment que cette voie assistée par la lumière abaisse les barrières énergétiques pour la déshydrogénation du méthane et l’oxydation des fragments carbonés tout en augmentant la barrière pour l’étape qui laisserait autrement des dépôts de carbone tenaces.
Efficacité et stabilité à des conditions plus douces
Le catalyseur optimisé dopé à l’azote, baptisé N1, a produit un gaz de synthèse avec un rapport hydrogène/monoxyde de carbone quasi idéal et a atteint une efficacité lumière‑vers‑énergie chimique d’environ 52 % — compétitive avec, voire supérieure à, de nombreux systèmes solaires rapportés — à une température de fonctionnement relativement modérée de 540 °C. Il a maintenu sa performance pendant 200 heures d’opération continue avec presque aucune trace de restructuration du catalyseur ou d’addition de carbone amorphe. En concevant une voie sans oxygène de réseau qui puise des oxygènes réactifs directement dans le dioxyde de carbone et en guidant les électrons le long de voies azote‑nickel précises, ce travail ouvre la voie à une nouvelle famille de catalyseurs durables assistés par la lumière, capables à la fois de recycler les gaz à effet de serre et de produire des carburants de valeur de façon plus efficace.
Citation: Pan, T., Xu, W., Deng, H. et al. A lattice oxygen-free design for efficient and stable photothermal methane dry reforming. Nat Commun 17, 2151 (2026). https://doi.org/10.1038/s41467-026-68898-z
Mots-clés: reformage sec du méthane, catalyse photothermique, catalyseur NiCo, production de gaz de synthèse, conversion des gaz à effet de serre