Clear Sky Science · fr
La formation de polarons dépendant du potentiel active TiO2 pour la réaction d'évolution de l'hydrogène
Transformer des matériaux semblables à la rouille en producteurs de carburant propre
La division de l'eau en hydrogène combustible repose généralement sur des métaux précieux coûteux. Cette étude montre qu'un oxyde courant et stable, le dioxyde de titane (TiO2), peut passer d'une activité médiocre à une activité élevée simplement en modifiant le potentiel électrique qui lui est appliqué. L'élément clé est la création de petites poches de charge réversibles appelées polarons à la surface, qui ouvrent de nouvelles voies efficaces pour la production de gaz hydrogène.
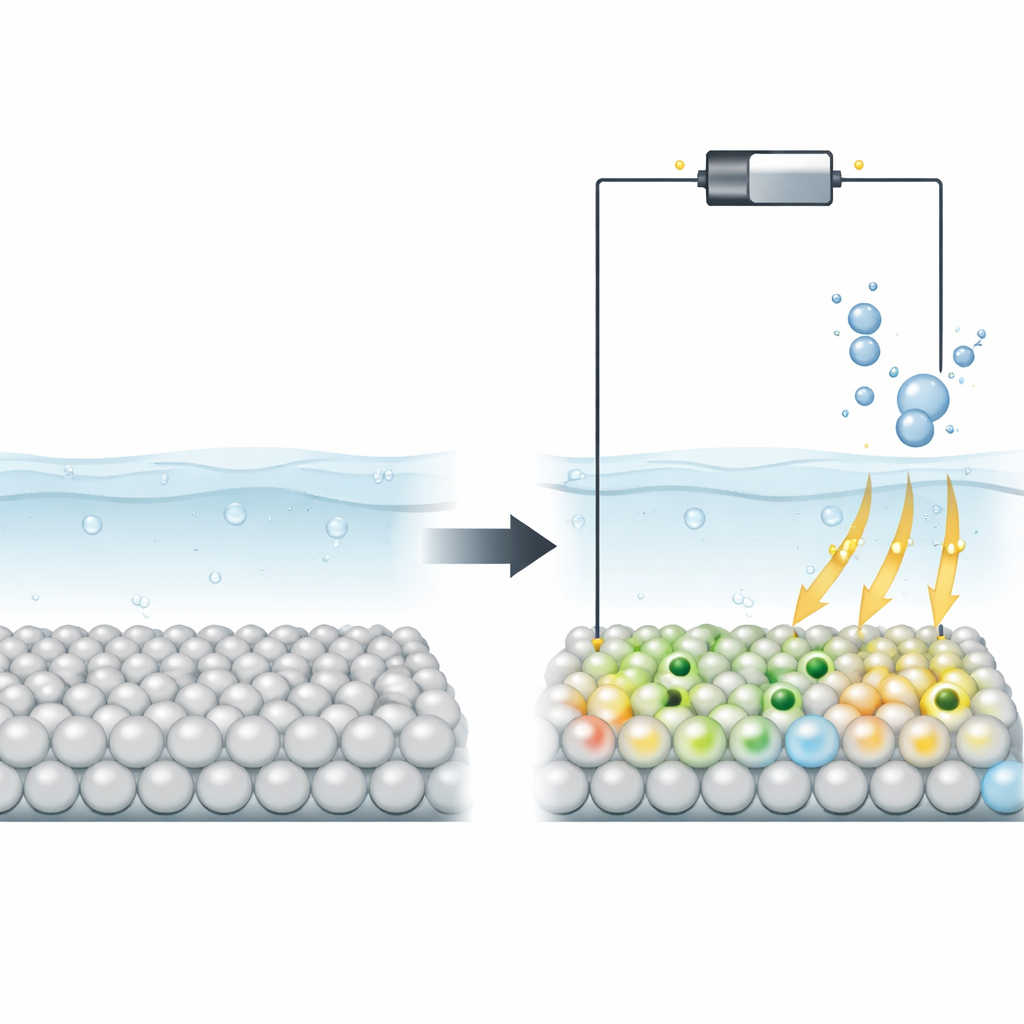
Pourquoi les semi-conducteurs peinent et comment les défauts aident
Les semi-conducteurs comme le TiO2 sont attractifs pour l'énergie propre parce qu'ils sont peu coûteux, abondants et déjà largement utilisés dans les technologies solaires et photocatalytiques. Pourtant, à l'état pur, ils conduisent mal l'électricité et lient souvent les intermédiaires réactionnels soit trop fortement soit trop faiblement, ce qui en fait des catalyseurs médiocres. Les chercheurs ont longtemps tenté de remédier à cela en incorporant des défauts — atomes manquants ou distorsions — lors de la synthèse. Ces modifications permanentes peuvent améliorer les performances mais sont difficiles à contrôler précisément, et il demeurait flou, au niveau atomique, comment ces défauts modifient la surface pour accélérer des réactions comme l'évolution de l'hydrogène.
Créer des poches de charge commutables par tension
Les auteurs proposent une stratégie différente : utiliser le potentiel d'exploitation lui-même pour sculpter en temps réel la structure électronique du TiO2. Lorsqu'un potentiel suffisamment négatif est appliqué, certains ions titane à la surface passent d'un état de charge plus élevé à un état plus faible et piègent des électrons supplémentaires dans des régions localisées connues sous le nom de polarons. En combinant des calculs quantiques à potentiel constant avancés et des mesures spectroscopiques in situ, l'équipe montre que ces polarons ne se forment que en conditions réductrices, qu'ils sont confinés à la couche atomique la plus externe et qu'ils apparaissent et disparaissent de façon réversible lorsque le potentiel est cyclé. Cela signifie que la surface active du catalyseur peut être ajustée dynamiquement pendant le fonctionnement, plutôt que d'être fixée lors de la fabrication.
Défauts, charges mobiles et libération d'hydrogène plus rapide
L'étude examine en outre ce qui se passe lorsque la surface de TiO2 contient déjà des lacunes en oxygène — atomes d'oxygène manquants fréquents dans les matériaux réels. Ces lacunes favorisent la présence d'électrons près de certains atomes de titane, facilitant ainsi la formation de polarons à des tensions moins négatives. Les simulations révèlent que plusieurs polarons peuvent s'aligner en chaînes et sauter entre atomes voisins, augmentant fortement la conductivité de surface. Des expériences suivant les signaux magnétiques et le transfert de charge confirment que le TiO2 déficient accumule davantage de ces poches de charge et transporte les électrons plus aisément que le TiO2 pur. En conséquence, les électrodes présentant des lacunes en oxygène pilotent la réaction d'évolution de l'hydrogène à des surtensions beaucoup plus faibles et avec des courants bien plus élevés.
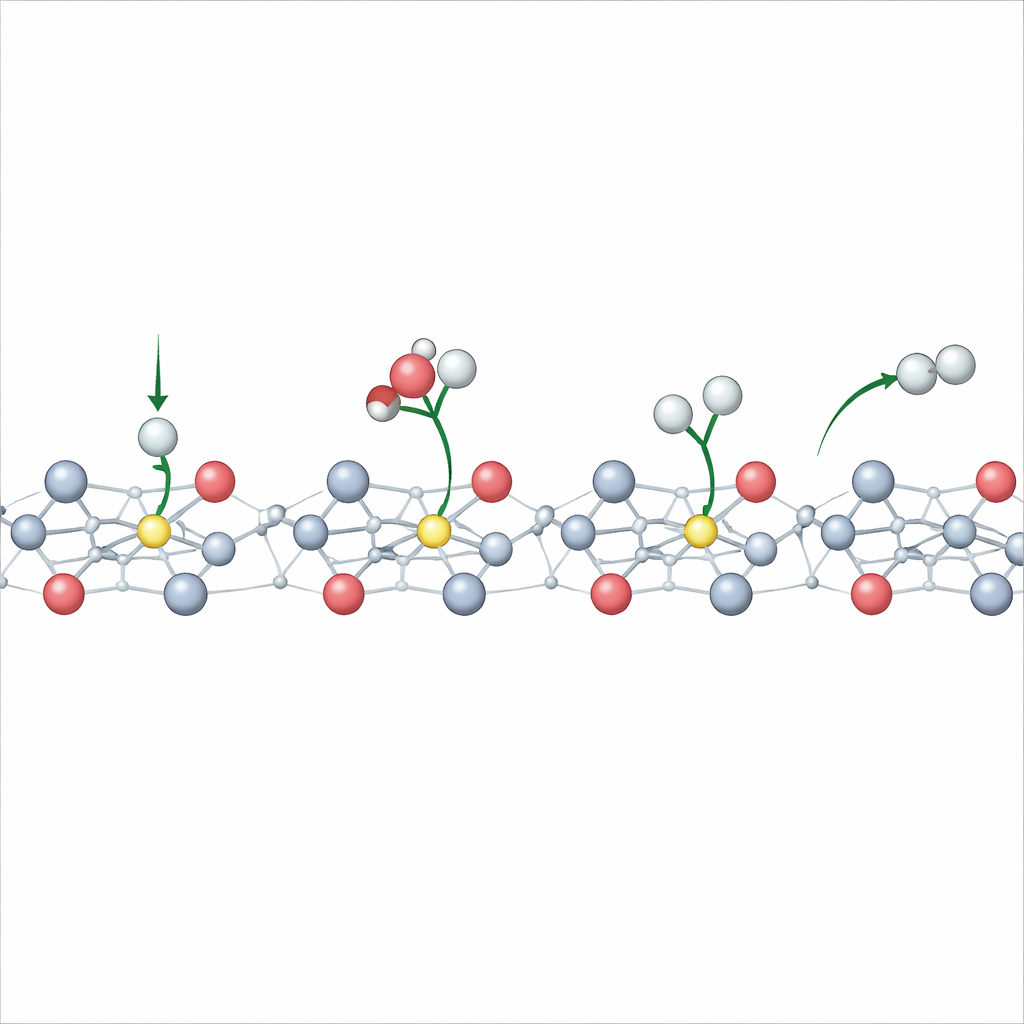
Repenser les règles simples pour les énergies de réaction
Sur les électrodes métalliques, les chimistes s'appuient souvent sur des règles linéaires élégantes qui relient les énergies de réaction, les barrières d'activation et le potentiel appliqué. Les auteurs montrent que ces règles commencent à se dégrader sur le TiO2 dès que les polarons interviennent. L'énergie d'adsorption de l'hydrogène sur la surface ne varie plus de manière lisse avec le potentiel ; elle présente plutôt des coudes et des déformations lorsque de nouveaux états de polarons s'activent. Fait surprenant, même si ce lien simple tension–énergie échoue, une relation plus générale liant les barrières de réaction aux énergies de réaction reste valable. Cela signifie que, en tenant compte soigneusement du moment et du lieu d'apparition des polarons, on peut encore prédire la vitesse de formation de l'hydrogène sur ces surfaces semi-conductrices.
Concevoir des catalyseurs plus intelligents et réglables
Pris ensemble, les résultats dressent le portrait du TiO2 comme d'un catalyseur dont la performance n'est pas uniquement déterminée par sa composition, mais peut être activement ajustée par le potentiel d'exploitation. En combinant des défauts intrinsèques tels que les lacunes en oxygène avec la formation de polarons contrôlée par tension, la surface peut se transformer en un réseau dense de sites hautement actifs et conducteurs pour l'évolution de l'hydrogène. Pour un lecteur non spécialiste, le message principal est que des matériaux semi-conducteurs peu coûteux peuvent rivaliser avec les métaux nobles en apprenant à « activer » et diriger ces petites poches de charge pendant le fonctionnement, ouvrant de nouvelles voies vers une production d'hydrogène efficace et évolutive et d'autres technologies électrochimiques propres.
Citation: Wu, T., Guo, X., Zhang, G. et al. Potential-dependent polaron formation activates TiO2 for the hydrogen evolution reaction. Nat Commun 17, 2104 (2026). https://doi.org/10.1038/s41467-026-68892-5
Mots-clés: réaction d'évolution de l'hydrogène, dioxide de titane, polarons, électrocatalyse des semi-conducteurs, vacances d'oxygène