Clear Sky Science · fr
Inhibition de la signalisation TGF-β dans les microglies stimule la neurogenèse adulte hippocampique et réduit les comportements anxieux chez la souris adulte
Pourquoi les cellules immunitaires du cerveau comptent pour l’humeur et la mémoire
La plupart d’entre nous considèrent les cellules immunitaires comme patrouillant le corps, pas comme façonnant nos pensées et nos émotions. Cette étude remet en question cette vision en montrant que les microglies — cellules immunitaires résidant dans le cerveau — peuvent influencer puissamment la naissance de nouveaux neurones dans l’hippocampe, une région importante pour la mémoire et les émotions. En désactivant une voie de signalisation spécifique dans les microglies chez des souris adultes, les chercheurs ont augmenté la production et la survie de nouveaux neurones et observé des changements mesurables dans les comportements de type anxieux.
La nurserie tranquille du cerveau pour les nouveaux neurones
Chez les mammifères adultes, de nouveaux neurones naissent encore dans quelques « nurseries » spécialisées. L’une des plus importantes est la zone sous-granulaire de l’hippocampe, qui aide à distinguer des souvenirs similaires, soutient l’apprentissage et contribue à la régulation de l’humeur. Dans des conditions normales, beaucoup de ces cellules nouvellement nées meurent avant d’atteindre la maturité. Leur nombre peut augmenter ou diminuer en réponse à l’exercice, à un environnement enrichi, au stress, à un AVC ou à l’épilepsie. Les microglies surveillent constamment cet environnement, mais il restait incertain si leur état réactif, « inflammatoire », aide ou nuit à cette neurogenèse adulte.
Désactiver un frein clé dans les microglies
L’équipe s’est intéressée à une molécule de signalisation appelée TGF-bêta, qui maintient habituellement les microglies dans un état calme et homéostatique. À l’aide de souris génétiquement modifiées, ils ont désactivé sélectivement la signalisation TGF-bêta dans les microglies à l’âge adulte — soit en supprimant le ligand TGF-bêta lui-même, soit en retirant les récepteurs (ALK5 ou TβRII) qui le détectent. Cela a poussé les microglies vers un profil réactif, pro-inflammatoire sans provoquer de perte neuronale généralisée. Dans cet état, les microglies ont augmenté en nombre et changé de morphologie, signe d’activation, tandis que les cellules gliales voisines appelées astrocytes restaient en grande partie inchangées.
Plus de nouveaux neurones, meilleure survie et anxiété modifiée
Lorsque la signalisation TGF-bêta a été interrompue dans les microglies, la nurserie hippocampique a produit une poussée de neurones immatures marqués par la protéine DCX. Ce pic est apparu environ trois semaines après l’interruption génétique et a conduit à une augmentation durable de neurones pleinement matures quelques semaines plus tard. Le suivi précis des cellules en division a montré que l’effet principal était une meilleure survie des nouveaux neurones, et non une simple accélération de la division cellulaire. L’élimination complète des microglies par un médicament n’a pas reproduit cet effet, ce qui suggère que ce n’est pas l’absence des microglies qui compte, mais le profil réactif spécifique créé lorsque la voie TGF-bêta est silencieuse. Au plan comportemental, les souris dont les microglies étaient déficientes en TGF-bêta passaient plus de temps dans les bras ouverts de labyrinthes surélevés, signe courant d’une réduction de l’anxiété ou d’une désinhibition. Ces changements ont disparu lorsque les microglies sont redevenues plus normales dans certains modèles, mais ont persisté dans d’autres où les microglies sont restées réactives.
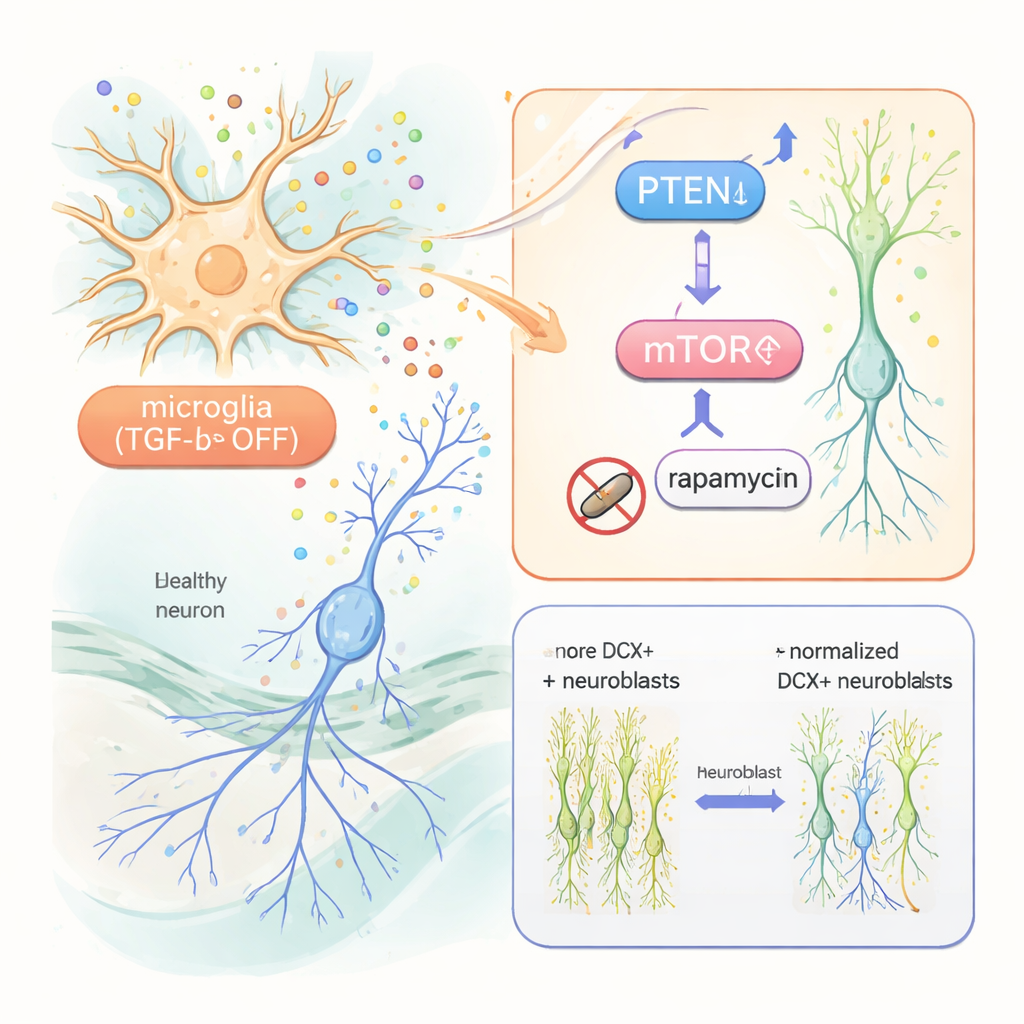
Découvrir la voie à l’intérieur des nouveaux neurones
Pour comprendre comment les microglies altérées communiquent avec les nouveaux neurones, les chercheurs ont utilisé le séquençage ARN unicellulaire sur des cellules hippocampiques. Ils ont trouvé de larges modifications de l’activité génique non seulement chez les microglies mais aussi chez les neurones immatures. Parmi les changements clés figure une réduction de PTEN, une protéine qui limite normalement la croissance cellulaire, et des indices d’une activité accrue de la voie mTOR, qui favorise la survie et la croissance cellulaires. Fait intéressant, des facteurs de croissance bien connus comme IGF‑1 et TNF‑alpha, bien qu’élevés dans les microglies réactives, se sont révélés non nécessaires : même lorsqu’ils étaient éliminés génétiquement, l’augmentation de la neurogenèse persistait. En revanche, lorsque l’équipe a traité les souris avec du rapamycine, un médicament qui bloque mTOR, l’excès de neurones immatures et leur ramification exubérante est revenu à la normale. Les nouveaux neurones présentaient également des niveaux accrus d’un marqueur mTOR en aval, que la rapamycine réduisait.
Ce que cela pourrait signifier pour la santé cérébrale
Pris ensemble, ces résultats suggèrent que lorsque la signalisation TGF-bêta dans les microglies est désactivée, ces cellules adoptent un état réactif qui favorise la survie et l’intégration des nouveaux neurones hippocampiques via une voie PTEN–mTOR à l’intérieur de ces neurones. Cela est, à son tour, associé à une diminution des comportements de type anxieux chez la souris, bien que cela puisse aussi s’accompagner de modifications de l’apprentissage et de la mémoire. Pour un non-spécialiste, le message clé est que les cellules immunitaires du cerveau peuvent ajuster finement le nombre de nouveaux neurones qui rejoignent nos circuits mnésiques — et que manipuler prudemment ce système pourrait un jour aider à stimuler une neurogenèse bénéfique ou à contenir des neurones excessivement ramifiés dans des conditions comme l’épilepsie ou après une lésion cérébrale.
Citation: Ware, K., Peter, J., Yazell, J. et al. Inhibition of TGF-β signaling in microglia stimulates hippocampal adult neurogenesis and reduces anxiety-like behavior in adult mice. Nat Commun 17, 1440 (2026). https://doi.org/10.1038/s41467-026-68885-4
Mots-clés: neurogenèse adulte, microglies, hippocampe, comportement anxieux, signalisation TGF-bêta