Clear Sky Science · fr
Adaptation post-traductionnelle médiée par PRMT3 en réponse au jeûne régule la flexibilité métabolique
Pourquoi le moment des repas et le carburant corporel comptent
Beaucoup de personnes essaient le jeûne ou l’alimentation à temps restreint pour perdre du poids ou améliorer la glycémie, mais les résultats peuvent être aléatoires. Cette étude examine en profondeur notre métabolisme pour comprendre pourquoi. En se concentrant sur la graisse abdominale chez la souris et sur des échantillons humains, les chercheurs mettent au jour un interrupteur moléculaire qui aide le tissu adipeux à décider s’il doit brûler ou stocker du carburant, et montrent comment le moment des repas et un médicament peuvent orienter cet interrupteur vers une meilleure santé.
Un moteur flexible à l’intérieur de notre graisse
Notre organisme fonctionne au mieux lorsqu’il peut passer facilement de la combustion des lipides pendant le jeûne à l’utilisation du sucre après les repas. Cette « flexibilité métabolique » se perd souvent dans l’obésité, rendant plus difficile la gestion des variations d’apport et de demande énergétique. L’équipe a étudié la graisse blanche viscérale — la graisse abdominale profonde fortement associée au diabète et aux maladies cardiovasculaires — et a découvert que des marques chimiques spécifiques sur les protéines, appelées groupes méthyle, varient entre l’alimentation et le jeûne. Chez la souris comme chez l’humain, deux de ces marques, MMA et ADMA, s’accumulent dans la graisse viscérale à mesure que le poids corporel et l’indice de masse corporelle augmentent, ce qui suggère qu’elles sont des marqueurs d’un métabolisme ralenti et moins adaptable.
Un signal d’alimentation qui rigidifie le métabolisme
Les chercheurs se sont focalisés sur une enzyme dans les adipocytes nommée PRMT3, qui ajoute ces marques de méthylation. Chez la souris, les niveaux de PRMT3 dans la graisse viscérale augmentent la nuit quand les animaux mangent et diminuent le jour quand ils jeûnent, suivant de près le rythme des MMA et ADMA. Ce rythme dépend de l’insuline et d’une protéine de signalisation clé, AKT : lorsque la nourriture ou l’insuline injectée active AKT, PRMT3 est activée et davantage modifiée, ce qui augmente à son tour la quantité de protéines méthylées. Bloquer AKT ou inhiber directement PRMT3 aplatit rapidement ce signal de méthylation, mimant même l’effet d’un jeûne beaucoup plus long.
Reprogrammer les adipocytes du stockage à la combustion
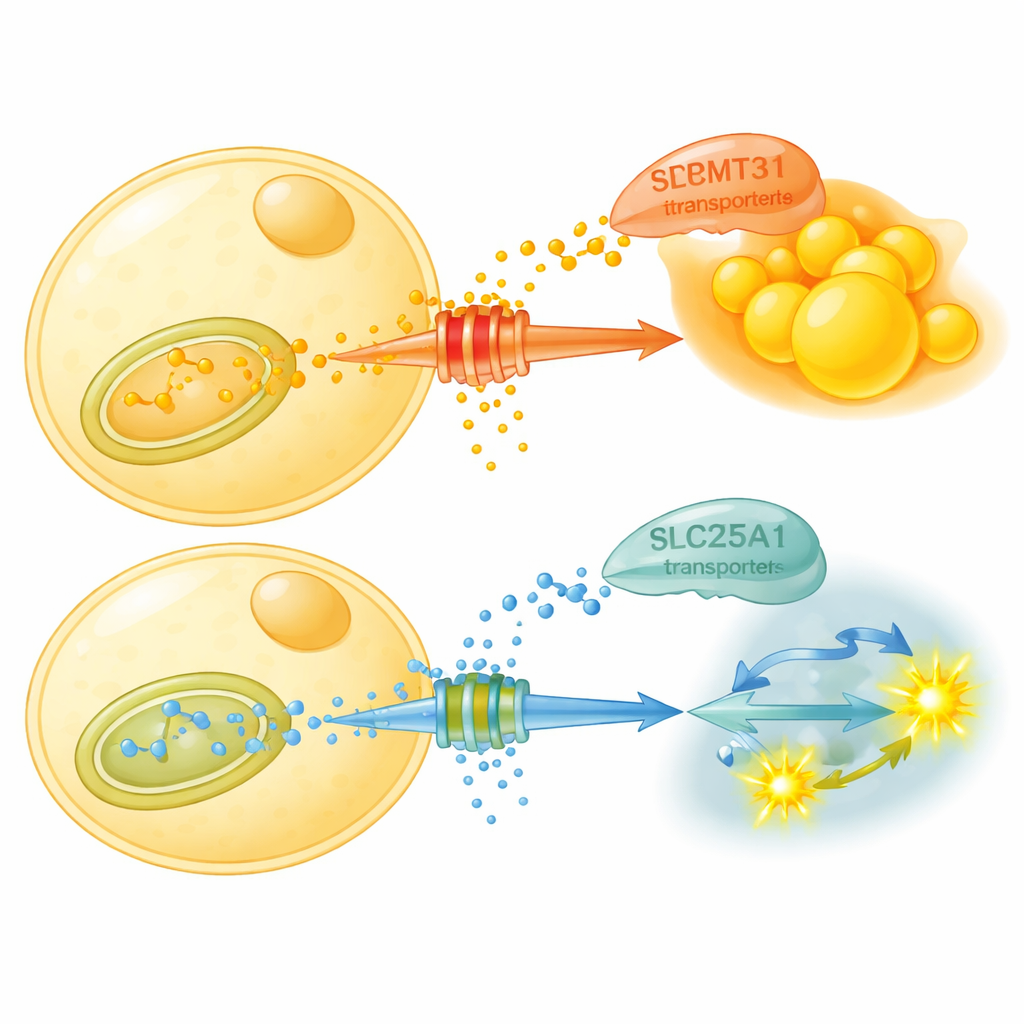
Que fait concrètement ce marquage chimique ? L’étude montre que PRMT3 stabilise un transporteur situé dans les mitochondries, appelé SLC25A1 — les usines énergétiques de la cellule. SLC25A1 exporte le citrate, un intermédiaire métabolique clé, hors des mitochondries vers le cytosol où il alimente la néosynthèse des lipides. PRMT3 méthyle deux sites arginine spécifiques sur SLC25A1, rendant le transporteur plus stable et favorisant l’export de citrate et la construction de graisse. Lorsque PRMT3 est bloqué, les niveaux de SLC25A1 chutent, l’export de citrate diminue et les adipocytes basculent vers la dégradation du glucose plutôt que la synthèse lipidique. Chez des souris nourries avec un régime riche en graisses, un médicament bloquant PRMT3 réduit la masse grasse, améliore le contrôle de la glycémie et augmente une mesure appelée quotient respiratoire, montrant que les animaux passent plus facilement à la combustion des glucides.
Les horaires de jeûne et les modifications génétiques pointent vers la même voie
Les chercheurs ont ensuite vérifié si des schémas de jeûne courants utilisaient ce même interrupteur. Sous un régime d’alimentation à temps restreint 16:8 — 16 heures de jeûne et 8 heures d’alimentation — les souris ont perdu du poids et mieux géré le glucose sans manger moins au total. Leur graisse viscérale présentait des niveaux plus faibles de PRMT3, de SLC25A1 et de protéines méthylées, et leur utilisation des carburants est devenue plus flexible, surtout la nuit quand elles mangent habituellement. De manière remarquable, administrer le médicament inhibiteur de PRMT3 à des moments précis de la journée produisait de nombreux bénéfices identiques au régime 16:8. La suppression génétique de SLC25A1 uniquement dans les cellules adipeuses protégeait aussi les souris de l’hyperglycémie et de la stéatose induites par le régime, encore une fois en augmentant la dégradation du sucre et l’utilisation d’énergie dans la graisse, même sans réduction de la masse grasse.
Ce que cela signifie pour les thérapeutiques futures
Pris ensemble, ces résultats suggèrent que la graisse abdominale profonde contient un interrupteur sensible au temps, contrôlé par l’insuline, AKT, PRMT3 et SLC25A1, qui détermine si notre organisme reste métaboliquement agile ou se verrouille dans un mode de stockage. L’alimentation à temps restreint semble orienter cet interrupteur vers la flexibilité en diminuant PRMT3 et ses effets en aval. Un médicament inhibant PRMT3 peut reproduire nombre de ces avantages chez des souris obèses, laissant entrevoir un traitement futur rendant plus accessibles les bénéfices métaboliques du jeûne. Pour le lecteur quotidien, le message est que le moment où nous mangeons, pas seulement ce que nous mangeons, peut remodeler la façon dont notre tissu adipeux gère le carburant — avec des conséquences importantes pour le poids, la glycémie et la santé à long terme.
Citation: Huang, Z., Liu, X., Chen, X. et al. PRMT3-mediated post-translational adaptation to fasting regulates metabolic flexibility. Nat Commun 17, 2264 (2026). https://doi.org/10.1038/s41467-026-68883-6
Mots-clés: flexibilité métabolique, alimentation à temps restreint, graisse viscérale, méthylation des protéines, métabolisme du glucose