Clear Sky Science · fr
Un nanodispositif à base d’ADN détecte la signalisation purinergique et déclenche un commutateur immunitaire pour résoudre l’inflammation
Atténuer le système d’alarme du corps
Lorsque nos tissus sont blessés, les cellules libèrent une rafale de « signaux d’alarme » chimiques qui attirent les cellules immunitaires pour combattre l’infection et éliminer les débris. Cette réponse est vitale, mais si l’alarme sonne trop fort ou trop longtemps, elle peut provoquer une inflammation dommageable dans les poumons, les reins et d’autres organes. Cette étude décrit un minuscule dispositif programmable à base d’ADN capable de détecter quand la signalisation d’alarme est excessive et de la réduire discrètement, aidant ainsi le système immunitaire à passer du mode d’attaque au mode réparation.
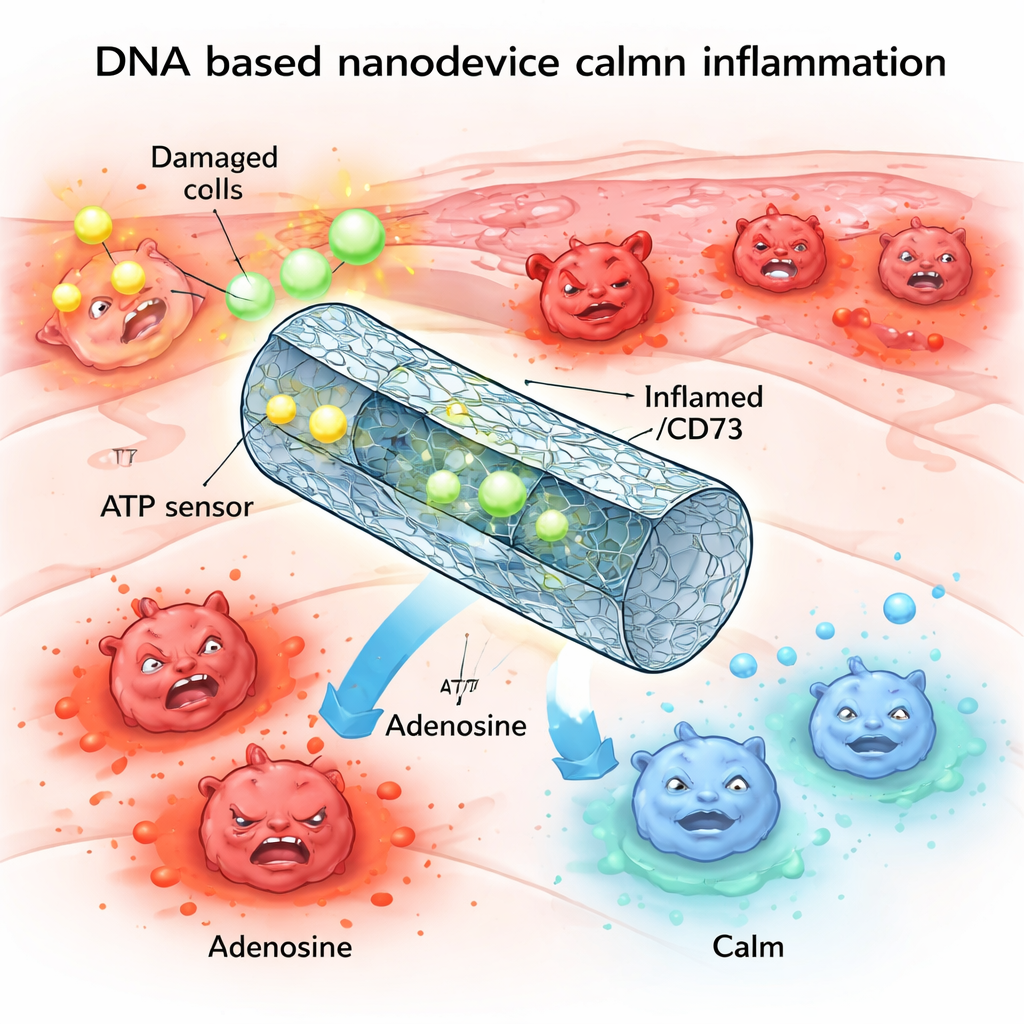
Une alarme chimique qui peut dégénérer
Un des principaux messagers d’alarme du corps est l’ATP, surtout connu comme « monnaie énergétique » à l’intérieur des cellules. Lors d’une lésion ou d’un stress, de grandes quantités d’ATP s’échappent des cellules endommagées dans l’espace extracellulaire. Là, cet ATP extracellulaire agit comme un signal de détresse, se liant aux récepteurs des cellules immunitaires et les poussant vers un état fortement inflammatoire. Dans des conditions saines, des enzymes présentes à la surface des cellules dégradent rapidement l’excès d’ATP en adénosine, une molécule apparentée qui a un effet calmant et anti-inflammatoire. Mais dans de nombreuses maladies inflammatoires chroniques ou sévères, ce système de dégradation est perturbé, laissant des niveaux élevés d’ATP, peu d’adénosine, et des tissus coincés dans un cycle de dommages.
Construire un tube d’ADN intelligent
Les chercheurs ont cherché à imiter et réparer ce système de contrôle naturel en utilisant la nanotechnologie de l’ADN. Ils ont construit un tube creux en ADN, plié à la manière d’une origami, et l’ont équipé de deux composants principaux : des « capteurs » qui reconnaissent l’ATP, et des enzymes qui convertissent l’ATP en adénosine. À l’état de repos, fermé, le tube est maintenu verrouillé par de courts segments d’ADN qui font aussi office de capteurs d’ATP. Lorsque les niveaux d’ATP dépassent un certain seuil typique des tissus blessés, l’ATP se lie à ces segments, provoquant l’ouverture du tube et l’exposition des enzymes ENPP1 et CD73 à l’intérieur. Celles-ci dégradent alors l’excès d’ATP et produisent de l’adénosine, déplaçant en douceur l’équilibre chimique local du danger vers la résolution.
Montrer que le commutateur fonctionne
Dans des tests de laboratoire contrôlés, l’équipe a confirmé que leur tube d’ADN reste fermé à de faibles concentrations d’ATP mais s’ouvre de façon fiable lorsque l’ATP devient abondant, à la manière d’une soupape d’urgence. Une fois déverrouillé, le dispositif convertit progressivement l’ATP en produits intermédiaires puis en adénosine, sans altérer de façon notable l’activité des enzymes. Dans des cellules immunitaires exposées à de fortes quantités d’ATP, ce nanodispositif a réduit les sous-produits toxiques dans les mitochondries, diminué l’activation de voies inflammatoires telles que NF-κB et l’inflammasome NLRP3, et renforcé les signaux associés aux effets apaisants de l’adénosine. Autrement dit, le dispositif n’a pas seulement éliminé l’ATP ; il a activement reprogrammé le comportement des cellules, passant d’un état inflammatoire à un état régulateur.
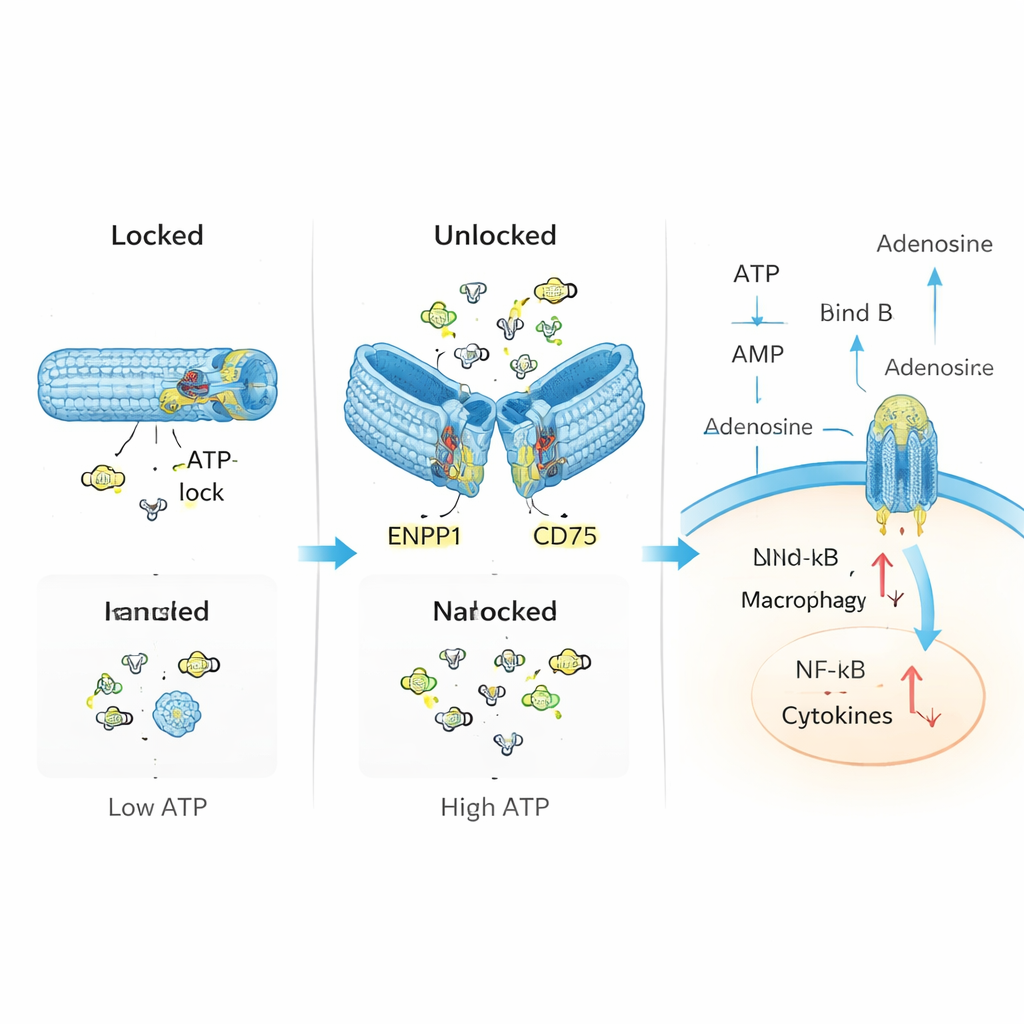
Se rendre sur les sites de blessure
Concevoir un commutateur intelligent est une chose ; l’acheminer au bon endroit dans l’organisme en est une autre. Pour résoudre ce problème de distribution, les chercheurs ont fixé leurs tubes d’ADN à la surface de monocytes circulants, un type de globule blanc qui se rend naturellement aux tissus enflammés. À l’aide d’une ancre d’ADN liée au cholestérol, ils ont « garé » un grand nombre de nanodispositifs sur la membrane de chaque cellule, où les dispositifs sont restés majoritairement en surface plutôt que d’être internalisés. Dans des modèles murins de lésions pulmonaires et rénales aiguës, ces monocytes décorés se sont accumulés dans les organes endommagés bien plus efficacement que les dispositifs en suspension, et les nanodispositifs ont continué de répondre spécifiquement aux niveaux élevés d’ATP dans les tissus lésés.
Aider les tissus à guérir
Chez des souris présentant des lésions pulmonaires ou rénales induites chimiquement, le traitement par le dispositif à base d’ADN a réduit les dommages tissulaires, l’accumulation de cellules immunitaires et les médiateurs inflammatoires. La version portée par les monocytes a donné les meilleurs résultats, offrant une protection plus forte que le dispositif libre ou que les enzymes seules. Des analyses génétiques et métaboliques approfondies du tissu pulmonaire ont montré que cette approche atténuait non seulement les gènes inflammatoires mais contribuait aussi à rétablir le métabolisme énergétique perturbé des cellules. Fait important, les dispositifs ont montré une faible toxicité et n’ont pas déclenché de réactions immunitaires nocives chez les animaux sains.
Pourquoi c’est important pour les thérapies futures
Pour un non-spécialiste, l’idée principale est que ce travail démontre un « thermostat » moléculaire programmable pour l’inflammation. Construit à partir d’ADN et d’enzymes naturelles, le nanodispositif détecte quand un signal de danger est trop fort et le convertit automatiquement en un signal apaisant, aidant les cellules immunitaires à se calmer et les tissus à se réparer. Bien qu’encore à un stade expérimental précoce, cette stratégie suggère une nouvelle classe de traitements qui ne se contentent pas de bloquer les voies immunitaires partout, mais qui rééquilibrent localement les signaux chimiques sur les sites de lésion, offrant potentiellement un contrôle précis de l’inflammation nocive dans de nombreuses maladies.
Citation: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
Mots-clés: nanodispositif en ADN, ATP extracellulaire, inflammation, signalisation par adénosine, nanomédecine