Clear Sky Science · fr
Caractérisation des conditions de traitement qui biaisent artificiellement les transcriptomes des tissus cérébraux humains
Pourquoi la manipulation du cerveau après la mort compte
Beaucoup des découvertes les plus importantes sur la maladie d’Alzheimer, la maladie de Parkinson et d’autres troubles cérébraux proviennent de l’étude de tissus cérébraux donnés après le décès. Mais la manière dont ces tissus sont traités dans les heures qui suivent la mort peut modifier subtilement, et parfois de façon spectaculaire, les gènes qui semblent actifs. Cette étude pose une question apparemment simple mais aux grandes conséquences : lorsque nous lisons les « messages » moléculaires dans les tissus cérébraux d’autopsie, dans quelle mesure ce que nous observons reflète la biologie de la personne, et dans quelle mesure est-ce un effet secondaire du temps et de la température après la mort ?
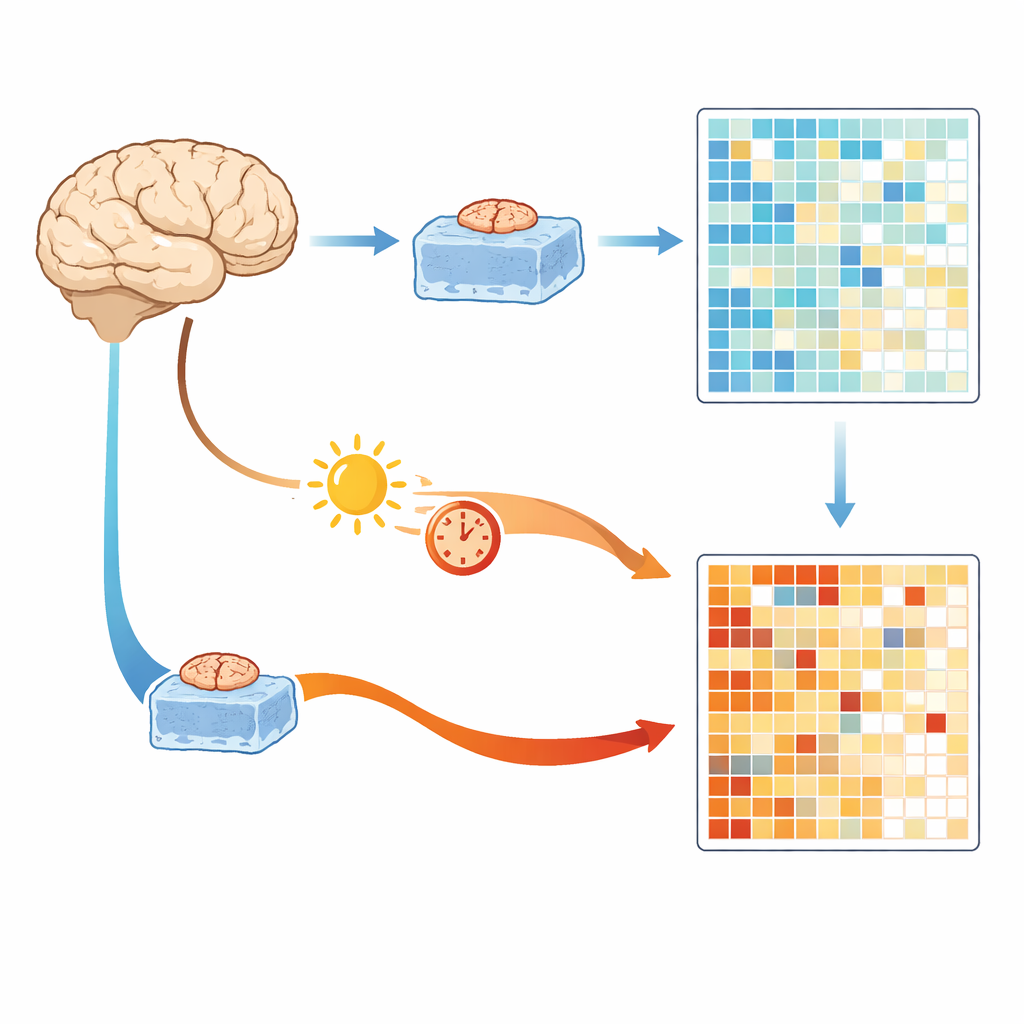
Comparer des tissus chirurgicaux rapidement congelés et des cerveaux d’autopsie
Les chercheurs ont commencé avec un avantage rare : l’accès à de petits fragments de tissu cérébral à l’aspect sain prélevés lors d’interventions chirurgicales pour tumeurs, qui peuvent être refroidis et congelés en environ une demi-heure. Ces échantillons offrent un instantané proche de l’activité génique du cerveau vivant. L’équipe les a comparés à des tissus provenant de grandes banques d’autopsie collectés après un délai court d’environ six heures ou un délai long d’environ 36 heures. Tous les échantillons ont été traités et séquencés de la même manière afin d’éviter des différences techniques. Sur des milliers de gènes, le principal facteur qui a séparé les échantillons n’était ni l’âge ni le sexe du donneur, mais le fait que le tissu provienne d’échantillons chirurgicaux rapidement congelés ou d’échantillons d’autopsie conservés avec retard.
Signaux de stress cachés et émergence de gènes artefacts
Tant les tissus d’autopsie à délai court qu’à délai long montraient de fortes modifications d’activité génique comparés aux tissus congelés immédiatement après la chirurgie. Beaucoup des gènes augmentés étaient liés aux réponses au stress, à la production d’énergie mitochondriale et aux voies inflammatoires. Les auteurs désignent ce groupe partagé de gènes par « Brain Artifact Genes », ou BAGs, car ils semblent être activés par les conditions post-mortem plutôt que par la maladie elle-même. Même un délai relativement court de six heures suffisait à produire des milliers de changements, y compris des gènes impliqués dans la communication entre neurones, ce qui suggère que certains « signaux de maladie » apparents dans des études antérieures reflètent en partie la durée pendant laquelle le cerveau est resté avant d’être préservé.
Tester les rôles du temps, de la température et du type cellulaire
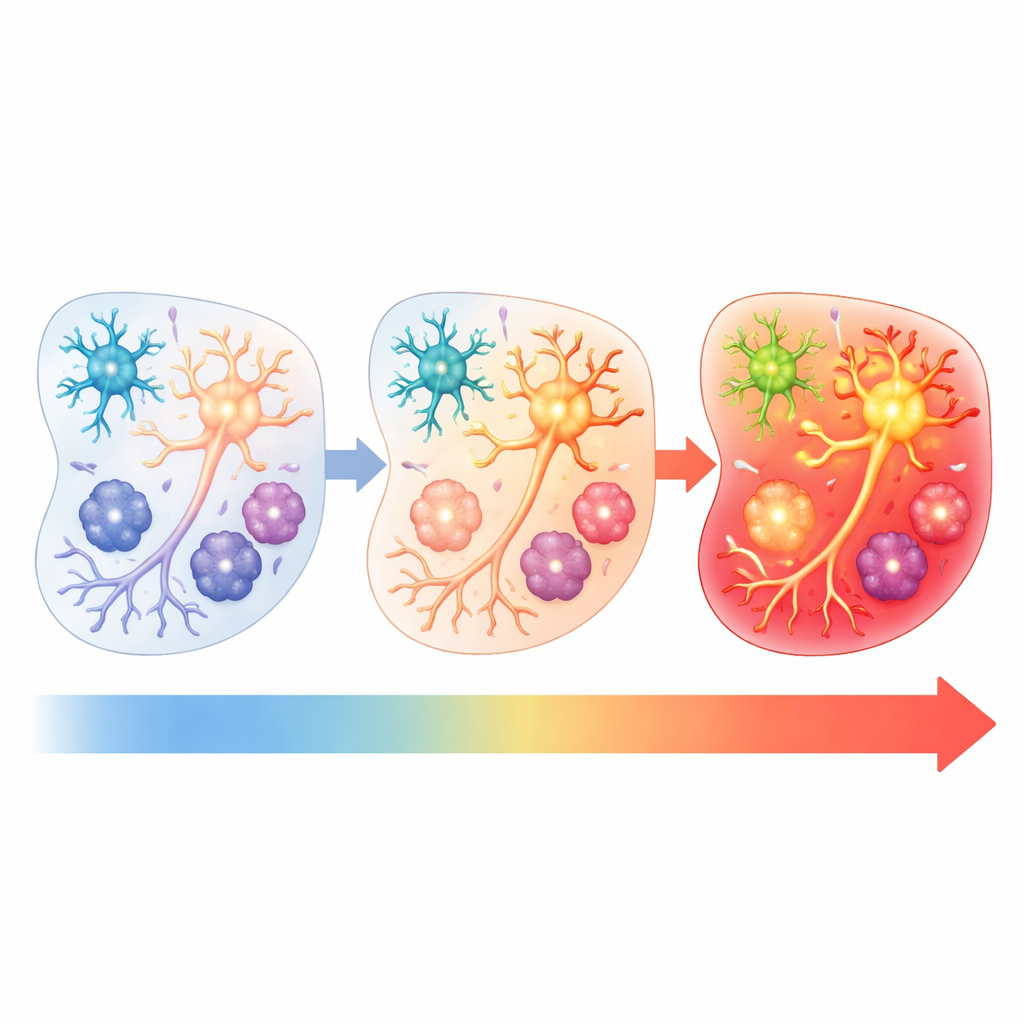
Pour démêler quels facteurs post-mortem importaient le plus, l’équipe a pris des fragments du tissu d’origine chirurgicale et les a délibérément conservés soit à la température du réfrigérateur soit à la température ambiante pendant différentes durées avant congélation. Ils ont ensuite mesuré à nouveau l’activité génique. Les tissus brièvement gardés au réfrigérateur ressemblaient davantage aux échantillons congelés immédiatement, tandis que des temps plus longs et des températures plus chaudes provoquaient une activation BAG plus forte et plus étendue. En analysant des noyaux cellulaires individuels, les chercheurs ont également constaté que différents types cellulaires du cerveau répondaient à des stades différents : les neurones glutamatergiques étaient les premiers « répondeurs » après plusieurs heures à température ambiante, tandis que les oligodendrocytes et les microglies présentaient les signatures d’artefact les plus marquées après environ un jour. Cela signifie que les mesures de populations cellulaires spécifiques peuvent être biaisées de manière dépendante du temps.
Construire un score moléculaire de qualité avec l’apprentissage automatique
Parce qu’aucune biobanque cérébrale ne peut contrôler parfaitement tous les détails de la manipulation post-mortem, les auteurs se sont tournés vers l’apprentissage automatique pour créer un outil pratique de contrôle de qualité. En utilisant des motifs d’activité génique issus de tissus exposés à des combinaisons connues de temps et de température, ils ont entraîné un modèle à reconnaître trois grandes « domaines » de conditions de traitement. À partir de milliers de gènes, le modèle a distillé une signature plus petite qu’ils appellent TTRUTH (Time and Temperature Response genes Underlying Transcriptional Heterogeneity). Le score TTRUTH résultant estime à quel point un échantillon cérébral donné porte des artefacts liés au temps et à la température. Lorsqu’on l’applique à plusieurs jeux de données d’autopsies indépendants provenant d’autres études, la plupart des échantillons se situaient dans un domaine cohérent avec une exposition modérée aux artefacts, tandis qu’une minorité montrait des profils plus proches d’une manipulation idéale ou d’un stress sévère, soulignant la variabilité réelle entre donneurs et centres.
Ce que cela signifie pour la recherche cérébrale
Pour les non-spécialistes, le message à retenir est que le tissu cérébral « se souvient » de la manière dont il a été traité après la mort, et ces souvenirs peuvent se faire passer pour des signes de maladie. Ce travail fournit une feuille de route et un outil en ligne accessible qui permet aux chercheurs d’évaluer leurs propres jeux de données pour y déceler des effets de manipulation cachés, de distinguer les signaux biologiques du bruit technique et de mieux regrouper les échantillons pour l’analyse. En fin de compte, en reconnaissant et en corrigeant ces artefacts, les scientifiques peuvent tirer des conclusions plus fiables sur le fonctionnement du cerveau humain en santé et en maladie — et progresser avec davantage de confiance vers de nouveaux traitements.
Citation: Yaqubi, M., Thomas, M., Talbot-Martin, J. et al. Characterising processing conditions that artifactually bias human brain tissue transcriptomes. Nat Commun 17, 2848 (2026). https://doi.org/10.1038/s41467-026-68872-9
Mots-clés: biobanques cérébrales, tissu post-mortem, expression génique, séquençage ARN, apprentissage automatique