Clear Sky Science · fr
Olig2 agit comme une barrière inductible à la conversion in vivo d’astrocytes en neurones
Transformer les cellules de soutien du cerveau en neurones
Le cerveau adulte ne peut remplacer les neurones perdus que dans une mesure limitée, ce qui constitue un obstacle majeur dans des pathologies comme l’accident vasculaire cérébral, la maladie d’Alzheimer et les lésions de la moelle épinière. Une idée prometteuse consiste à convertir directement en nouveaux neurones des « cellules de soutien » voisines appelées astrocytes, au moyen de la thérapie génique. Cette étude pose une question clé : qu’est‑ce qui empêche cette conversion de fonctionner efficacement in vivo — et peut‑on lever ces freins ?
Un frein caché à la métamorphose cellulaire
Les astrocytes nourrissent normalement les neurones, maintiennent la chimie du cerveau et réagissent aux lésions. Dans certains états pathologiques, ils peuvent adopter des comportements proches des cellules souches, laissant espérer qu’on puisse les reprogrammer en neurones sur place. On sait déjà qu’une classe de gènes appelés facteurs de transcription proneuraux — tels que Ngn2, Ascl1 et NeuroD1 — peut pousser les astrocytes vers une identité neuronale. Pourtant, chez l’animal, cette conversion astrocyte‑en‑neurone reste frustrantement peu efficace. Les auteurs ont émis l’hypothèse que, au‑delà de défenses préexistantes, les astrocytes pourraient déclencher une nouvelle barrière inductible lorsque la reprogrammation est activée.
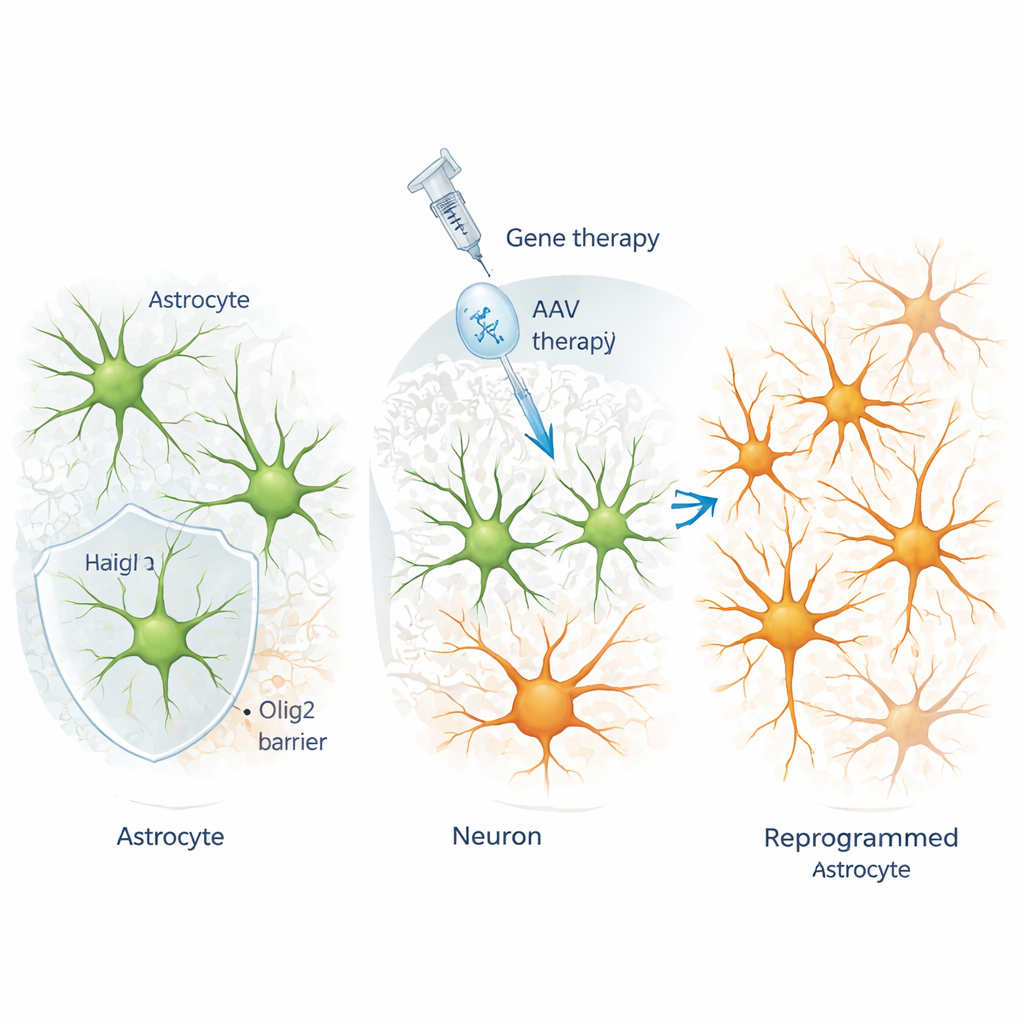
Une protéine appelée Olig2 intervient pour résister au changement
Travaillant dans le cortex de souris adultes, les chercheurs ont délivré des facteurs de reprogrammation aux astrocytes à l’aide de virus ingénierés hautement sélectifs pour ces cellules. Ils ont découvert que chaque fois qu’un facteur bHLH (hélice‑boucle‑hélice) comme Ngn2, Ascl1 ou NeuroD1 était forcé dans les astrocytes, une autre protéine bHLH, Olig2, était fortement activée. Dans des conditions normales, Olig2 se trouve dans la lignée des oligodendrocytes, et non dans les astrocytes corticaux matures. Des expériences de traçage minutieuses ont montré que les cellules additionnelles positives pour Olig2 après traitement n’étaient pas produites par prolifération de précurseurs d’oligodendrocytes — au contraire, ce sont bien les astrocytes ciblés pour la conversion qui activaient Olig2 en réponse au signal de reprogrammation.
Enlever le frein triple la conversion et donne des neurones fonctionnels
Pour tester si Olig2 constitue réellement une barrière, l’équipe a utilisé des ARN à courte épingle (shRNA) pour réduire spécifiquement Olig2 dans des astrocytes auxquels on donnait aussi Ngn2. La suppression d’Olig2 a fait chuter pratiquement à zéro les niveaux protéiques de cette molécule dans ces cellules et a eu un effet saisissant : la proportion d’astrocytes marqués devenus neurones a augmenté d’environ trois fois par rapport à Ngn2 seul. Sur plusieurs semaines, de nombreuses cellules ont traversé un stade intermédiaire, perdant d’abord les marqueurs astrocytaires typiques avant d’acquérir pleinement des marqueurs neuronaux. Des enregistrements électriques sur coupes de cerveau ont montré que les cellules converties émettaient des potentiels d’action et, dans environ la moitié des cas, recevaient des entrées synaptiques excitatrices et inhibitrices — signes d’une intégration fonctionnelle aux circuits locaux.
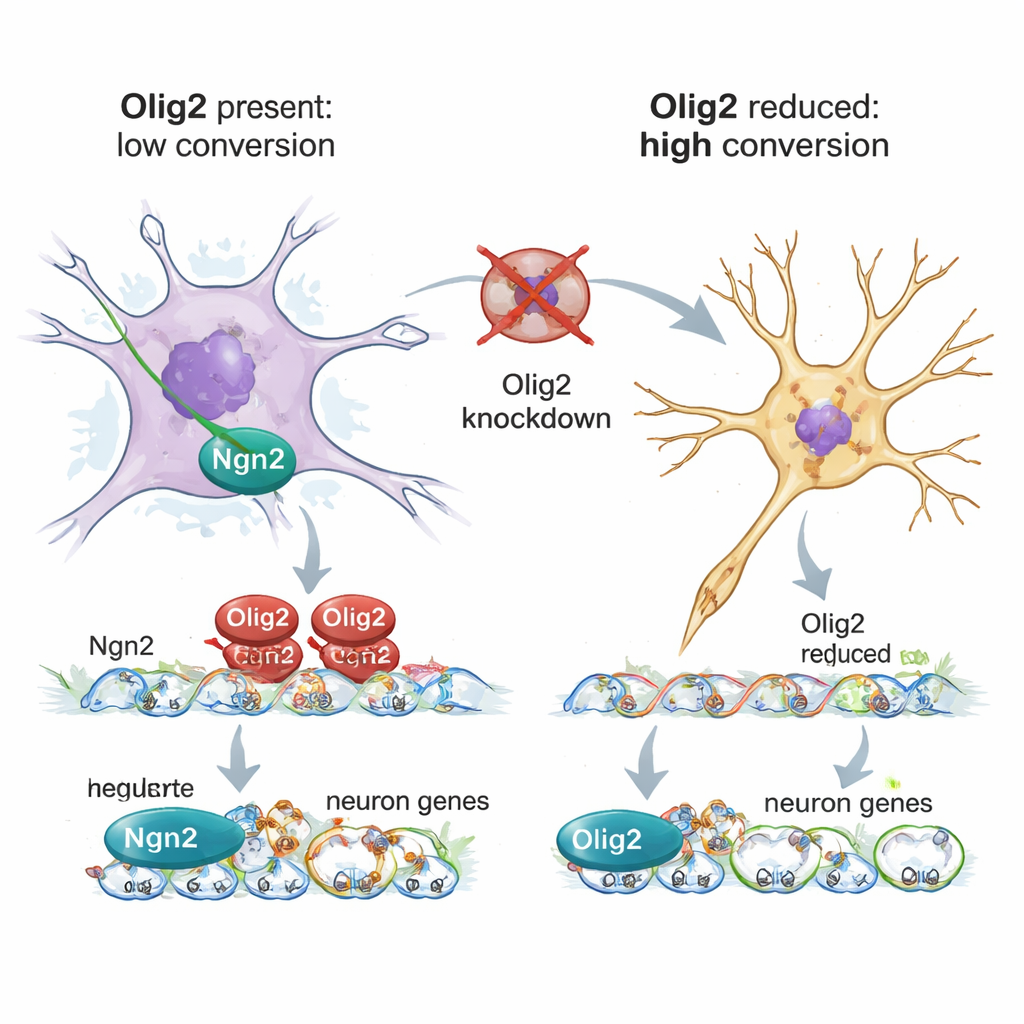
Comment Olig2 bloque le basculement vers un programme neuronal
Grâce au séquençage ARN unicellulaire, les auteurs ont profilé des milliers d’astrocytes individuels exposés à Ngn2, avec ou sans réduction d’Olig2. Lorsque Olig2 était présent, les astrocytes ne changeaient leur expression génique que partiellement : certaines voies métaboliques et de synthèse protéique étaient modifiées, mais les gènes centraux des astrocytes restaient actifs et de nombreux gènes impliqués dans la construction neuronale restaient silencieux. Lorsque Olig2 était réduit, les astrocytes supprimaient plus complètement leur programme de cellules de soutien matures et surexprimaient des gènes associés aux cellules souches neurales, à la neurogénèse et à la croissance axonale. Une méthode complémentaire, CUT&Tag, a cartographié où Olig2 se lie sur l’ADN dans ces astrocytes reprogrammés. Olig2 se positionnait sur des régulateurs de nombreux gènes pro‑neurogénétiques — y compris Ngn2 lui‑même — ce qui concorde avec un rôle de répresseur direct qui à la fois atténue le facteur de reprogrammation et maintient l’inactivation des gènes neuronaux.
Reconfigurer l’identité cellulaire en levant une défense inductible
Dans l’ensemble, ce travail révèle que les astrocytes mettent en place une défense active et inductible contre leur transformation en neurones : une fois qu’un facteur proneural comme Ngn2 est introduit, il déclenche Olig2, lequel restreint à son tour Ngn2 et bloque des gènes neuronaux clés. Désactiver Olig2 ne résout pas tous les problèmes — les rendements de conversion restent modestes — mais cela augmente substantiellement la production de nouveaux neurones fonctionnels et fait basculer le métabolisme et l’expression génique des astrocytes vers un état proche du neurone. Pour le lecteur non spécialiste, la conclusion est que la réparation réussie du cerveau pourrait nécessiter non seulement d’appuyer sur l’accélérateur avec des facteurs pro‑neuronaux, mais aussi de relâcher des freins nouvellement découverts comme Olig2 que les cellules utilisent pour protéger leur identité.
Citation: Lai, C., Hou, K., Li, W. et al. Olig2 acts as an inducible barrier to in vivo astrocyte-to-neuron conversion. Nat Commun 17, 2033 (2026). https://doi.org/10.1038/s41467-026-68869-4
Mots-clés: conversion astrocyte-en-neurone, reprogrammation cellulaire, Olig2, thérapie génique, neurorégénération