Clear Sky Science · fr
Évolution coordonnée des familles de gènes façonne le génome des Mucorales dimorphes
Un champignon, deux formes
Certaines levures peuvent mener une double vie, passant d’une forme unicellulaire « levure » à une forme filamenteuse « moule ». Cette capacité de changement de forme les aide à survivre à des environnements variables et, dans certains cas, à envahir des tissus humains. L’étude résumée ici révèle comment un groupe de ces champignons, les Mucorales, réorganise et utilise son patrimoine génétique pour soutenir les deux modes de vie au sein d’un même génome.
Pourquoi ces champignons « caméléons » importent
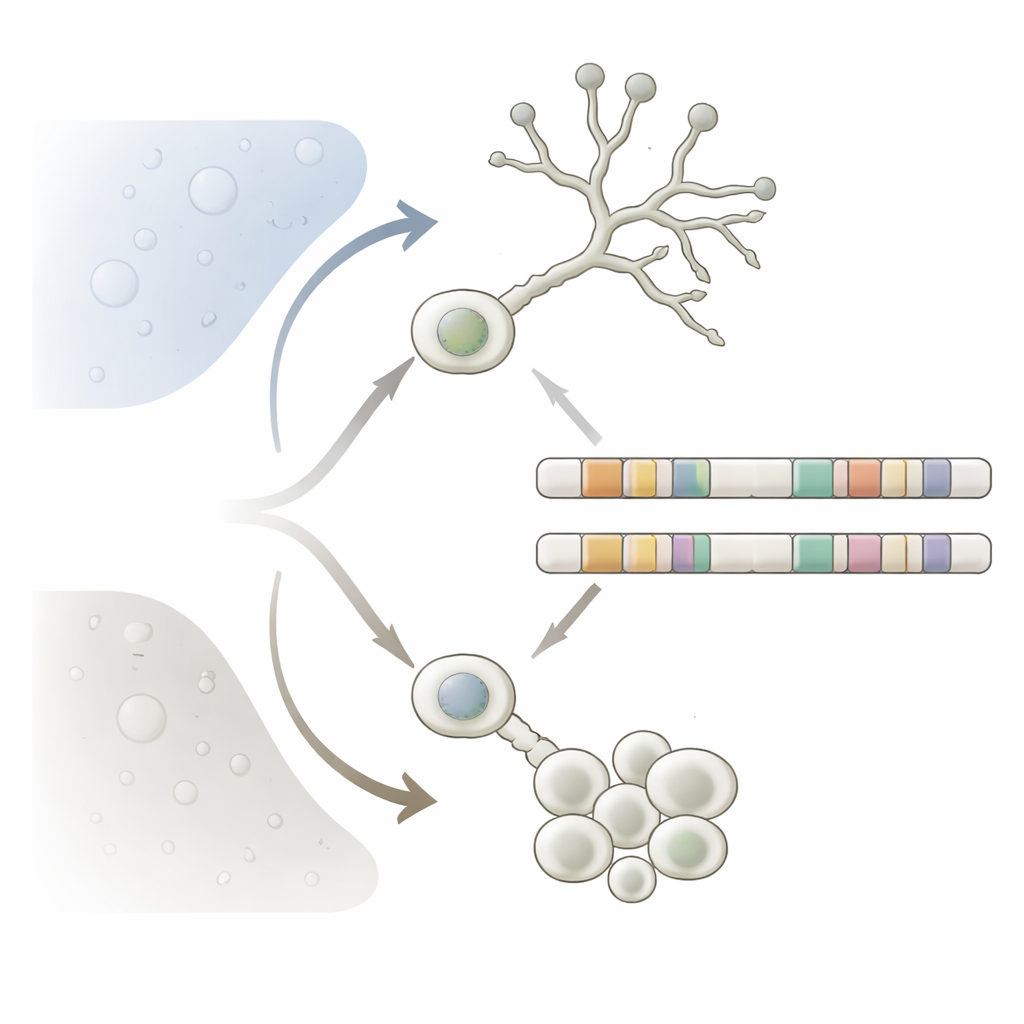
Les champignons dimorphes sont importants non seulement pour l’écologie mais aussi pour la santé humaine. Chez les Mucorales, la forme levure est constituée de cellules rondes isolées qui privilégient les milieux pauvres en oxygène et riches en sucres et croissent par bourgeonnement. La forme mycélienne forme de longs filaments qui prospèrent en présence d’oxygène et peuvent envahir les tissus et les surfaces. Chez plusieurs espèces de Mucorales, seule la forme filamenteuse est fortement infectieuse, provoquant la mucormycose, une maladie sévère chez les personnes immunodéprimées. Comprendre comment ces champignons changent de forme peut expliquer pourquoi ils sont si adaptables, pourquoi ils résistent à certains médicaments, et quelles caractéristiques génétiques distinguent les espèces dimorphes dangereuses de leurs parentes inoffensives.
Un génome conçu pour basculer
Les auteurs se sont concentrés sur le champignon modèle Mucor lusitanicus et l’ont suivi à travers quatre étapes : levure, mycélium précoce, le retour vers la levure, et mycélium mature. En séquençant l’ARN, ils ont mesuré quels gènes sont actifs à chaque état. Ils ont constaté qu’environ 70 % de tous les gènes modifient leur activité pendant la transition morphologique, bien plus que chez de nombreux autres champignons. Les cellules en forme de levure ont tendance à activer des gènes pour le métabolisme de base et la synthèse des éléments constitutifs cellulaires, tandis que les mycéliums favorisent des gènes impliqués dans la signalisation interne et le cytosquelette, qui soutient la croissance filamentaire. Cette large reprogrammation montre que le dimorphisme n’est pas un ajustement mineur mais une reconfiguration à l’échelle de l’organisme.
Gènes dupliqués aux fonctions séparées
Une découverte clé est que de nombreux gènes existent en paires ou en petites familles dont les copies se sont spécialisées pour l’une ou l’autre forme. L’équipe a d’abord revisité un exemple connu : deux gènes de ferroxydase et deux gènes de transporteur du fer qui importent ensemble le fer, un nutriment vital. Un membre de chaque paire est utilisé en forme levure, l’autre en mycélium. L’élimination des copies spécifiques à la levure a entravé la croissance en levure mais laissé la croissance mycélienne globalement intacte, et l’inverse était vrai pour les copies mycéliennes. En étendant cette analyse à l’échelle du génome, les chercheurs ont identifié 490 de ces « familles dimorphes » dans lesquelles au moins une copie est spécifique à la levure et une autre au mycélium. Au total, environ un gène sur neuf du génome appartient à de telles familles, couvrant de nombreux rôles cellulaires. Cela suggère que, plutôt que de compter sur une seule version d’une protéine fonctionnant partout, le champignon a évolué vers des versions jumelles adaptées aux conditions très différentes de la vie liquide et pauvre en oxygène en levure versus la vie solide et riche en oxygène en mycélium.
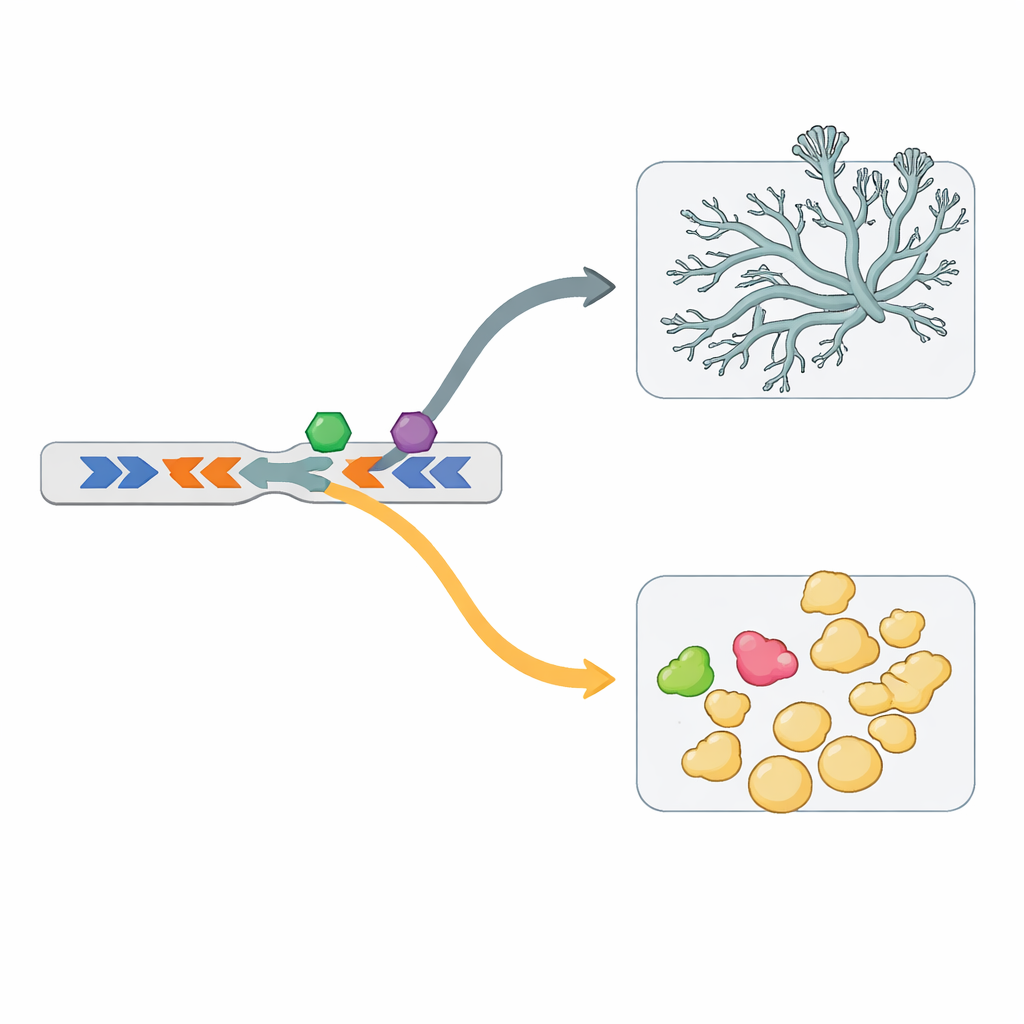
Gènes dos à dos et nouveaux interrupteurs de contrôle
Le génome ne se contente pas de dupliquer des gènes, il les organise aussi en configurations particulières. Beaucoup des gènes d’importation du fer, par exemple, se trouvent en paires « tête-à-tête » : deux gènes placés en directions opposées, partageant une région de contrôle centrale. Une telle paire est active en levure, la paire voisine en mycélium. L’échange expérimental de ces régions de contrôle partagées a inversé le moment d’activation de chaque gène, prouvant que cette organisation agit comme un interrupteur coordonné. Une analyse de l’ensemble du génome a trouvé plus d’un millier de ces paires tête-à-tête, dont des centaines impliquées dans le dimorphisme. Les régions de contrôle partagées pour les paires liées à la levure et au mycélium portent des motifs d’ADN distincts, ce qui implique qu’elles sont lues par des facteurs régulateurs différents.
Régulateurs principaux et indices évolutifs
Pour identifier ces régulateurs, les chercheurs ont utilisé l’ADN des régions de contrôle partagées des gènes d’importation du fer comme appât pour pêcher les protéines qui s’y lient. Ils ont identifié deux protéines auparavant non caractérisées, nommées DFL et DKL, et ont créé des souches mutantes dépourvues de chacune d’elles. Ces mutants présentaient un basculement fortement perturbé : les mutants DKL ne pouvaient plus du tout former de levure, et les deux mutants avaient perdu le modèle normal d’activation génique sur des milliers de gènes liés au dimorphisme. En comparant des espèces apparentées, l’équipe a observé que les Mucorales dimorphes tendent à conserver des familles de gènes dupliquées et spécifiques à une forme, des structures tête-à-tête, et le gène dfl, tandis que des champignons étroitement liés qui ne changent pas de forme manquent souvent de ces traits. Ce schéma suggère que ces caractéristiques génomiques ont évolué de concert comme une boîte à outils pour le dimorphisme et peuvent servir de marqueurs pour prédire quelles espèces sont susceptibles d’être des changeformes.
Implications pour les maladies fongiques
En termes simples, ce travail montre que les Mucorales ont reconstruit leur génome autour du défi de vivre deux vies distinctes. Ils résolvent cela en dupliquant des gènes importants, en adaptant une copie pour la levure et l’autre pour le mycélium, en connectant nombre d’entre eux en unités de contrôle dos-à-dos, et en utilisant des régulateurs dédiés pour coordonner quelle version est utilisée à quel moment. Parce que la forme envahissante et pathogène est souvent le mycélium, et parce que certains des gènes affectés contrôlent l’absorption du fer et la sensibilité aux médicaments, ces découvertes ouvrent la voie à de nouvelles méthodes pour prédire quelles espèces peuvent devenir dangereuses et pour concevoir des traitements qui perturbent leur capacité à changer de forme.
Citation: Tahiri, G., Navarro-Mendoza, M.I., Lax, C. et al. Coordinated gene family evolution shapes the genome of dimorphic Mucorales. Nat Commun 17, 2148 (2026). https://doi.org/10.1038/s41467-026-68866-7
Mots-clés: dimorphisme fongique, Mucorales, duplication de gènes, régulation du génome, pathogénicité fongique