Clear Sky Science · fr
La régulation à la hausse de NKG2D sensibilise les tumeurs à la thérapie combinée anti-PD1 et anti-VEGF et prévient la perte auditive
Pourquoi cette recherche compte pour les personnes ayant une perte auditive
Certaines personnes héritent d’une affection appelée schwannomatose liée à la NF2, qui entraîne la formation de tumeurs bénignes sur les nerfs de l’oreille interne et conduit souvent à une perte auditive progressive et permanente. Les traitements actuels peuvent réduire la taille des tumeurs mais risquent d’endommager l’audition ou de perdre de leur efficacité avec le temps. Cette étude explore une nouvelle combinaison médicamenteuse qui non seulement ralentit la croissance tumorale dans des modèles de laboratoire, mais contribue aussi à protéger l’audition, ouvrant la voie à des options plus douces et plus durables pour les patients.
Comprendre les tumeurs à l’origine du silence
Dans la schwannomatose liée à la NF2, des tumeurs appelées schwannomes vestibulaires se forment sur le nerf de l’équilibre et de l’audition à l’intérieur du crâne. À mesure que ces tumeurs grossissent, elles peuvent endommager les fibres nerveuses délicates qui transmettent les signaux sonores au cerveau et, dans les cas graves, exercer une pression sur le tronc cérébral. La chirurgie et la radiothérapie peuvent sauver des vies et enlever ou contrôler les tumeurs, mais comportent des risques réels : aggravation de l’audition, vertiges et faiblesse du nerf facial. Un médicament appelé bévacizumab, qui bloque un signal de croissance des vaisseaux sanguins (VEGF), est parfois utilisé pour réduire ces tumeurs et améliorer l’audition, mais seulement environ un tiers des patients en bénéficient et l’effet s’estompe souvent. Cela a stimulé la recherche de traitements à la fois plus sûrs et plus durables.
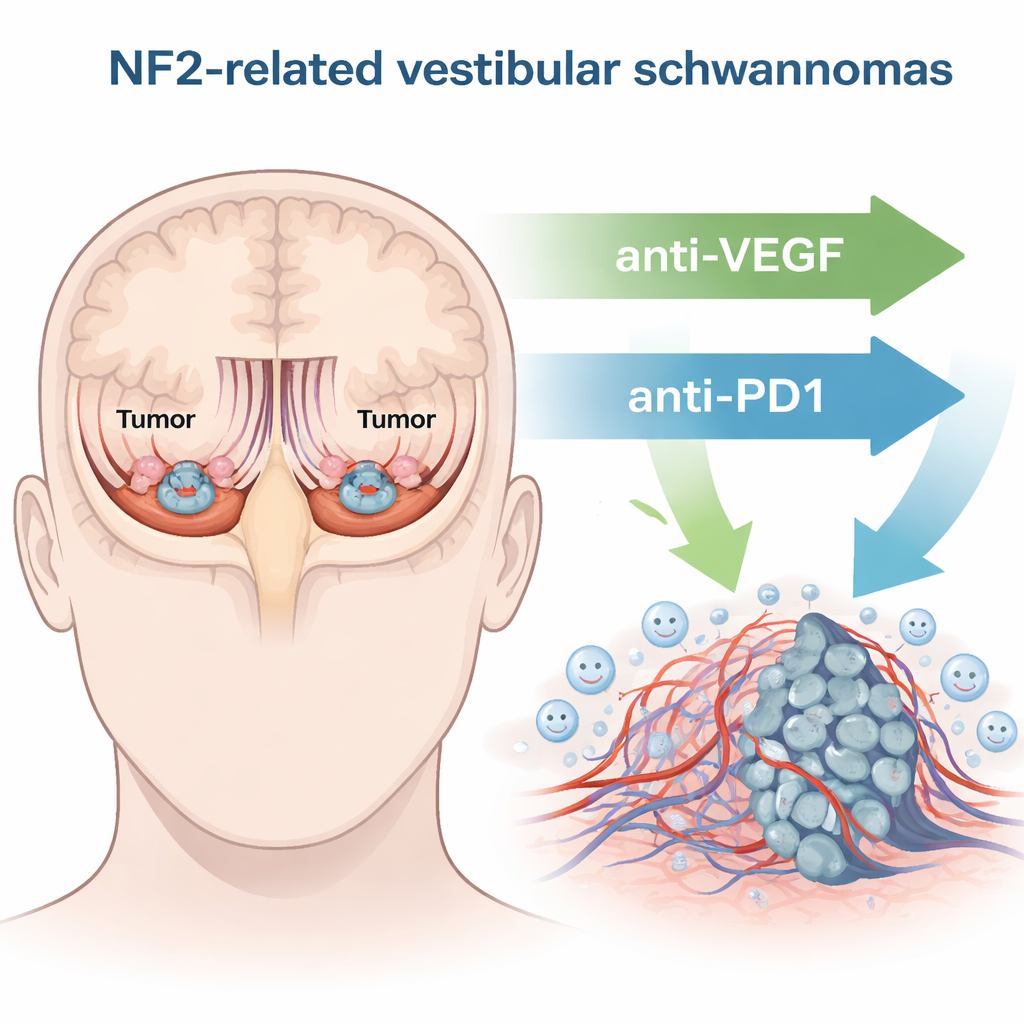
Recruter le système immunitaire comme allié
Au cours de la dernière décennie, la thérapie anticancéreuse a été transformée par les inhibiteurs de points de contrôle immunitaire — des médicaments qui relâchent les « freins » des cellules immunitaires afin qu’elles puissent mieux attaquer les tumeurs. L’un de ces freins, PD-1, se trouve à la surface des cellules immunitaires et peut les inactiver lorsqu’il est engagé. Les auteurs se sont demandé si le blocage de PD-1 (à l’aide d’un anticorps anti-PD1) pouvait aider le système immunitaire à contrôler les schwannomes vestibulaires, et si la combinaison avec une thérapie bloquant le VEGF serait encore plus efficace. En utilisant des modèles murins qui imitent de près les tumeurs humaines de l’oreille interne et des nerfs périphériques, ils ont traité les animaux avec anti-VEGF seul, anti-PD1 seul, ou la combinaison, puis ont suivi la croissance tumorale, la survie et l’audition.
Améliorer le fonctionnement des vaisseaux tumoraux plutôt que de les faire disparaître
L’équipe a constaté que l’anti-VEGF faisait plus que priver les tumeurs de nutriments. Il remodelait leurs vaisseaux sanguins anormaux et fuyants en canaux plus stables et mieux fonctionnels. Au microscope, les tumeurs traitées présentaient davantage de vaisseaux entourés de cellules de soutien et une plus forte proportion de vaisseaux réellement perfusés. Cette « normalisation » a amélioré la distribution de l’anticorps anti-PD1 dans la tumeur et a permis à davantage de cellules immunitaires combattant le cancer — en particulier les lymphocytes T CD8 et les cellules tueuses naturelles (NK) — d’y pénétrer. Chez les souris ayant reçu la thérapie combinée, les tumeurs croissaient plus lentement, comptaient moins de cellules en division et plus de cellules en apoptose, et les animaux vivaient plus longtemps que sous l’un ou l’autre médicament seul.
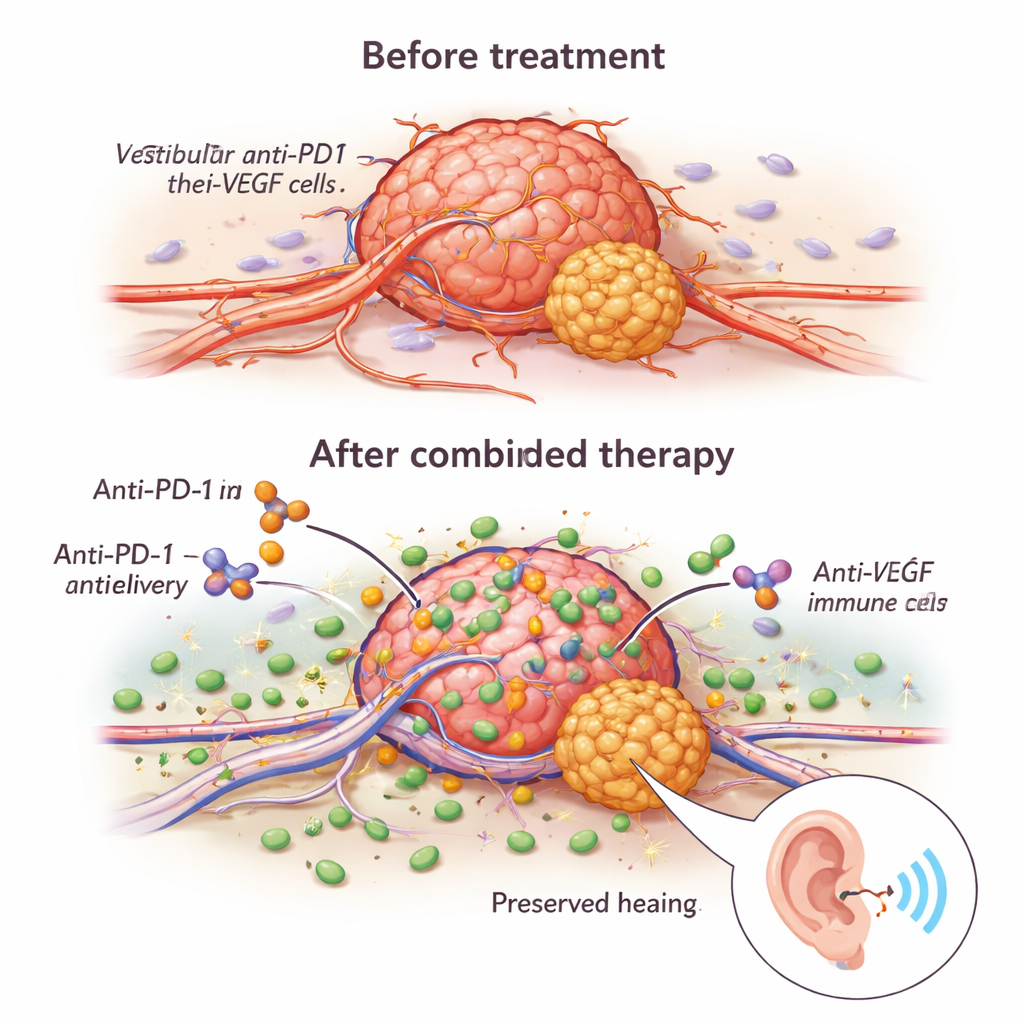
Renforcer le pouvoir de destruction des cellules immunitaires
Les bénéfices de la combinaison ne tenaient pas seulement à l’entrée accrue de cellules immunitaires dans la tumeur ; ces cellules étaient aussi plus agressives une fois sur place. Le traitement anti-VEGF augmentait la présence de molécules telles que la granzyme B et la perforine, qui sont les « munitions » moléculaires du système immunitaire pour perforer les cellules tumorales. Un interrupteur clé de ce processus était un récepteur appelé NKG2D, présent à la fois sur les cellules T et les cellules NK. L’anti-VEGF augmentait NKG2D et ses molécules partenaires sur les cellules tumorales, rendant les cellules immunitaires plus efficaces pour tuer en tests de laboratoire. Lorsque les chercheurs bloquaient NKG2D, les effets antitumoraux des thérapies chutaient fortement, montrant que cette voie est centrale dans la synergie médicamenteuse. De manière importante, de petits échantillons de tumeurs humaines traitées à long terme par bévacizumab présentaient des profils d’expression génique compatibles avec des cellules T et NK plus activées et moins « épuisées », suggérant qu’un renforcement immunitaire similaire pourrait se produire chez les patients.
Protéger l’audition tout en contrôlant les tumeurs
Une question cruciale était de savoir si ces traitements immunitaires nuiraient ou aideraient l’audition. Lorsque des souris saines recevaient uniquement de l’anti-PD1, leurs seuils auditifs restaient normaux, ce qui suggère que le médicament ne cause pas de dommages auditifs à court terme. Chez les souris porteuses de tumeurs, l’anti-VEGF seul améliorait l’audition par rapport à l’absence de traitement, en écho à l’expérience clinique. L’anti-PD1 seul et la combinaison anti-PD1/anti-VEGF rétablissaient tous deux les seuils auditifs à des niveaux proches de la normale. Lorsque les chercheurs ont simulé un scénario réaliste — traiter d’abord les tumeurs par anti-VEGF puis soit poursuivre, arrêter, ou ajouter l’anti-PD1 — ils ont constaté que le passage à l’anti-PD1 pouvait encore ralentir la croissance tumorale, mais l’arrêt de l’anti-VEGF supprimait son bénéfice sur l’audition. Maintenir l’anti-VEGF et ajouter l’anti-PD1 procurait les meilleurs résultats pour la survie et la préservation de l’audition.
Ce que cela pourrait signifier pour les patients
Pour les personnes vivant avec la schwannomatose liée à la NF2, ce travail suggère un avenir où le traitement ferait plus que contenir les tumeurs — il pourrait aussi préserver la capacité d’entendre. Dans des modèles murins soigneusement conçus, la combinaison d’un bloqueur de VEGF et d’un bloqueur de PD-1 a créé un environnement plus favorable aux cellules immunitaires, a amplifié leur pouvoir cytotoxique via NKG2D et a protégé l’audition mieux que chaque approche prise séparément. Bien que des essais cliniques restent nécessaires pour confirmer la sécurité et l’efficacité chez l’humain, l’étude trace une feuille de route claire pour tester cette association médicamenteuse comme stratégie potentiellement plus durable pour gérer les schwannomes vestibulaires et prévenir la perte auditive.
Citation: Lu, S., Yin, Z., Wu, L. et al. NKG2D upregulation sensitizes tumors to combined anti-PD1 and anti-VEGF therapy and prevents hearing loss. Nat Commun 17, 1148 (2026). https://doi.org/10.1038/s41467-026-68865-8
Mots-clés: schwannome vestibulaire, NF2, immunothérapie, bévacizumab, préservation de l'audition