Clear Sky Science · fr
Empilement antiparallèle des pili Csu qui pilote l’assemblage 3D des biofilms d’Acinetobacter baumannii
Comment les germes hospitaliers construisent des cités protégées
Certaines des bactéries les plus tenaces en milieu hospitalier survivent aux antibiotiques en se cachant dans des communautés visqueuses et tridimensionnelles appelées biofilms. Cette étude pose une question simple mais cruciale : comment des bactéries individuelles s’assemblent-elles en structures empilées et si résistantes ? En observant de près avec des microscopes électroniques avancés, les chercheurs ont mis au jour un « Velcro » microscopique constitué de filaments ressemblant à des poils qui permet au pathogène dangereux Acinetobacter baumannii de se tisser en agglomérats protecteurs en 3D. Comprendre cet échafaudage caché pourrait ouvrir de nouvelles voies pour désagréger les biofilms et rendre les traitements existants plus efficaces.
De minuscules poils qui tiennent les bactéries ensemble
A. baumannii, une cause importante d’infections hospitalières difficiles à traiter, est couvert de fins poils de surface appelés pili Csu. Des travaux antérieurs ont montré que ces pili sont essentiels à la formation de biofilms robustes en forme de dôme, mais on ignorait comment ils reliaient effectivement les cellules en une structure 3D. À l’aide de plusieurs techniques de microscopie électronique, les auteurs ont d’abord confirmé qu’en culture liquide les pili se projettent majoritairement séparément depuis chaque bactérie, comme des épines sur une bardane. Dans des colonies denses cultivées en surface, cependant, le tableau change radicalement : de nombreux pili se regroupent étroitement, formant de larges bandes plates qui courent entre les cellules voisines, créant un maillage étendu et d’apparence délicate en trois dimensions. 
Des échelles plates construites à partir de filaments appariés
Pour comprendre comment ces bandes se forment, l’équipe a purifié les pili Csu et observé leur comportement isolé. Sur plusieurs jours à semaines, des filaments simples ont commencé à s’apparier puis à fusionner en « superempilements » multi‑filaments, formant finalement un réseau gélifié qui reproduisait fidèlement les structures observées dans les biofilms réels. La cryo‑microscopie électronique à haute résolution a révélé le dessin sous‑jacent. Chaque pilus n’est pas un tube lisse, mais une tige en zigzag. Lorsque deux tiges sont côte à côte dans des directions opposées, elles se touchent à des points d’angle répétitifs, formant des jonctions latérales stables. De nombreuses paires antiparallèles peuvent ensuite s’aligner en une pile très fine en forme de feuille — essentiellement une petite échelle ou un ruban microscopique qui n’a qu’un filament d’épaisseur mais plusieurs filaments en largeur.
Un plan intégré pour la croissance 3D
Les structures détaillées montrent que cette capacité d’empilement est intégrée dans la géométrie même des pili. Le motif en zigzag se répète sur une très courte distance, créant de nombreux points de contact potentiels le long de chaque filament. Ainsi, une fois que deux pili se rencontrent dans la bonne orientation, une chaîne de jonctions peut se former comme une fermeture éclair, étendant rapidement la feuille. De façon importante, l’orientation des tiges fait que les contacts se forment généralement entre des pili appartenant à des cellules différentes, et non au sein d’une même cellule, ce qui favorise naturellement le lien cellule–cellule. Les empilements restent flexibles et extensibles, permettant au biofilm en croissance d’absorber les contraintes physiques sans se rompre. Les chercheurs ont observé que, lors de la division cellulaire, les nouvelles cellules filles se retrouvent souvent avec leurs pili face à face, ce qui favorise la formation des empilements précisément là où il faut pour lier les cellules en amas 3D. 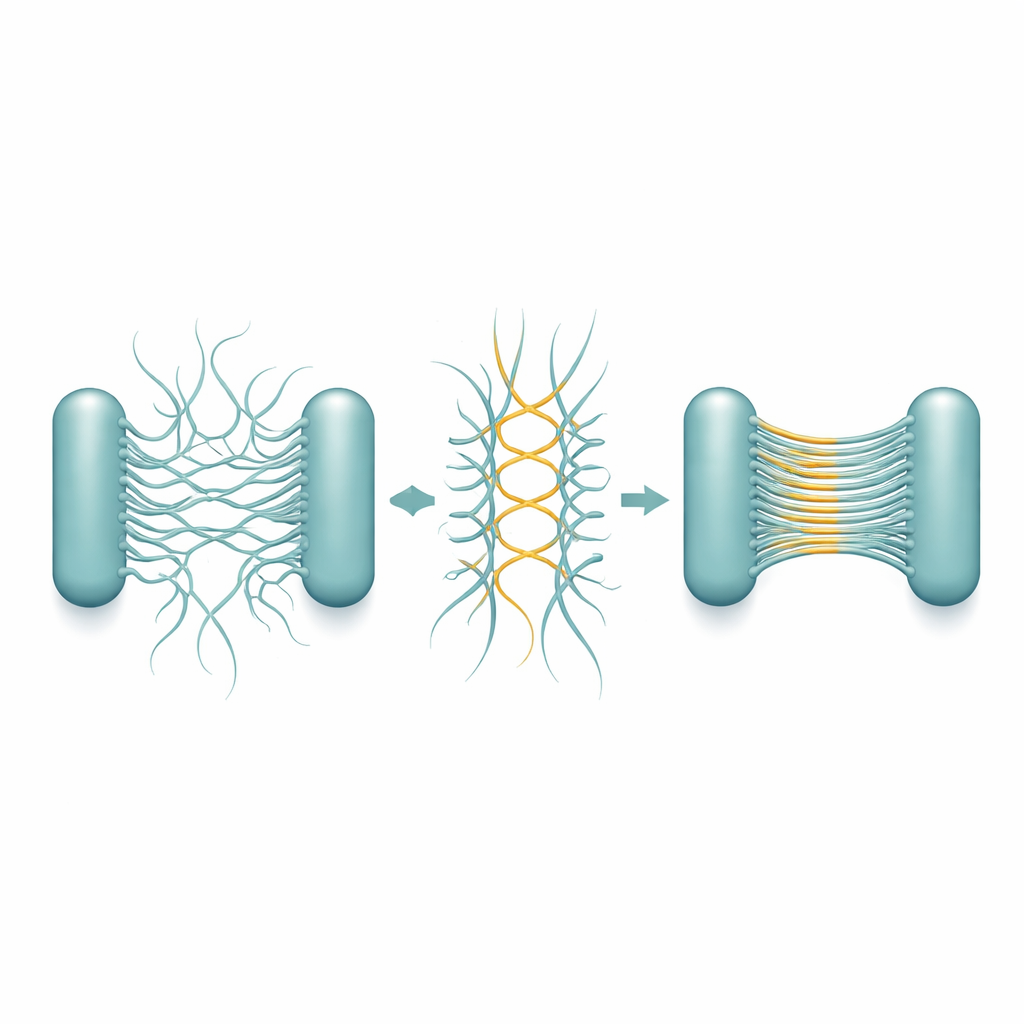
Colle, remplissage et ossature précoce
L’étude a également examiné comment d’autres composants du biofilm contribuent. Un polymère sucré appelé PNAG et de l’ADN libre provenant de cellules lysées s’accumulent dans les biofilms matures. La microscopie a révélé ces substances comblant les étroites interstices entre les bactéries et enroulant les empilements de pili, à la manière du béton coulé autour d’une armature en acier. Pourtant, lorsque l’équipe a retiré le PNAG et l’ADN, les bactéries ont tout de même formé des radeaux organisés maintenus uniquement par les empilements de pili Csu. Cela montre que les pili construisent l’ossature primaire, tandis que la matrice environnante cimente et stabilise ensuite la structure.
De nouveaux points faibles dans les forteresses bactériennes
En termes simples, ce travail explique comment A. baumannii utilise ses poils de surface pour se lacer en amas résistants et multicouches que les médicaments et les cellules immunitaires peinent à pénétrer. Les pili jouent d’abord le rôle d’accroches pour saisir des surfaces, puis de sangles flexibles qui s’empilent en feuilles plates, reliant les cellules voisines dans toutes les directions. Des polymères sucrés et de l’ADN remplissent ensuite les interstices, transformant ce réseau de sangles en une forteresse solide. En identifiant précisément la façon dont les pili adhèrent les uns aux autres, l’étude met en lumière une nouvelle cible : des médicaments ou des molécules qui bloquent les contacts pilus–pilus pourraient affaiblir les échafaudages des biofilms de l’intérieur, facilitant l’élimination des infections bactériennes persistantes.
Citation: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
Mots-clés: biofilms, Acinetobacter baumannii, pili, résistance aux antibiotiques, cryo-microscopie électronique