Clear Sky Science · fr
Dégradation de l’électrode négative induite par le dépôt du zinc en deux étapes et sa récupération dans les batteries au zinc
Pourquoi les batteries au zinc comptent au quotidien
Stocker l’électricité de façon sûre et économique est essentiel, que ce soit pour alimenter des panneaux solaires domestiques en secours ou pour stabiliser le réseau électrique. Les batteries au zinc métal sont des candidates attractives : le zinc est abondant, non toxique et fonctionne dans des électrolytes aqueux bien plus sûrs que les liquides inflammables de nombreuses batteries au lithium. Pourtant, ces batteries prometteuses s’estompent et se court‑circuitent encore trop vite. Cet article révèle un processus de croissance en deux étapes caché sur l’électrode de zinc qui cause ces dommages, et présente une stratégie chimique « d’auto‑réparation » qui permet aux batteries de fonctionner beaucoup plus longtemps.
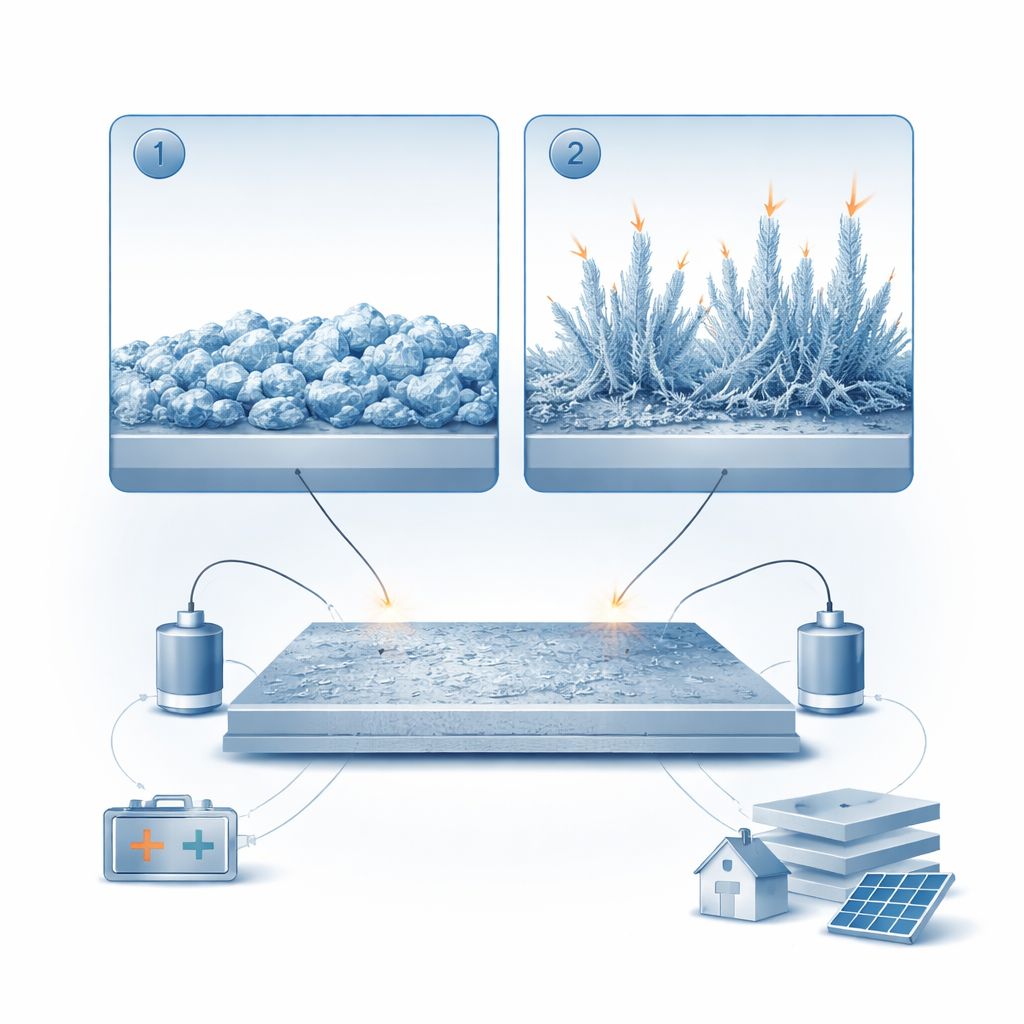
Du métal lisse au « moussage » du zinc
L’électrode négative de ces batteries est constituée de zinc métal, qui se plaque (ajout de zinc) et se dépote (retrait de zinc) à répétition lors des cycles de charge et de décharge. À l’aide d’une cellule transparente équipée d’un microscope, les chercheurs ont observé comment le zinc s’accumule sur une surface métallique au fil du temps. Ils ont découvert que la croissance du zinc n’est pas une seule et même voie, mais deux stades distincts. D’abord, il forme des cristaux relativement denses et bosselés qui créent une couche brillante et compacte. Ensuite, à mesure que le dépôt se poursuit, des structures fines et filamenteuses jaillissent des arêtes et des pointes aiguës. Ce second stade, le zinc « mousseux », comble l’espace entre les électrodes et finit par les relier, risquant des court‑circuits internes.
Comment le zinc mousseux devient du zinc « mort »
L’équipe a combiné imagerie directe, microscopie électronique et simulations informatiques pour comprendre pourquoi cette couche mousseuse apparaît. Les protubérances aiguës des dépôts bosselés concentrent le champ électrique—un effet analogue aux paratonnerres qui concentrent les décharges électriques. Cette concentration attire davantage d’ions zinc vers les pointes, favorisant une croissance rapide en forme de moustaches. Lors du processus inverse, lorsque le zinc est dissous, les filaments mousseux se dissolvent en premier et peuvent perdre le contact électrique avec le métal sous‑jacent. Ce qui reste est du zinc « mort » : de petits morceaux électriquement isolés qui ne participent plus à la réaction de la batterie mais contiennent encore du matériau actif utile, entraînant une perte de capacité et des surfaces rugueuses et instables.
Concevoir un électrolyte plus intelligent
Sachant que la croissance mousseuse provient d’un accroissement local d’ions aux sites saillants, les chercheurs ont conçu un additif d’électrolyte qui s’attaque à la fois à la formation du zinc mousseux et au gaspillage de zinc mort qu’il produit. Ils ont utilisé un sel appelé acétylcholine iodure, qui fournit des cations organiques positifs et des anions iodure au sein de la même molécule. Selon des mesures de masse sensibles et de la spectroscopie infrarouge, les cations s’adsorbent de manière forte et sélective à la surface du zinc, formant une fine couche chargée positivement qui homogénéise le flux d’ions zinc. Cela favorise un dépôt de zinc lisse et plat plutôt qu’une croissance filamenteuse, maintenant la surface compacte et plus résistante à la corrosion et à la formation d’hydrogène gazeux.
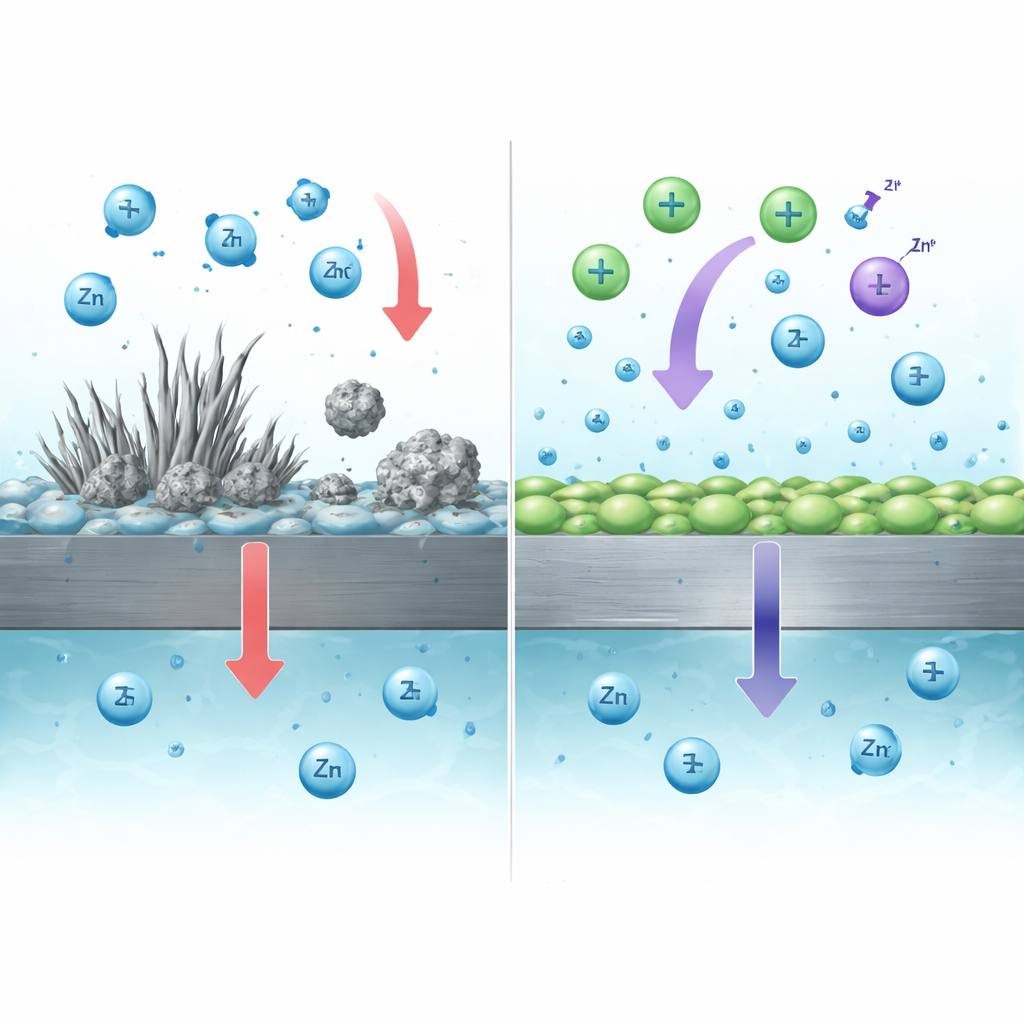
Raviver le zinc perdu pour prolonger la durée de vie
La partie iodure de l’additif joue un rôle différent mais complémentaire. Lors de la charge, l’iodure est partiellement converti en une espèce oxydante douce (I3−) qui peut réagir avec les particules de zinc mort et avec les sous‑produits isolants contenant du zinc qui se forment à la surface. Ces réactions transforment le zinc électriquement isolé en ions zinc dissous, qui peuvent ensuite se replaquer sur l’électrode lors des cycles suivants. Les expériences ont montré que le zinc mort immergé dans une solution contenant de l’iode se dissolvait presque dans la proportion théorique attendue, et que des cellules complètes utilisant l’additif double‑ion récupéraient plus de charge que ce qui serait possible avec le seul zinc fraîchement déposé—preuve claire que du zinc auparavant perdu était « recyclé » à l’intérieur de la batterie.
Que cela signifie pour les batteries réelles
En combinant des cations qui lissent le champ et un anion recyclant le zinc, le nouvel électrolyte a permis d’obtenir des électrodes de zinc avec une efficacité coulombienne moyenne d’environ 99,7 % et un fonctionnement stable pendant plus de 1 400 heures à des courants et des capacités élevés—des conditions pertinentes pour le stockage à l’échelle du réseau. Des cellules zinc symétriques et des cellules pratiques pouch zinc‑iode ont maintenu de faibles pertes de tension et conservé plus de 96 % de leur capacité après des centaines à des dizaines de milliers de cycles, selon le test. Pour un non‑spécialiste, le message clé est que les chercheurs ont identifié précisément comment les électrodes de zinc se dégradent—par une croissance mousseuse en deux étapes qui produit du métal mort—et ont montré une recette chimique qui à la fois empêche cette structure nuisible et ravive le matériau perdu. Cette approche double rapproche fortement les batteries au zinc aqueuses, sûres, d’une utilisation durable et à grande échelle dans les foyers et les réseaux électriques.
Citation: Gan, H., Liu, D., Zhang, Y. et al. Negative electrode degradation induced by two-stage zinc plating and its recovery in zinc batteries. Nat Commun 17, 2067 (2026). https://doi.org/10.1038/s41467-026-68844-z
Mots-clés: batteries au zinc métal, dégradation des électrodes, zinc mousseux, additifs d’électrolyte, stockage d’énergie réseau