Clear Sky Science · fr
Réponses cGAS-IFN-I par extraction d’ADN nucléaire de cellules mourantes via la nucléocytose
Comment notre système immunitaire lit l’ADN des morts
Lorsque nos cellules meurent lors d’infections, de cancers ou de l’usure quotidienne, leurs restes doivent être nettoyés sans provoquer une inflammation excessive. Cet article met au jour un mécanisme surprenant par lequel des cellules immunitaires peuvent en réalité s’introduire dans les noyaux de cellules mourantes, en extraire l’ADN et l’utiliser comme signal de danger. Comprendre ce système caché de nettoyage et d’alerte pourrait modifier notre vision des antiviraux, de l’auto-immunité, des thérapies contre le cancer et des effets secondaires des médicaments.
Une alarme à ADN dissimulée dans les cellules immunitaires
Nos cellules possèdent un capteur nommé cGAS qui détecte l’ADN au mauvais endroit — flottant dans le cytosol plutôt que confiné en toute sécurité dans le noyau ou les mitochondries. Lorsque cGAS rencontre un tel ADN, il déclenche un puissant programme d’alerte qui produit des interférons de type I, protéines essentielles à l’activité antivirale et à la régulation immunitaire. Les chercheurs savaient que les virus peuvent introduire leur matériel génétique dans les cellules pour activer cette voie, et que des fragments d’ADN propre à l’organisme peuvent parfois fuir et provoquer des maladies auto-immunes. Mais une question fondamentale restait : comment de grandes quantités de notre propre ADN, notamment provenant de cellules mortes, atteignent-elles cGAS sans être simplement digérées dans les « estomacs » cellulaires que sont les lysosomes ?
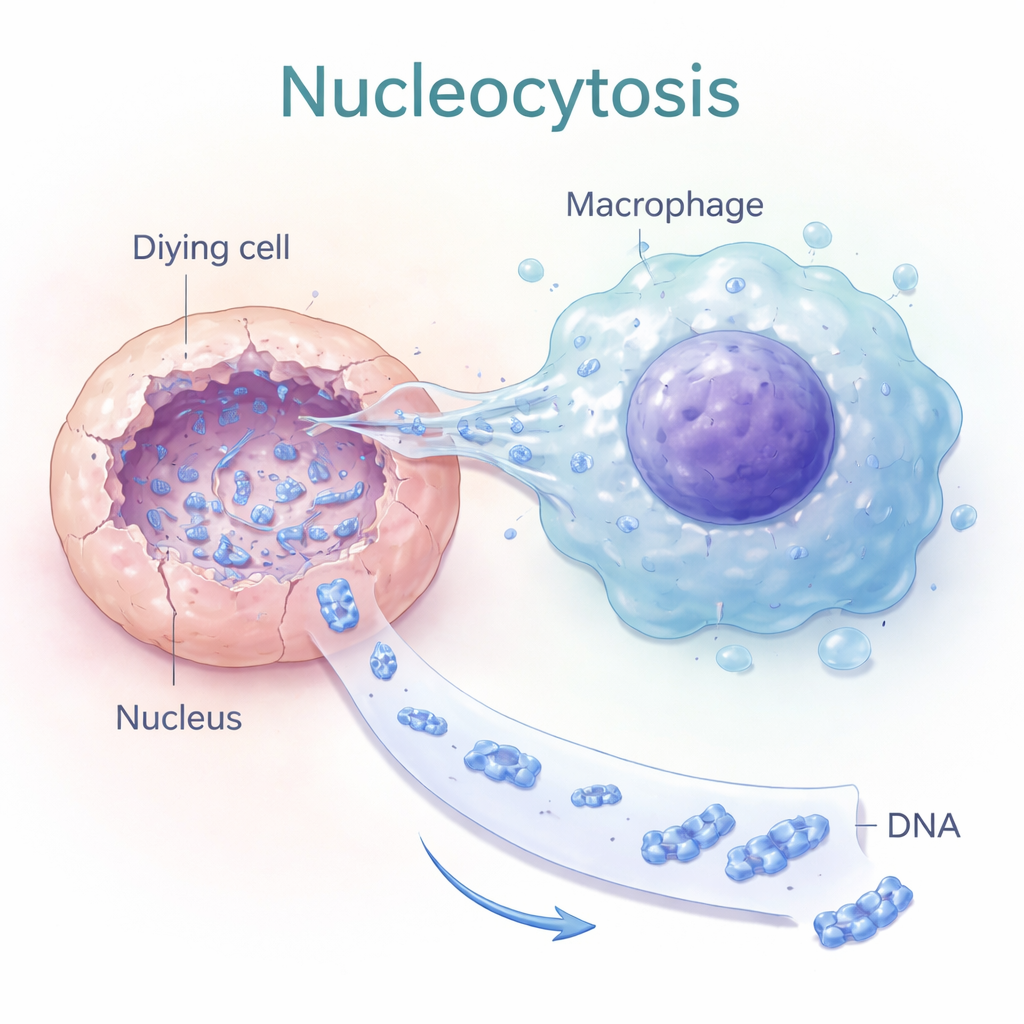
Nucléocytose : percer les noyaux des cellules mortes
Les auteurs ont découvert un processus qu’ils appellent « nucléocytose », dans lequel certains macrophages — cellules immunitaires qui ingèrent habituellement les débris — accomplissent une action beaucoup plus ciblée. Plutôt que d’engloutir une cellule morte entière, ils étendent de fines protrusions en forme de doigts directement dans le noyau de la cellule mourante. L’imagerie de cellules vivantes a montré une diminution de l’intensité d’ADN à l’intérieur du noyau de la cellule morte tandis que l’ADN augmentait dans le macrophage attaché, ce qui indique une extraction active de l’ADN nucléaire. Ce transfert dépendait du cytosquelette (actine) et de molécules de signalisation qui contrôlent la morphologie cellulaire, ce qui suggère que la nucléocytose est un comportement mécanique intentionnel et non une fuite passive.
Quand les antiviraux déclenchent l’alarme à ADN
Pendant la pandémie de COVID-19, des médicaments comme l’hydroxychloroquine ont été largement testés comme antiviraux, mais leurs actions précises dans l’organisme restaient floues. Les chercheurs ont constaté que l’hydroxychloroquine et plusieurs médicaments « amphiphiles cationiques » apparentés peuvent fortement activer la voie cGAS–STING–interféron — mais uniquement dans un sous‑ensemble de macrophages. Ces médicaments perturbent les lysosomes en augmentant leur pH et en bloquant une enzyme appelée PPT1, qui aide à dégrader des étiquettes lipidiques sur les protéines. L’effet combiné pousse certaines cellules vers une forme particulière de mort où la protéine calréticuline s’accumule dans le noyau. Les macrophages étendent alors préférentiellement des protrusions vers ces noyaux riches en calréticuline, extraient l’ADN par nucléocytose et déclenchent une production intense d’interférons dans seulement quelques cellules — suffisante pour générer un signal antiviral local fort sans inonder tout l’organisme.
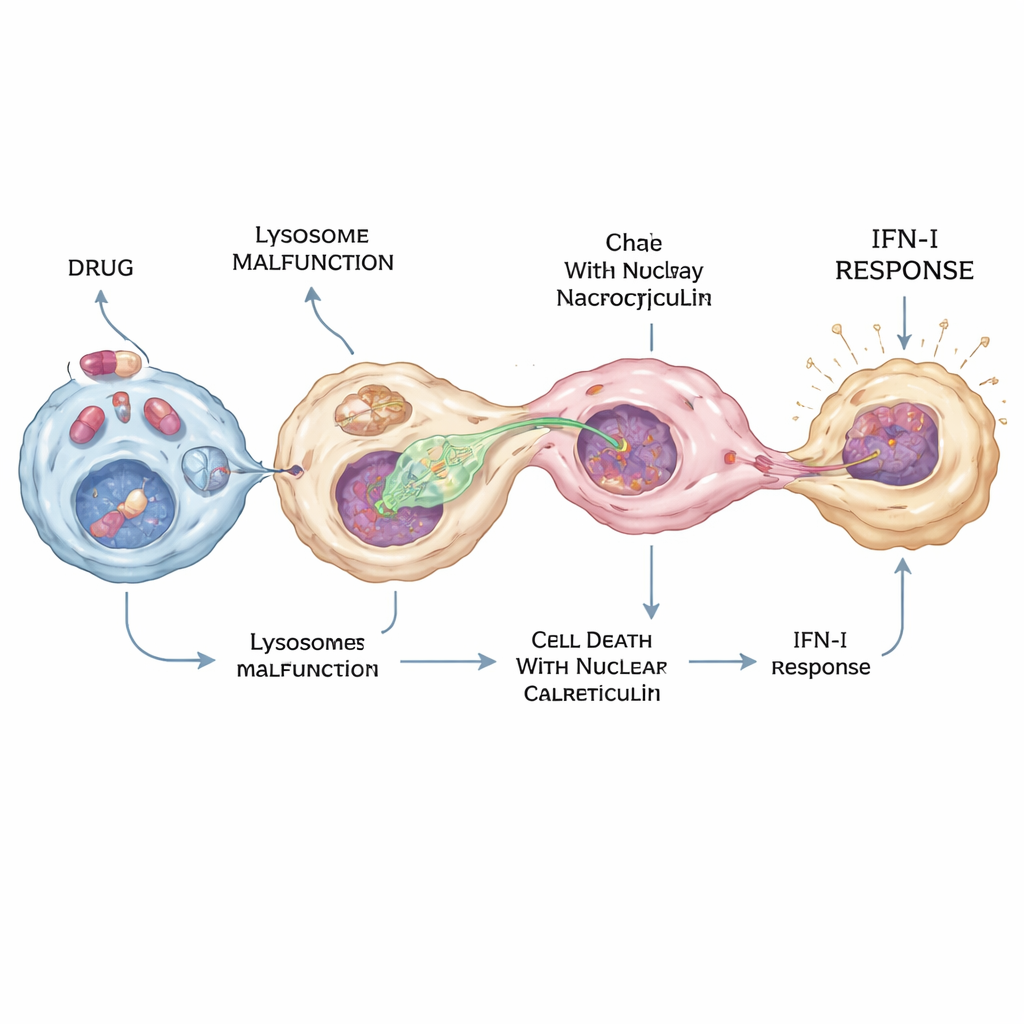
De la défense locale à la maladie et aux effets secondaires
En étudiant à la fois des cultures cellulaires et des poumons de souris, l’équipe a montré que des macrophages traités par ces médicaments peuvent déclencher une réponse aux interférons dépendante de STING qui reste en grande partie locale — par exemple dans le poumon — plutôt que systémique. Cela aide à expliquer pourquoi des médicaments comme l’hydroxychloroquine peuvent présenter des bénéfices antiviraux ou antitumoraux dans certains tissus, mais aussi pourquoi ils peuvent provoquer des effets secondaires spécifiques à des organes, tels que des toxicités oculaires ou cardiaques lors d’un usage prolongé. Le même processus de nucléocytose pourrait plausiblement contribuer à des maladies auto-immunes ou inflammatoires chaque fois que cellules mortes et stress lysosomial coïncident, car il offre une voie directe pour que l’ADN du soi active l’alarme cGAS.
Pourquoi cela importe pour les traitements futurs
Pour un non-spécialiste, le message clé est que les cellules immunitaires ne se contentent pas d’engloutir passivement les cellules mortes ; elles peuvent activement exploiter leurs noyaux pour en extraire l’ADN et l’utiliser comme signal d’alerte. Cette voie de nucléocytose explique comment notre propre ADN peut activer de puissantes défenses antivirales de manière ciblée et locale, tout en soulignant comment des médicaments qui perturbent les lysosomes ou PPT1 peuvent involontairement activer ce mécanisme. En apprenant à réguler la nucléocytose — soit en concevant des antiviraux et des traitements anticancéreux plus intelligents, soit en évitant des signaux indésirables d’ADN du soi dans les maladies auto-immunes — les chercheurs espèrent exploiter ce mécanisme récemment découvert pour des thérapies plus sûres et plus précises.
Citation: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
Mots-clés: nucléocytose, cGAS-STING, hydroxychloroquine, interféron de type I, macrophages