Clear Sky Science · fr
Évolution de la photoredox catalyse au manganèse à basse énergie lumineuse à partir de la photocatalyse par lumière visible haute énergie
Baisser la lumière, garder la chimie
Les chimistes utilisent souvent une lumière vive et haute énergie—comme des lampes bleues intenses ou des UV—pour mener des réactions qui construisent des molécules complexes. Mais cette lumière « dure » peut gaspiller de l'énergie, endommager des parties délicates des molécules et être difficile à utiliser en profondeur dans des tissus ou de grands réacteurs. Cette étude montre comment de simples sels de manganèse peu coûteux peuvent être assemblés directement dans le flacon de réaction pour fonctionner avec une lumière beaucoup plus douce, rouge et proche infrarouge, tout en réalisant une chimie de formation de liaisons puissante, utile pour la découverte de médicaments et la science des matériaux.
Pourquoi une lumière plus douce compte
La lumière haute énergie, c'est un peu comme utiliser un chalumeau pour allumer une bougie : ça marche, mais ça peut aussi brûler tout ce qui l'entoure. Dans les réactions chimiques, cela peut entraîner des sur‑réactions, la destruction de groupes sensibles et un mauvais contrôle. Une lumière plus douce—en particulier le rouge et le proche infrarouge, qui transportent moins d'énergie—pénètre plus profondément dans les liquides et même les tissus biologiques et est généralement plus compatible avec des molécules complexes et fragiles. Le défi est que la plupart des catalyseurs photodirigés existants sont conçus pour absorber une lumière de plus haute énergie, et les repenser exige généralement des synthèses longues et complexes. Les auteurs ont cherché à réduire le « budget photon » de ces réactions sans avoir à reconstruire les catalyseurs depuis zéro.
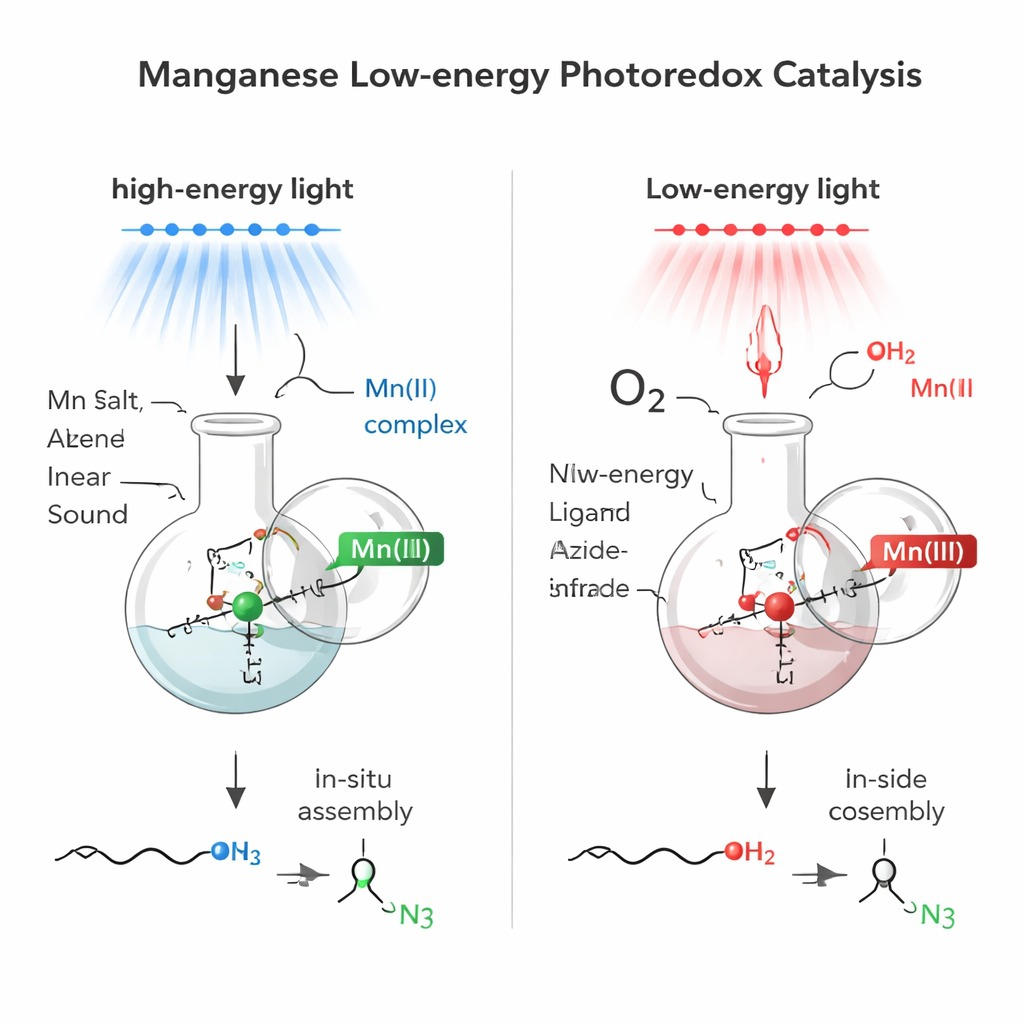
Construire le catalyseur sur place
Au lieu de préparer à l'avance des complexes métalliques élaborés, l'équipe a utilisé une stratégie in situ : ils ont simplement mélangé des sels de manganèse commerciaux avec une petite molécule auxiliaire (un ligand) et une source d'azide directement dans le mélange réactionnel. Cette auto‑assemblage a créé un système absorbant la lumière basé sur le manganèse. Avec un sel de manganèse(II), le mélange absorbait fortement la lumière bleue et pouvait générer des « radicaux azotés » de courte durée à partir d'un réactif courant appelé TMSN3. Ces fragments réactifs s'additionnaient ensuite à travers des doubles liaisons carbone‑carbone simples (alcènes), plaçant un groupe azide (N3) sur l'extrémité la moins substituée de la double liaison—un motif connu sous le nom d'addition anti‑Markovnikov. Fait remarquable, l'eau ordinaire servait de source d'hydrogène, rendant le procédé à la fois simple et atomiquement efficace.
Passer du bleu au rouge profond
Les chercheurs se sont ensuite demandé si un système de manganèse étroitement lié pouvait fonctionner avec une lumière de bien plus basse énergie, dans la région du rouge profond et du proche infrarouge. En passant du manganèse(II) au manganèse(III) et en ajustant finement le milieu réactionnel, ils ont créé un nouveau mélange qui absorbait la lumière jusqu'à environ 850 nanomètres—bien dans le proche infrarouge. Sous cette lumière douce, le complexe de manganèse(III) produisait toujours des radicaux azotés, mais désormais en présence d'air (comme source d'oxygène) et d'un alcool simple, la réaction installait à la fois un groupe azide et un groupe alcool à travers l'alcène en une seule étape. Le résultat est un bêta‑azido‑alcool, un bloc de construction particulièrement utile car il contient deux fonctions très polyvalentes—N3 et OH—sur des atomes de carbone voisins.
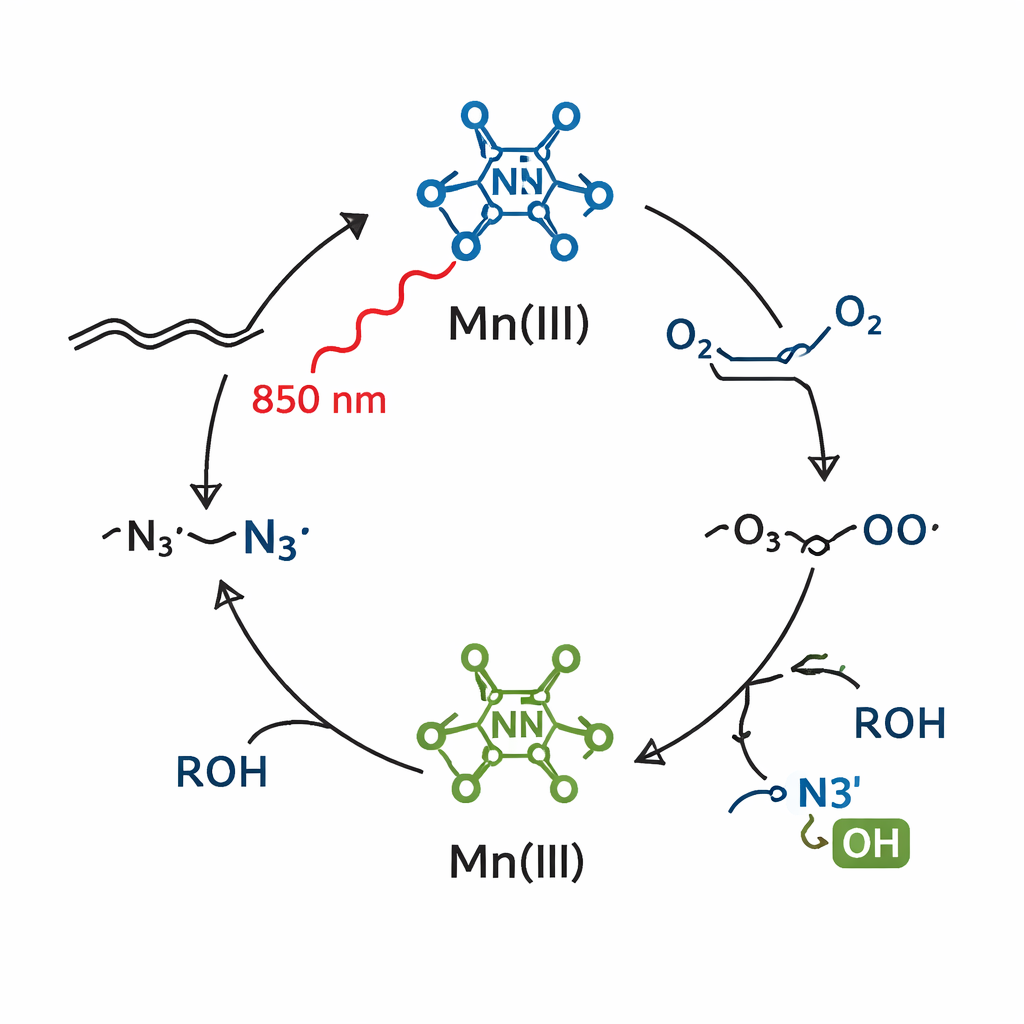
Des alcènes simples à des molécules complexes de type médicament
Avec les systèmes à lumière bleue et à basse énergie en main, l'équipe a testé une grande variété d'alcènes. Ils ont converti de nombreux matériaux de départ différents en azides alkyles ou en bêta‑azido‑alcools avec des rendements modérés à élevés, même lorsque les molécules portaient des groupes qui interfèrent typiquement avec les catalyseurs métalliques, tels que des amines non protégées, des alcools, des groupes contenant du soufre et des systèmes cycliques complexes. Ils ont également démontré la « fonctionnalisation en fin de chaîne » en modifiant des molécules avancées de type médicament, transformant des produits pharmaceutiques existants en nouveaux dérivés auxquels des groupes azide et, dans certains cas, alcool ont été ajoutés. Ces nouvelles fonctions peuvent ensuite être transformées en autres structures riches en azote ou être « cliquées » sur des cibles biologiques, élargissant la boîte à outils de la chimie médicinale.
Une chimie économe en énergie avec un potentiel réel
Le travail montre qu'il est possible « d'évoluer » une réaction à lumière bleue haute énergie vers un procédé à basse énergie proche infrarouge simplement en changeant la façon dont un sel métallique courant est assemblé en solution. Les systèmes de manganèse construits in situ évitent la synthèse chronophage de catalyseurs, utilisent un métal abondant et relativement peu toxique, et peuvent même être alimentés par la lumière naturelle du soleil. Pour les non‑spécialistes, le message clé est que nous n'avons pas toujours besoin d'une lumière plus agressive ou de métaux rares coûteux pour réaliser une chimie exigeante. En concevant des catalyseurs qui se forment eux‑mêmes à partir de composants simples et qui répondent à une lumière plus douce, cette approche ouvre la voie à des méthodes plus économes en énergie, évolutives et compatibles avec le monde biologique pour fabriquer les molécules complexes sur lesquelles reposent la médecine moderne et les matériaux.
Citation: Yang, W., Song, Y., Yu, X. et al. Evolution of manganese low-energy photoredox catalysis from high-energy visible light photocatalysis. Nat Commun 17, 2062 (2026). https://doi.org/10.1038/s41467-026-68837-y
Mots-clés: photoredox catalyse, catalyse au manganèse, lumière basse énergie, fonctionnalisation d'alcènes, radicaux azotés