Clear Sky Science · fr
Amorcer versus propager : effets immunitaires distincts des radiopharmaceutiques émetteurs de particules alpha ou bêta associés à une inhibition des points de contrôle immunitaire chez la souris
Transformer la radiation en alliée du système immunitaire
Les oncologues cherchent de plus en plus à mobiliser le système immunitaire contre les tumeurs, mais de nombreux cancers restent insensibles ou résistants à ces médicaments. Cette étude pose une question d’actualité : différents types de radiations ciblées peuvent‑ils servir non seulement à réduire les tumeurs directement, mais aussi à entraîner le système immunitaire pour qu’il soit plus efficace — et le choix du radiopharmaceutique modifie‑t‑il la manière dont cet entraînement fonctionne ?
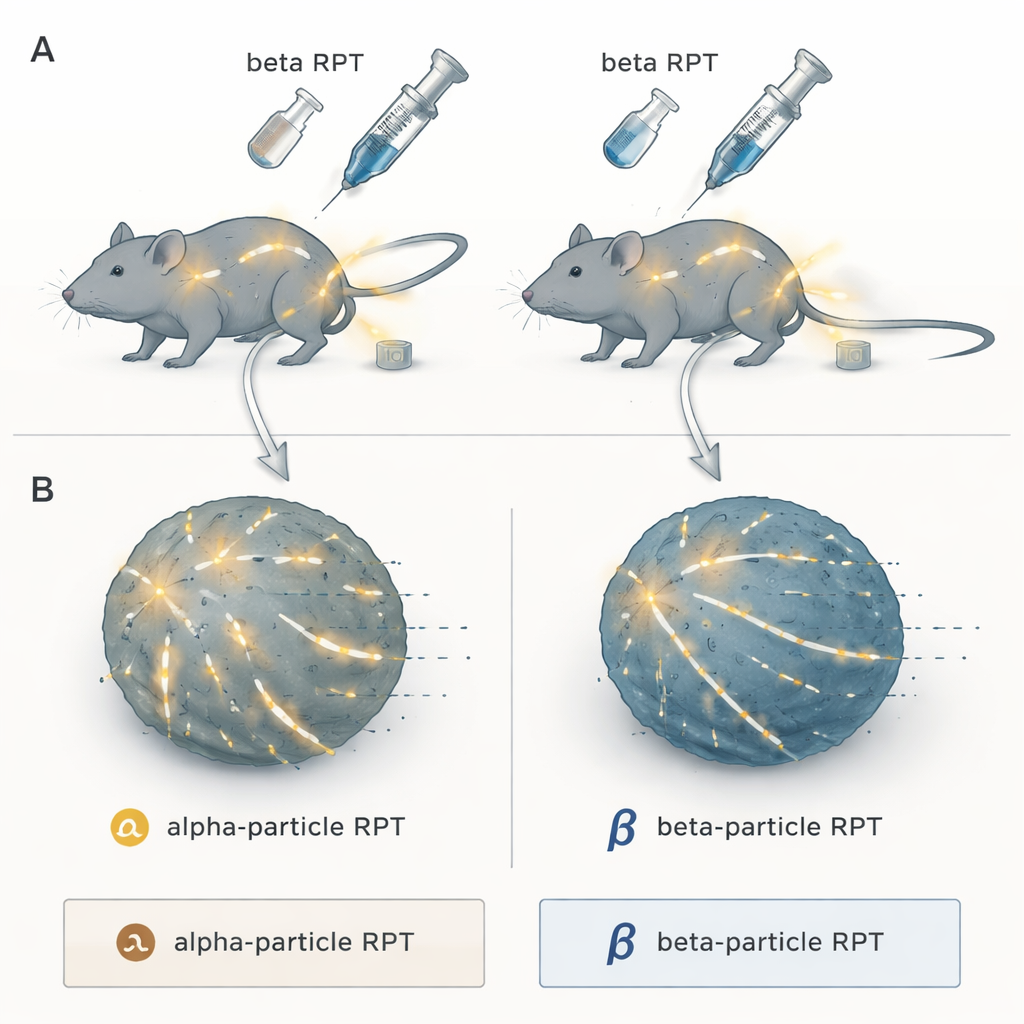
Deux formes de radiation de précision
Les chercheurs se sont intéressés à la thérapie radiopharmaceutique, une approche « chercher‑et‑détruire » où une charge radioactive est fixée à une molécule qui se dirige naturellement vers les tumeurs. Une fois injectée, elle circule dans l’organisme et délivre de la radiation aux foyers cancéreux où qu’ils se trouvent, ce que la radiothérapie externe ne peut pas facilement faire en cas de maladie disséminée. L’équipe a comparé deux grandes catégories : les émetteurs de particules alpha, qui libèrent des décharges d’énergie extrêmement denses sur une très courte distance, et les émetteurs de particules bêta, qui produisent une radiation de moindre densité se propageant plus loin dans les tissus. Tous étaient couplés au même composé ciblant les tumeurs, le NM600, de sorte que seule la nature de la radiation — et non le ciblage — différait.
Associer la radiation aux bloqueurs des points de contrôle immunitaire
Pris isolément, des inhibiteurs de points de contrôle comme anti‑PD‑L1 et anti‑CTLA4 peuvent lever les freins sur les cellules immunitaires, mais ils fonctionnent mieux quand la tumeur est déjà visible par le système immunitaire. Dans des modèles murins de mélanome, de cancer de la prostate et de cancer colorectal, les scientifiques ont administré une faible dose de radiation, choisie avec soin, issue soit du NM600 émetteur alpha soit du NM600 émetteur bêta, avec ou sans combinaison d’inhibiteurs de points de contrôle. Ils ont aussi varié le moment d’administration des immunothérapies — avant, peu après ou bien après le traitement radiatif — pour voir comment le calendrier influençait des résultats tels que la croissance tumorale, la survie et la mémoire immunitaire à long terme.
Quand la radiation bêta brille : renforcer une réponse existante
Dans un modèle de cancer colorectal « immuno‑chaud » qui répond déjà à l’immunothérapie, les meilleurs résultats ont été obtenus avec le NM600 émetteur bêta, en particulier lorsque les immunothérapies étaient débutées tôt ou à un moment intermédiaire. Les tumeurs ont davantage régressé, les souris ont vécu plus longtemps, et les animaux guéris ont souvent rejeté la même tumeur réintroduite plusieurs mois plus tard. Le profilage immunitaire détaillé a montré que le traitement à base de bêta associé au blocage des points de contrôle n’avait pas tant créé une nouvelle réponse que renforcé une réponse déjà présente : des lymphocytes T cytotoxiques tumoraux préexistants se sont amplifiés, sont devenus plus activés et ont produit davantage de signaux d’attaque. En résumé, les émetteurs bêta étaient excellents pour propager une réponse immunitaire en cours.
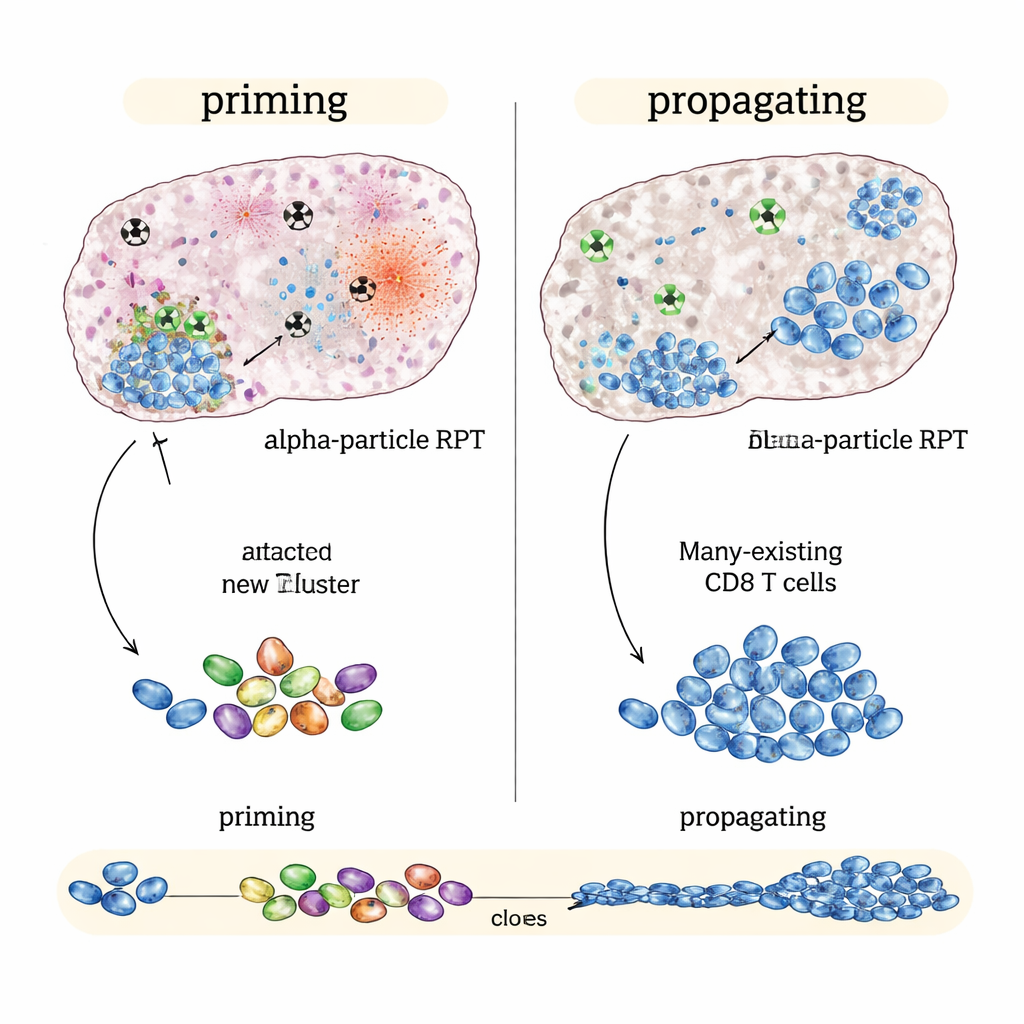
Quand la radiation alpha brille : déclencher une nouvelle attaque immunitaire
Inversement, dans des tumeurs « immuno‑froides » telles qu’un modèle de mélanome et un modèle de cancer de la prostate qui répondent peu aux seuls inhibiteurs de points de contrôle, la version émettrice alpha a mieux performé que les bêta à dose moyenne tumorale équivalente. La thérapie alpha associée aux médicaments immunitaires a ralenti davantage la croissance tumorale et prolongé la survie. Des analyses génétiques cellule par cellule suggèrent pourquoi : la radiation alpha provoquait des dommages intenses et localisés qui semblaient générer de puissants signaux d’alerte au sein de la tumeur tout en épargnant les structures immunitaires proches. Ce schéma était associé à des réponses de lymphocytes T plus larges et diversifiées et à des signes de formation de nouveaux lymphocytes T cytotoxiques reconnaissant la tumeur et connectés à des cellules mémoire de longue durée — preuve d’un amorçage immunitaire plutôt que d’une simple amplification.
Pourquoi le type et le timing de la radiation comptent
À travers les différents modèles, une administration précoce ou intermédiaire des inhibiteurs de points de contrôle — coïncidant approximativement avec le pic des signaux de danger induits par la radiation — a régulièrement surpassé un traitement retardé. Le travail suggère une règle pratique : dans les cancers déjà visibles par le système immunitaire, de faibles doses de radiopharmaceutiques à base de bêta peuvent être des partenaires idéaux des inhibiteurs de points de contrôle parce qu’ils propagent et renforcent l’immunité existante. Dans des cancers plus résistants sur le plan immunitaire, des émetteurs alpha à fort impact peuvent mieux amorcer de nouvelles réponses des lymphocytes T et transformer une tumeur « froide » en tumeur « chaude ». Pour les patients, cela signifie que tous les radiopharmaceutiques ne sont pas interchangeables ; adapter l’isotope et le calendrier à la personnalité immunitaire de la tumeur pourrait rendre la radio‑immunothérapie combinée à la fois plus efficace et plus durable.
Citation: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Mots-clés: thérapie radiopharmaceutique, radiation alpha vs bêta, inhibiteurs des points de contrôle immunitaire, immunothérapie du cancer, microenvironnement tumoral