Clear Sky Science · fr
Sécurité et activité biologique d’un récepteur T bispécifique ciblant le Gag du VIH chez des hommes vivant avec le VIH : un essai de première administration chez l’homme
Pourquoi cette nouvelle étude sur le VIH est importante
Les personnes vivant avec le VIH peuvent aujourd’hui espérer une espérance de vie proche de la normale grâce aux cocktails médicamenteux modernes. Mais ces traitements, appelés thérapie antirétrovirale (TAR), n’éliminent pas le virus ; ils le contrôlent simplement. Des poches cachées de VIH subsistent dans l’organisme et peuvent relancer l’infection si le traitement est interrompu. Cette étude évalue une nouvelle forme de thérapie immunitaire de précision — construite à partir d’un récepteur T synthétique — qui vise à apprendre au système immunitaire à traquer ces cachettes en toute sécurité chez des personnes déjà bien contrôlées sous TAR.
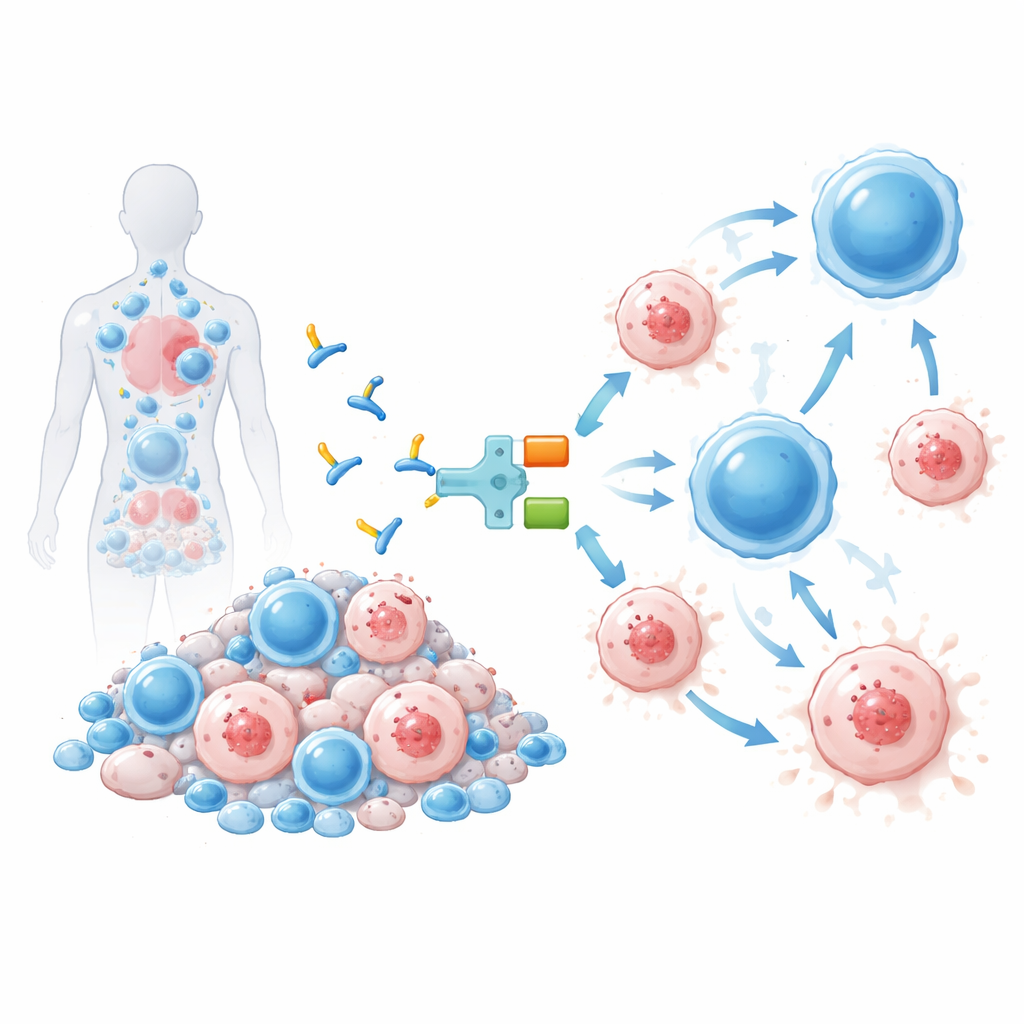
Le virus caché qui ne disparaît pas
Même lorsque les tests sanguins indiquent un virus « indétectable », le VIH persiste sous forme de matériel génétique logé dans des cellules de longue durée de vie, principalement un type de globules blancs appelés cellules T CD4. Ces cellules réservoirs portent un virus silencieux mais intact qui peut se réactiver et obliger les personnes à prendre des comprimés quotidiennement à vie. Effacer complètement chaque cellule infectée est extrêmement difficile et n’a été réalisé que chez quelques personnes ayant subi des greffes de moelle osseuse risquées pour un cancer. Beaucoup de chercheurs visent plutôt une « guérison fonctionnelle » : réduire suffisamment le réservoir pour que les défenses naturelles du corps puissent maintenir le VIH sous contrôle sans médication continue.
Une molécule conçue pour rediriger les cellules T
La thérapie testée ici, appelée IMC‑M113V, est une petite protéine qui agit comme un adaptateur moléculaire entre les cellules infectées et le système immunitaire. Une extrémité d’IMC‑M113V est un récepteur T conçu qui reconnaît un petit fragment du VIH provenant de la protéine Gag présenté à la surface des cellules infectées dans le contexte d’un marqueur immunitaire courant (HLA‑A*02:01). L’autre extrémité se fixe sur CD3, une structure présente sur toutes les cellules T. Quand IMC‑M113V se lie aux deux côtés à la fois, il rapproche des cellules T ordinaires d’une cellule infectée par le VIH et déclenche leur destruction. En tests de laboratoire, cette molécule était extrêmement sensible, détectant seulement quelques copies du fragment viral à la surface d’une cellule et éliminant efficacement des cellules infectées par plusieurs variants courants du VIH, tout en ne provoquant pas d’activation significative contre un panel de cellules humaines saines.
Premier test chez des personnes vivant avec le VIH
Pour évaluer la sécurité de cette approche chez l’homme, les chercheurs ont mené un essai de phase précoce chez douze hommes adultes vivant avec le VIH au Royaume‑Uni, en Belgique et en Espagne. Tous les participants avaient une infection bien contrôlée sous TAR, des taux élevés de CD4 et possédaient le type HLA requis. Chaque personne a reçu une dose intraveineuse unique d’IMC‑M113V à l’un des trois faibles niveaux de dose, puis a été étroitement suivie pendant un mois. L’objectif principal à ce stade était la sécurité : rechercher des effets indésirables tels que fièvre, inflammation sévère ou problèmes neurologiques, qui peuvent survenir avec d’autres médicaments puissants mobilisant les cellules T utilisés en oncologie.
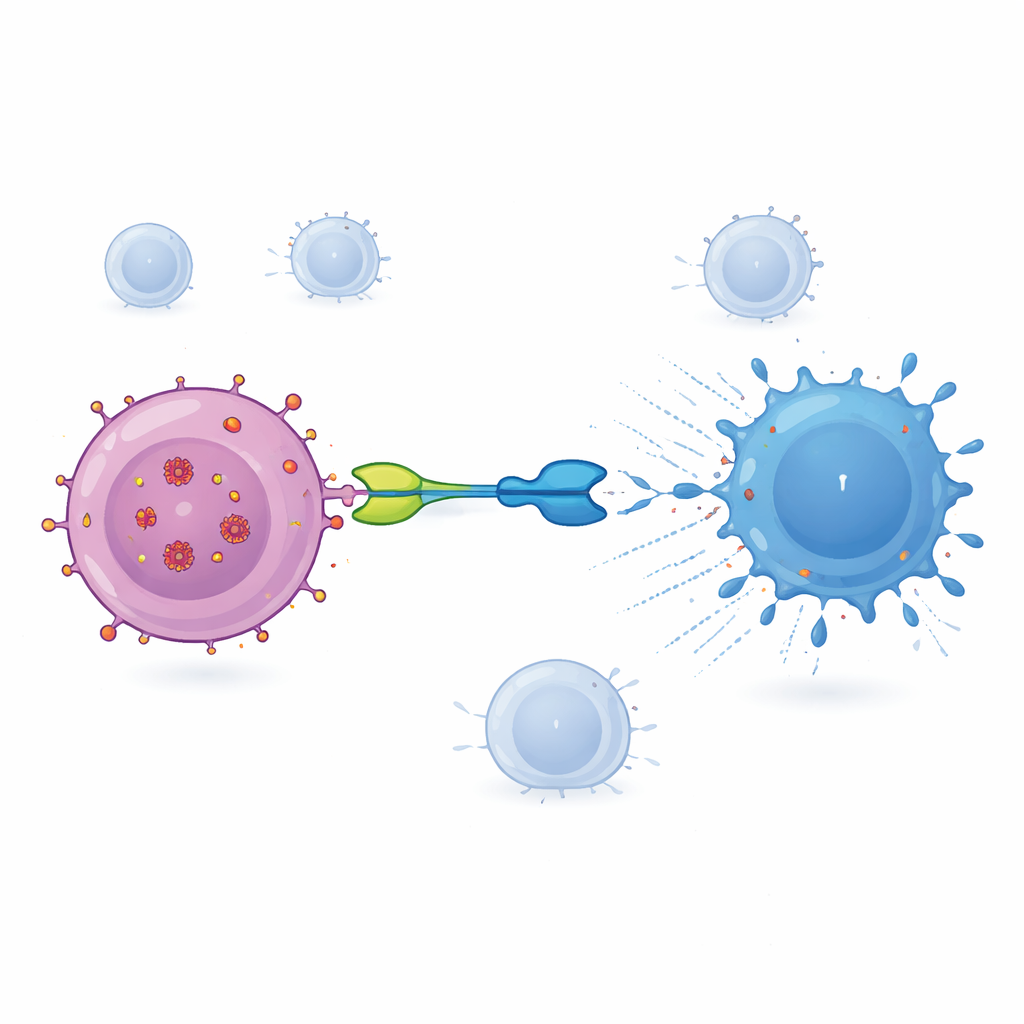
Ce que les chercheurs ont observé en clinique
Sur l’ensemble des doses, IMC‑M113V a été généralement bien toléré. La moitié des participants ont signalé des effets indésirables, principalement des problèmes légers comme de la fatigue ou des irritations cutanées, et personne n’a développé de complications graves telles que le syndrome de libération de cytokines ou une neurotoxicité. Les analyses sanguines ont montré que les niveaux du médicament augmentaient puis diminuaient en environ un jour, avec une demi‑vie d’environ 15–22 heures. À la dose la plus élevée (15 microgrammes), plusieurs participants ont présenté des augmentations temporaires de molécules inflammatoires, en particulier de l’interleukine‑6, et des signes d’activation des cellules T avec une plus grande capacité à produire des protéines cytotoxiques. Ces changements immunitaires étaient les plus marqués chez les volontaires dont les virus portaient des variantes de Gag que l’IMC‑M113V peut lier particulièrement bien, ce qui suggère que le médicament ciblait ses cibles prévues in vivo. Cependant, après une dose unique, il n’y a pas eu de réduction mesurable de la taille du réservoir viral dans le sang, évaluée par l’ARN viral et l’ADN viral intact à l’intérieur des cellules CD4.
Ce que cela signifie pour les traitements futurs du VIH
Pour un lecteur non spécialiste, le message principal est que cette étude apporte une première preuve de concept importante : une molécule « pont » immunitaire très ciblée peut être administrée en toute sécurité à des personnes vivant avec un VIH bien contrôlé et peut réveiller leurs cellules T pour reconnaître des cellules abritant le virus. Elle n’a pas guéri le VIH ni permis d’arrêter la TAR, mais ce n’était pas l’objectif de cet essai de première administration chez l’humain. Ces résultats soutiennent l’évaluation de doses plus élevées et répétées, éventuellement en combinaison avec des médicaments qui incitent davantage de cellules infectées à se révéler, et l’élargissement de l’approche à d’autres types HLA au‑delà de HLA‑A*02:01. Si des études futures confirment que cette stratégie peut réduire de façon fiable les réservoirs viraux sans effets indésirables dangereux, elle pourrait devenir une composante clé des traitements combinés visant un contrôle durable du VIH sans médicaments.
Citation: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
Mots-clés: Guérison du VIH, Thérapie cellulaire T, réservoir viral, récepteur bispécifique, essai clinique