Clear Sky Science · fr
La transcriptomique unicellulaire guidée par la chimie révèle une remodelage de l’échafaudage médié par des sulfotransférases dans la biosynthèse de la sécurinine
Pourquoi la chimie d’un arbuste compte
Les alcaloïdes de type securinega sont des molécules puissantes présentes dans un petit arbuste ornemental, Flueggea suffruticosa, longtemps étudié pour ses applications possibles contre le cancer et les maladies neurologiques. Pourtant, jusqu’à présent, personne ne savait vraiment comment cette plante fabriquait ces composés complexes. Cette étude combine la lecture moderne des gènes cellule par cellule avec des expériences chimiques astucieuses pour révéler, étape par étape, comment la plante assemble et remanie ces molécules — et met au jour, en chemin, un rôle surprenant pour un type d’enzyme commun. 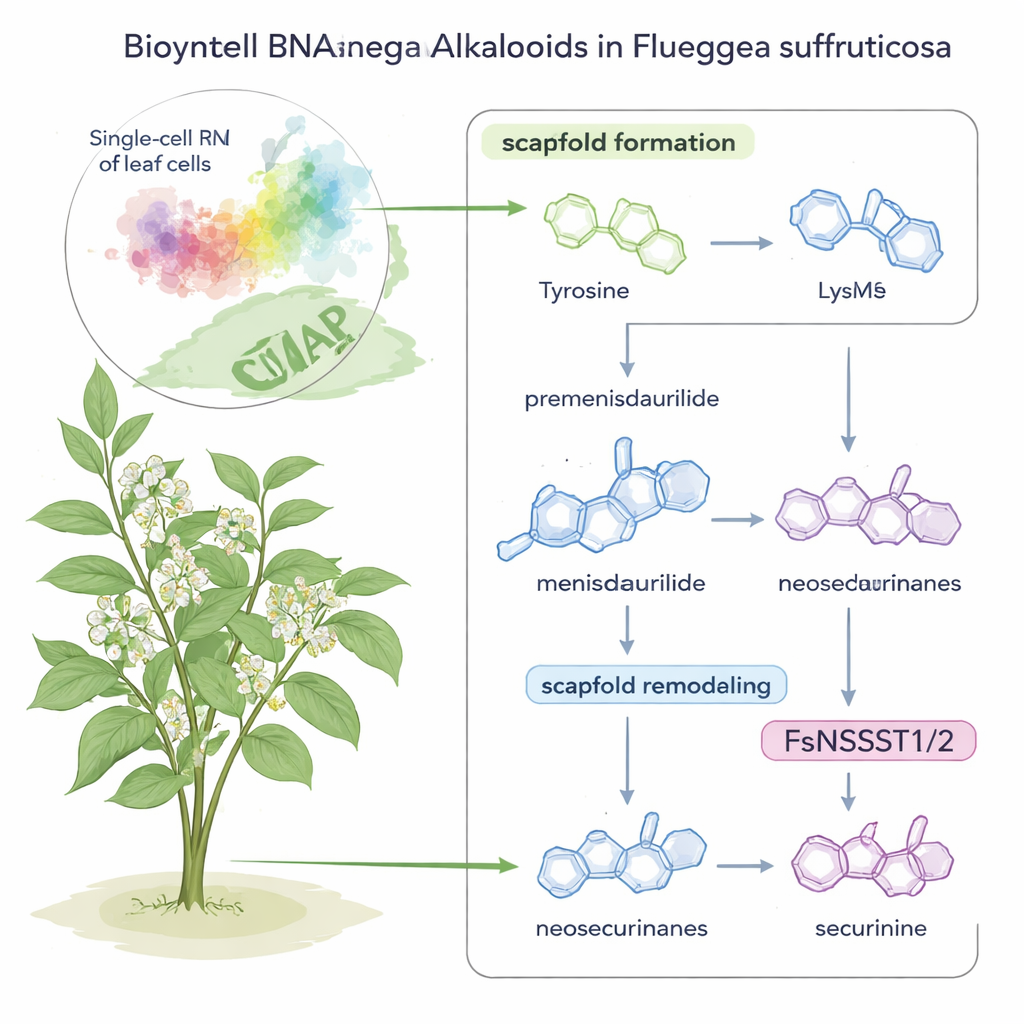
Des blocs de construction issus d’acides aminés courants
L’histoire commence avec deux nutriments familiers : les acides aminés tyrosine et lysine. Chez F. suffruticosa, la tyrosine est transformée en une molécule annulaire inhabituelle appelée prémenisdaurilide, qui est ensuite réduite en menisdaurilide par une enzyme nouvellement découverte que les auteurs nomment FsMS (pour « menisdaurilide synthase »). Parallèlement, la lysine est convertie en un petit cycle azoté appelé 1-pipérideine par une autre enzyme, FsPS, découverte dans des travaux antérieurs. Lorsque menisdaurilide et 1-pipérideine se rencontrent dans des conditions légèrement basiques et aquatiques, ils fusionnent spontanément pour former des alcaloïdes « néosécurinane » — des structures intermédiaires sur la voie menant aux composés finaux d’intérêt médical.
Observer la chimie en temps réel
Pour prouver que ces étapes proposées ne sont pas que théoriques, l’équipe a synthétisé des versions des intermédiaires suspectés marquées avec des atomes de carbone lourds. En administrant ces molécules marquées à des extraits de plante, les chercheurs ont pu tracer exactement où les atomes aboutissaient. Ils ont observé la conversion du menisdaurilide marqué en néosécurinanes marqués, puis en les alcaloïdes connus allosécurinine et sécurinine, confirmant que ces intermédiaires appartiennent bien à la voie naturelle. Fait important, certaines des réactions clés de formation d’anneau ont eu lieu même dans des extraits bouillis, montrant qu’une partie de la route peut se dérouler sans enzymes, simplement portée par la chimie intrinsèque des molécules.
Se concentrer sur les bonnes cellules
Savoir quelles molécules apparaissent où n’est que la moitié de l’équation ; identifier les gènes qui contrôlent chaque étape nécessite de savoir quelles cellules effectuent le travail. Les chercheurs ont séquencé l’ARN de milliers de cellules individuelles prélevées sur des feuilles de F. suffruticosa, les regroupant en types cellulaires distincts selon les profils d’activité génique. Un groupe, associé aux nervures de la feuille, a émergé : il exprimait fortement les gènes de la voie connus ainsi que de nombreuses enzymes liées au métabolisme de la tyrosine, de la lysine et du soufre. En examinant quels gènes variaient de concert avec les enzymes de la voie au sein de ce groupe, l’équipe a ciblé FsMS et deux sulfotransférases, FsNSST1 et FsNSST2, comme candidats principaux pour les étapes manquantes. 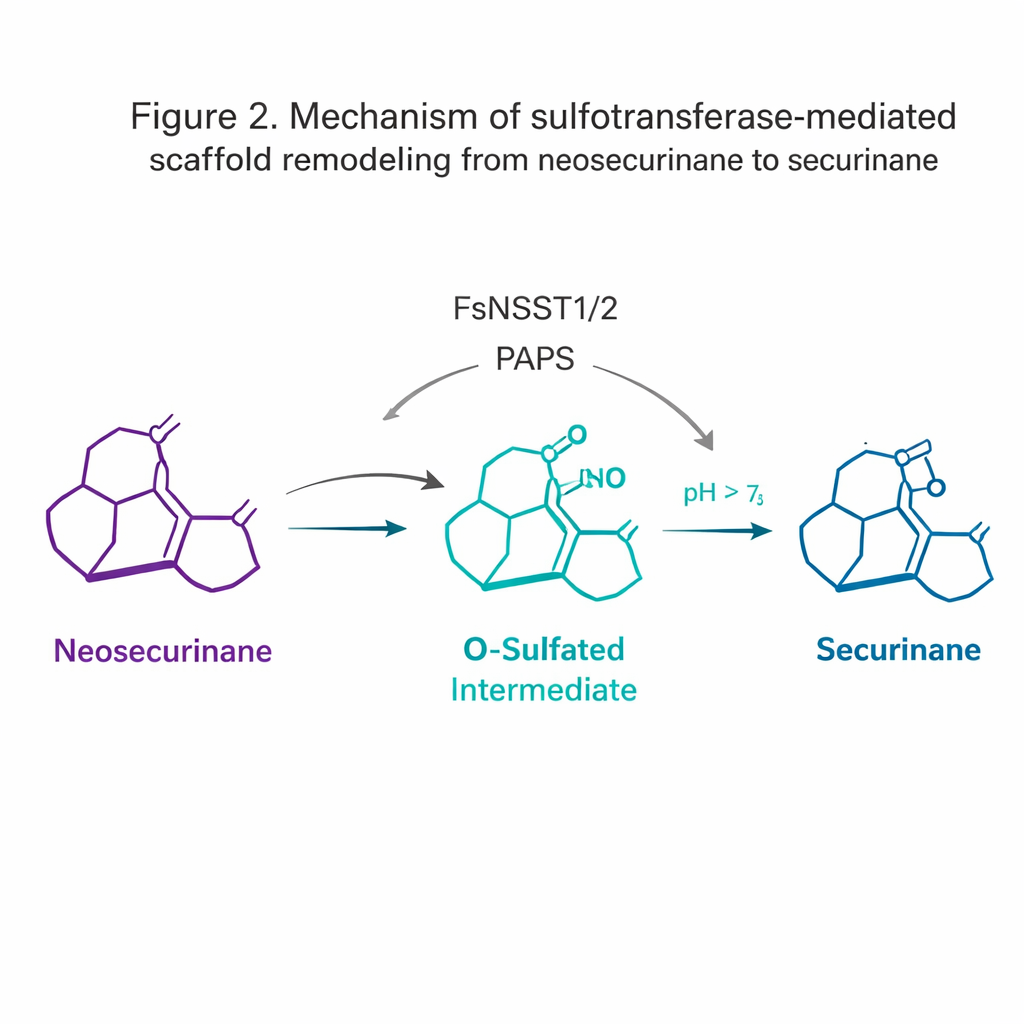
Une enzyme qui remodèle l’échafaudage moléculaire
La découverte la plus surprenante provient des sulfotransférases. Les sulfotransférases ajoutent habituellement un groupe sulfate aux molécules pour améliorer leur solubilité ou les marquer pour la dégradation. Ici, FsNSST1 et FsNSST2 jouent plutôt le rôle de commutateurs : elles fixent un sulfate sur l’échafaudage néosécurinane, le transformant brièvement en un intermédiaire « O-sulfoné » à haute énergie. Cette forme activée subit ensuite un déplacement spontané 1,2-amine — une petite réorganisation où un atome d’azote migre — convertissant la charpente bicyclique [2.2.2] « néosécurinane » en la charpente [3.2.1] « sécurinane ». Ce remaniement subtil est ce qui donne le cœur tétracyclique distinctif des alcaloïdes biologiquement actifs.
Pourquoi cette voie a de l’importance
Pour le non-spécialiste, le message clé est que la plante assemble les alcaloïdes securinega en deux phases principales : d’abord, elle construit un système d’anneaux préliminaire à partir d’acides aminés courants ; puis elle remanie chimiquement cet échafaudage en une forme plus complexe au moyen d’un « déclencheur » sulfate. En combinant le profilage génique cellule par cellule avec la chimie aux isotopes marqués, les auteurs cartographient cette voie en détail et révèlent que les sulfotransférases — des enzymes présentes chez tous les êtres vivants — peuvent faire plus que simplement décorer des molécules ; elles peuvent initier des réarrangements complets de leur architecture. Comprendre cette voie clarifie non seulement comment une classe prometteuse de molécules de type médicament est produite dans la nature, mais ouvre aussi la voie à l’ingénierie de plantes ou de microbes pour produire de nouveaux médicaments inspirés des securinega.
Citation: Choung, S., Kang, G., Kim, T. et al. Chemically guided single-cell transcriptomics reveals sulfotransferase-mediated scaffold remodeling in securinine biosynthesis. Nat Commun 17, 1954 (2026). https://doi.org/10.1038/s41467-026-68816-3
Mots-clés: alcaloïdes végétaux, biosynthèse, transcriptomique unicellulaire, sulfotransférase, chimie des produits naturels