Clear Sky Science · fr
La méthylation de l’ARNt dépendante d’ALKB‑1 est nécessaire à l’élimination paternelle efficace des mitochondries
Pourquoi les mitochondries paternelles disparaissent discrètement
Tous les humains, les nématodes et la plupart des autres animaux héritent de leurs centrales cellulaires — les mitochondries — presque entièrement de leur mère. Les mitochondries du père pénètrent dans l’ovule avec le spermatozoïde mais sont rapidement éliminées, un nettoyage biologique qui évite la transmission d’ADN mitochondrial endommagé. Cette étude menée chez de petits vers ronds révèle un « point de contrôle » moléculaire lié au stress qui contribue à décider si les mitochondries paternelles sont efficacement éliminées, donnant des pistes susceptibles un jour d’éclairer certains cas d’infertilité et de maladies mitochondriales.
Les usines énergétiques que nous héritons de notre mère
Les mitochondries produisent l’énergie qui maintient les cellules en vie et portent leur propre petit cercle d’ADN. Au cours d’une vie, cet ADN mitochondrial peut accumuler des mutations délétères. Si les deux parents transmettaient systématiquement leurs mitochondries, ces défauts pourraient se mélanger et s’amplifier de génération en génération. Pour l’éviter, la plupart des animaux reposent sur l’héritage maternel : l’embryon conserve les mitochondries maternelles et élimine presque toutes celles du père peu après la fécondation. Bien que plusieurs voies d’élimination soient connues — comme les systèmes de recyclage cellulaires et des enzymes qui coupent l’ADN — les scientifiques n’avaient pas entièrement compris comment de subtiles marques chimiques sur l’ADN et l’ARN peuvent influencer cette élimination des mitochondries paternelles.
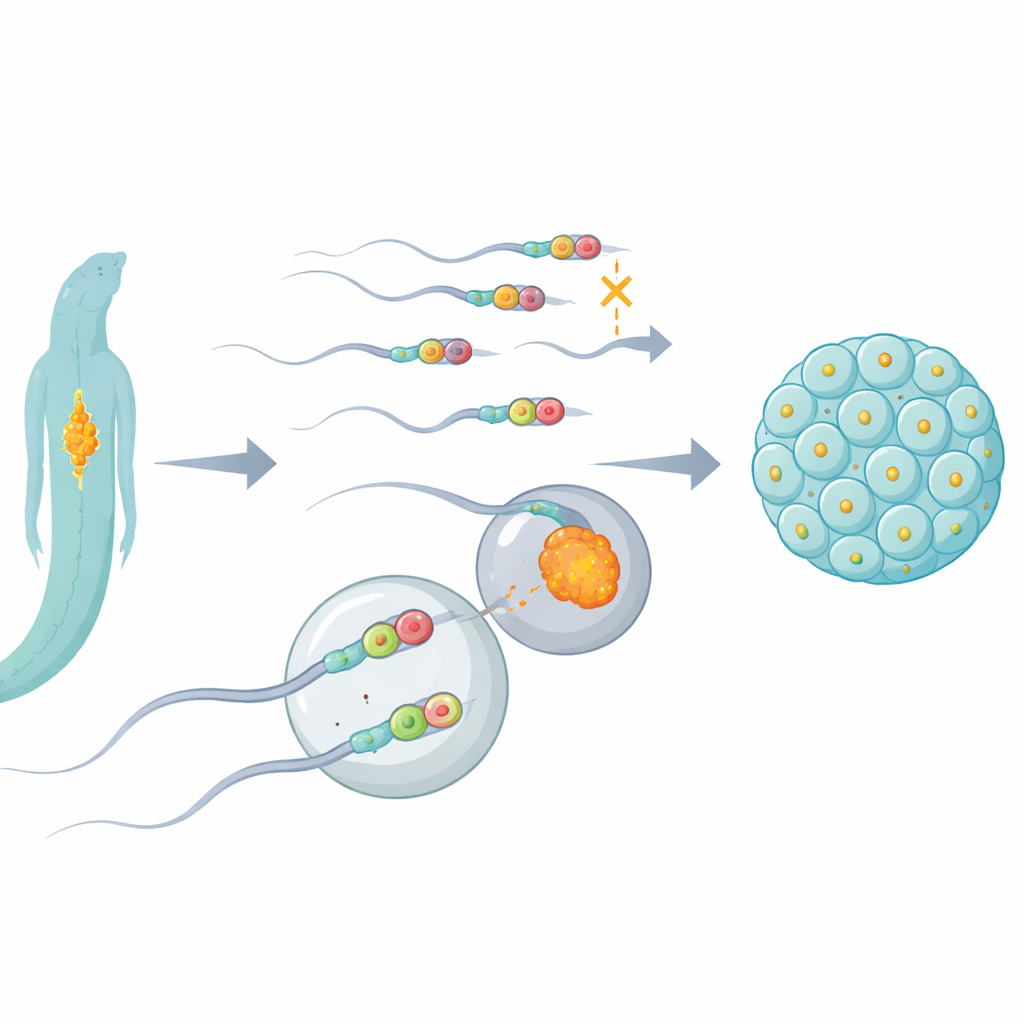
Une gomme moléculaire avec un rôle clé en reproduction
Les chercheurs se sont concentrés sur une protéine appelée ALKB‑1 chez le nématode Caenorhabditis elegans, un modèle de prédilection en génétique. ALKB‑1 est une sorte d’effaceur moléculaire capable d’enlever des groupes méthyle — de minuscules étiquettes chimiques — de l’ADN et de l’ARN. En désactivant sélectivement ALKB‑1 ou en réduisant son niveau, l’équipe a suivi ce qui arrivait aux mitochondries spermatiques et à leur ADN après la fécondation. Ils ont constaté que lorsque l’activité « d’effacement » chimique d’ALKB‑1 était perdue, les mitochondries paternelles et leur ADN persistaient anormalement longtemps dans les embryons en développement, au lieu d’être rapidement éliminés. Ce retard survenait principalement lorsque ALKB‑1 manquait dans les spermatozoïdes, et s’accompagnait de spermatozoïdes contenant un nombre inhabituellement élevé de mitochondries et d’ADN mitochondrial.
Comment la manipulation de la chimie de l’ARNt perturbe les mitochondries
En approfondissant, les scientifiques ont cherché quelles marques chimiques importaient vraiment pour ALKB‑1. Les tests sur l’ADN ont suggéré que des modifications de la méthylation de l’ADN seules ne pouvaient pas expliquer le problème d’élimination. L’attention s’est donc portée sur les ARNt, de petites molécules adaptatrices qui aident à traduire les messages génétiques en protéines. Chez les vers normaux, ALKB‑1 retire une marque spécifique — appelée m1A — d’un sous-ensemble d’ARNt. Sans ALKB‑1, ces marques s’accumulaient. Ce changement subtil dans la chimie des ARNt a largement modifié l’efficacité de synthèse de nombreuses protéines : la production protéique dans le cytosol a augmenté, tandis que la synthèse protéique à l’intérieur des mitochondries s’est détériorée. Le résultat a été un décalage entre les protéines destinées aux mitochondries et ce que les organites pouvaient gérer, conduisant à des agrégats de protéines mal traitées et à des signes de stress mitochondrial.
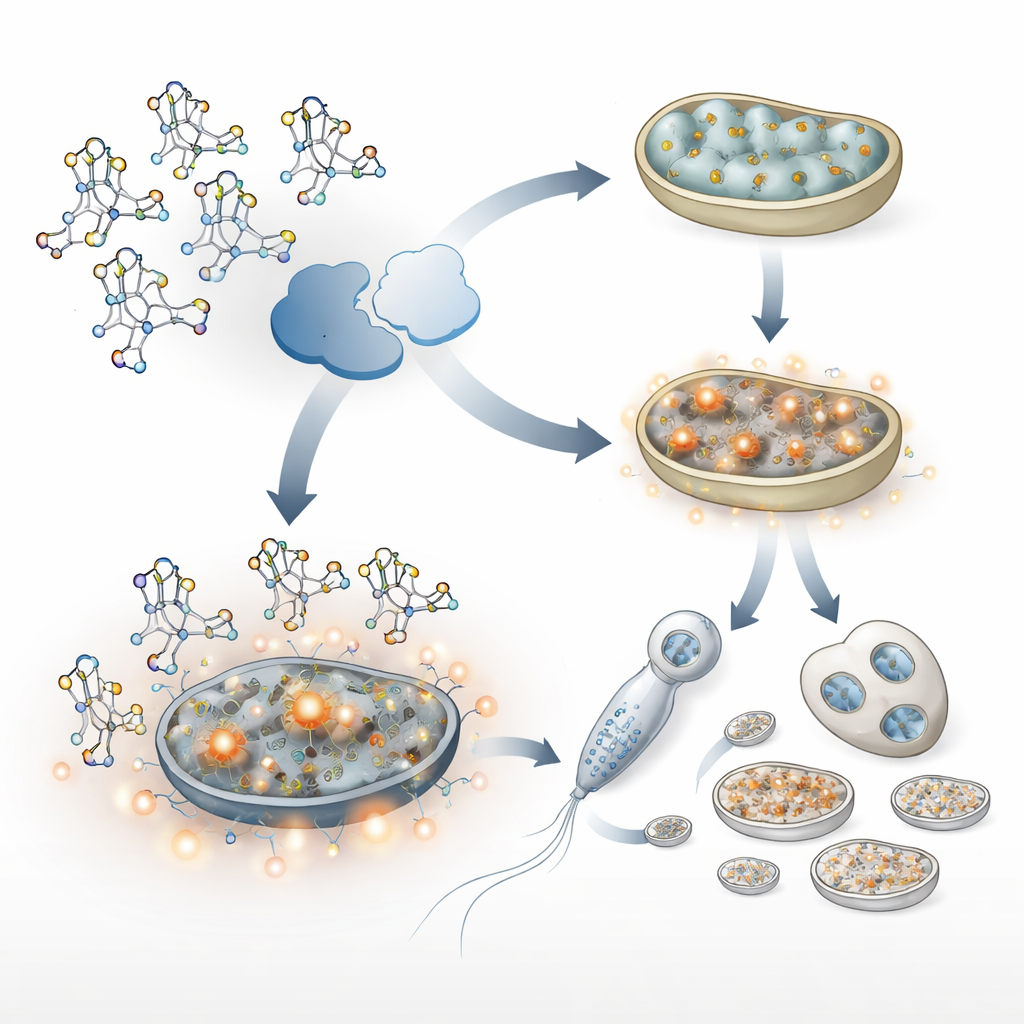
Signaux de stress qui protègent — et préservent involontairement — les mitochondries paternelles
Les mitochondries stressées produisent souvent davantage d’espèces réactives de l’oxygène, des sous‑produits chimiquement agressifs du métabolisme. Chez les vers déficients en ALKB‑1, ces molécules réactives augmentaient fortement. Cela a activé deux programmes clés de réponse au stress : l’un conduit par un facteur semblable au Nrf2 humain (appelé SKN‑1 chez les vers), et l’autre connu sous le nom de réponse mitochondriale aux protéines non repliées. Ensemble, ces voies ont stimulé la production de nouvelles mitochondries et augmenté la réplication de l’ADN mitochondrial, en particulier dans les spermatozoïdes. Si cette réponse aide les cellules à faire face aux dommages, elle avait aussi un effet indésirable : davantage de mitochondries paternelles et d’ADN mitochondrial s’accumulaient et étaient plus difficiles à éliminer après la fécondation. Bloquer ces voies de stress, ou réduire les dommages oxydatifs avec des antioxydants, rétablissait une élimination plus normale des mitochondries paternelles.
Quand le nettoyage échoue, la fertilité et les embryons en pâtissent
Le retard d’élimination des mitochondries paternelles n’était pas qu’une curiosité microscopique. Les mâles dépourvus d’une activité ALKB‑1 adéquate engendraient moins de descendants, et les embryons qu’ils contribuaient à former mouraient plus souvent. Pourtant, leurs spermatozoïdes se formaient en nombre normal et semblaient structurellement intacts, ce qui suggère que le problème principal résidait dans le contrôle de la qualité mitochondriale plutôt que dans la production de spermatozoïdes. L’étude propose que les marques d’ARNt contrôlées par ALKB‑1 agissent comme un point de contrôle épigénétique : lorsque ce système fonctionne, l’équilibre des protéines mitochondriales est maintenu, le stress reste maîtrisé et les mitochondries paternelles sont éliminées en toute sécurité. Lorsqu’il échoue, des mitochondries paternelles stressées et en surnombre persistent, nuisant à la fertilité et au développement précoce. Bien que ces expériences aient été réalisées chez des vers, elles éclairent un principe fondamental — de minuscules modifications chimiques de l’ARN peuvent orienter la manière dont nous héritons de nos centrales cellulaires et pourraient, in fine, influencer la santé reproductive chez des animaux plus complexes, y compris les humains.
Citation: Luo, Z., Li, Y., He, C. et al. ALKB-1-dependent tRNA methylation is required for efficient paternal mitochondrial elimination. Nat Commun 17, 2144 (2026). https://doi.org/10.1038/s41467-026-68813-6
Mots-clés: héritage mitochondrial, mitochondries paternelles, méthylation de l’ARNt, stress oxydatif, fertilité masculine