Clear Sky Science · fr
Le paysage fonctionnel de l'épissage alternatif dans l'engagement des lignées hématopoïétiques
Comment de minuscules retouches dans les gènes façonnent notre sang
Toutes les secondes, votre corps produit des millions de nouvelles cellules sanguines. Derrière ce miracle discret se cache un système moléculaire d'édition capable de couper et recoller des fragments de messages génétiques de manières différentes, créant des variantes légèrement distinctes d'une même protéine. Cette étude examine comment ce processus d'édition, appelé épissage alternatif, aide à orienter les cellules souches immatures vers la formation de globules rouges, de globules blancs ou d'autres types cellulaires sanguins — et ce qui se passe lorsqu'un seul segment édité fait défaut.
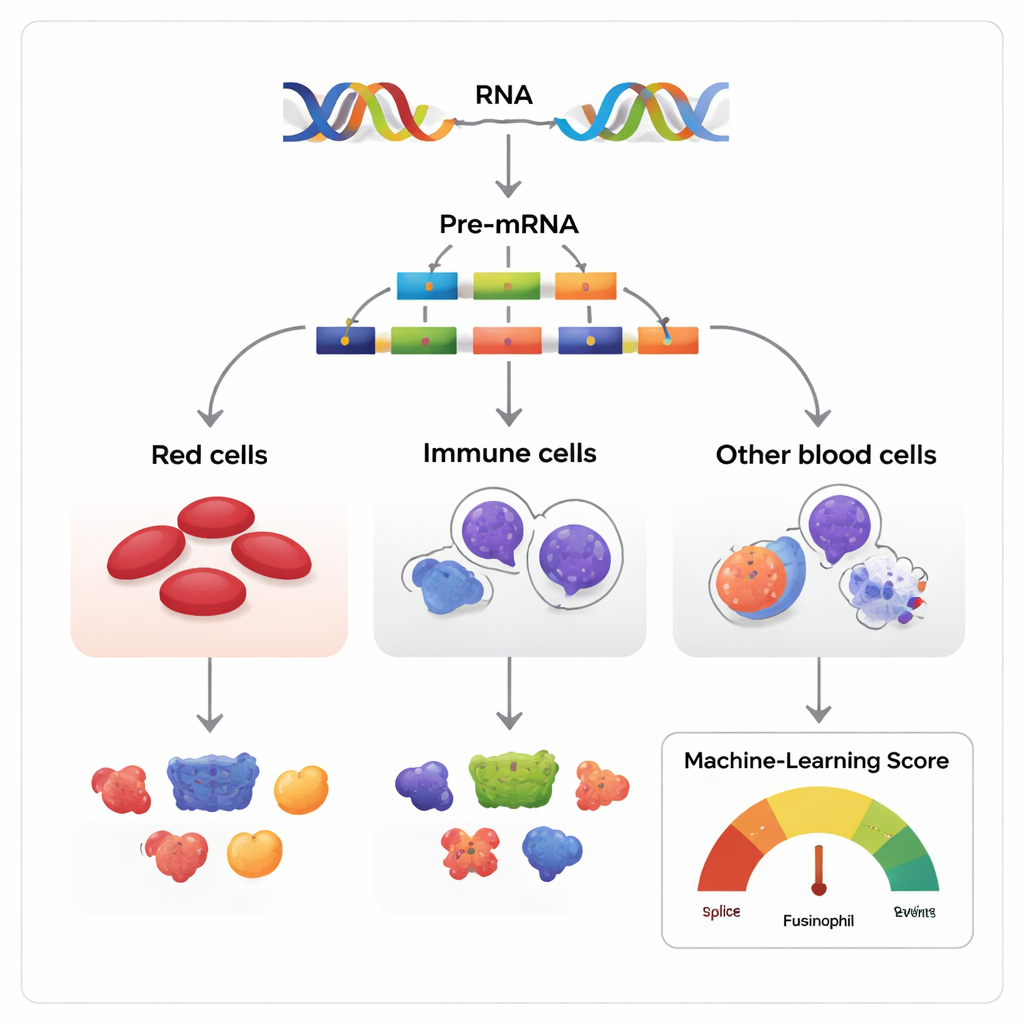
De nombreuses versions à partir du même script génétique
On décrit souvent les gènes comme des plans, mais en réalité ils ressemblent davantage à des scripts qui peuvent être réarrangés. Lorsqu'un gène est lu, la copie initiale d'ARN contient des segments appelés exons qui peuvent être conservés ou sautés avant que le message final ne soit traduit en protéine. Les auteurs ont étudié ce processus, connu sous le nom de saut d'exon, dans les tissus hématopoïétiques de l'homme, de la souris et de plusieurs autres vertébrés. Ils ont assemblé plus de 270 jeux de données ARN suivant ensemble les cellules souches et progénitrices sanguines à mesure qu'elles maturent en trois grandes familles : les cellules érythroïdes productrices de globules rouges, les cellules myéloïdes combattant les infections et les cellules lymphoïdes productrices d'anticorps.
Classer les changements d'épissage qui comptent vraiment
Parce que la plupart des gènes multi-exons peuvent être épissés de multiples façons, le défi central est de distinguer les variations sans conséquence de celles qui influencent réellement le destin cellulaire. Les chercheurs ont construit un modèle d'apprentissage automatique, appelé Functional AS Score (FAScore), pour relever ce défi. Pour chaque événement de saut d'exon, le modèle prend en compte 19 éléments d'information, comme l'ampleur de la variation d'utilisation au cours du développement cellulaire, la conservation du ADN environnant entre les espèces, l'altération éventuelle de domaines protéiques connus, ou la présence de sites de modifications chimiques de la protéine. L'algorithme, entraîné selon une stratégie positive–non étiqueté et un classifieur random forest, produit un score entre 0 et 1 indiquant la probabilité qu'un événement d'épissage donné ait un impact fonctionnel.
Détection d'interrupteurs conservés et spécifiques aux lignées
En appliquant FAScore à des dizaines de milliers d'événements de saut d'exon, l'équipe les a classés en groupes probables fonctionnels, non fonctionnels ou incertains. Les événements prédits comme fonctionnels se trouvaient plus souvent dans des régions protéiques importantes pour les interactions, dans des séquences conservées évolutivement, et dans des segments hébergeant des marques chimiques telles que la phosphorylation ou la SUMOylation. Beaucoup de ces événements étaient également actifs uniquement dans des lignées sanguines spécifiques ou pendant la formation du sang fœtal, ce qui suggère qu'ils agissent comme des commutateurs finement réglés à des fenêtres développementales particulières. L'étude a montré en outre que certains des événements d'épissage les plus anciens — partagés entre vertébrés depuis des centaines de millions d'années — sont particulièrement susceptibles d'être fonctionnels, reflétant la tendance des gènes plus anciens à assumer des rôles biologiques centraux.
Preuve expérimentale : ajuster les résultats de la formation cellulaire sanguine
Pour tester les prédictions du modèle, les auteurs ont choisi plusieurs exons à score élevé dans des gènes actifs dans différentes lignées sanguines et ont supprimé ces exons dans des cellules souches et progénitrices sanguines de souris en utilisant CRISPR. Les résultats correspondaient aux attentes du modèle : la suppression de certains exons des gènes KLF6 et SSBP3 altérait la formation de colonies myéloïdes sans nuire à la production de cellules rouges, tandis que la suppression d'exons dans EPB41L1 et TBC1D23 modifiait la formation de colonies érythroïdes. En particulier, le saut de l'exon 15 de TBC1D23 réduisait la production de précurseurs des globules rouges chez la souris et le poisson zèbre, entraînant moins de globules rouges circulants et des taux d'hémoglobine plus faibles, tout en épargnant dans une large mesure les globules blancs.
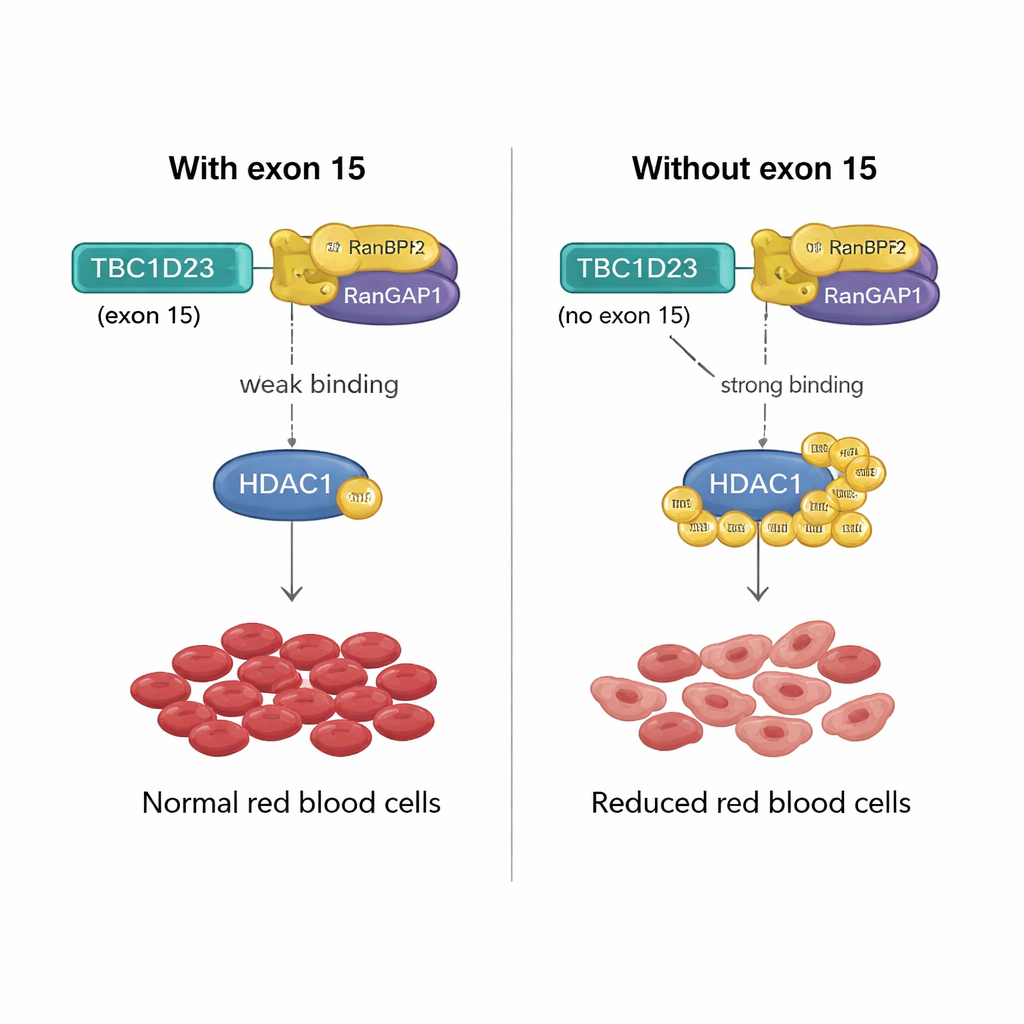
Un levier moléculaire pour la production de globules rouges
Comment un fragment de 15 acides aminés codé par l'exon 15 de TBC1D23 peut-il avoir un tel effet ? L'équipe a découvert que l'inclusion de cet exon affaiblit la liaison de TBC1D23 à un couple de protéines appelé RANBP2/RANGAP1, qui collabore pour attacher des étiquettes SUMO à d'autres protéines. En l'absence de l'exon 15, TBC1D23 se lie plus fortement à ce couple, augmentant la SUMOylation d'une enzyme clé, HDAC1. Cette étiquetage accru modifie l'activité de nombreux facteurs de transcription — régulateurs maîtres de l'expression génique — perturbant les programmes géniques nécessaires à la maturation correcte des globules rouges. Lorsque les chercheurs ont conçu une version de HDAC1 incapable d'être SUMOylée en deux positions cruciales, elle a permis de restaurer la formation des cellules rouges dans des cellules dépourvues de l'exon 15 de TBC1D23, confirmant que cette modification chimique est l'étape critique.
Pourquoi cela compte pour la santé et les thérapies futures
Pour un non-spécialiste, le message de ce travail est que toutes les modifications génétiques ne se valent pas : parfois, la différence entre un sang sain et une anémie tient à la conservation ou non d'un minuscule segment d'un gène dans le message final. En combinant des données ARN à grande échelle avec un système de notation sophistiqué, l'étude fournit une feuille de route pour repérer les variantes d'épissage les plus susceptibles d'influencer le choix de destin des cellules souches. Cette approche approfondit non seulement notre compréhension de la formation des cellules sanguines en santé et en maladie, mais offre aussi une stratégie générale pour identifier des événements d'épissage importants dans d'autres organes, pouvant guider de futures thérapies géniques et des traitements de précision.
Citation: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
Mots-clés: épissage alternatif, hématopoïèse, apprentissage automatique, globules rouges, régulation génique