Clear Sky Science · fr
Base structurale de la régulation transcriptionnelle par le régulateur de division cellulaire MraZ chez Mycoplasma genitalium
Comment une bactérie minuscule contrôle le moment de sa division
Chaque cellule vivante doit décider quand se scinder en deux, et cette décision peut faire la différence entre une croissance saine et une infection incontrôlée. Cette étude pénètre à l’intérieur d’une des bactéries les plus simples connues, Mycoplasma genitalium, pour révéler en détail atomique comment une seule protéine, nommée MraZ, s’accroche à l’ADN et active ou réprime des gènes clés de la division cellulaire. En comprenant ce système de contrôle minimaliste, les scientifiques espèrent dégager des règles générales de la croissance bactérienne qui pourraient un jour inspirer de nouveaux types d’antibiotiques ou des « cellules minimales » synthétiques.
Une cellule épurée qui livre de grandes leçons
Mycoplasma genitalium est célèbre pour son génome extrêmement réduit : une fraction seulement de l’ADN présent chez des bactéries courantes comme E. coli. Cette petite taille en fait un modèle puissant pour déterminer quels gènes et systèmes de contrôle sont vraiment indispensables à la vie. Beaucoup de bactéries regroupent leurs gènes de division cellulaire et de paroi dans un bloc appelé le cluster dcw. Chez les mycoplasmes dépourvus de paroi, la plupart de ces gènes ont disparu, mais quelques-uns subsistent, dont mraZ à l’avant du cluster. MraZ joue le rôle de chef de circulation, contrôlant l’activité de ses gènes voisins, qui influent à leur tour sur la façon et le moment où la cellule se divise.
Un motif d’ADN répété comme interrupteur de contrôle
Juste en amont du gène mraZ, les chercheurs ont identifié un segment d’ADN hautement conservé qui sert de station d’accostage pour la protéine MraZ. Cette région contient quatre courts segments répétés, ou « boîtes », dont la séquence est presque identique dans de nombreuses espèces bactériennes. En mutagenant soigneusement une, deux ou plusieurs de ces boîtes puis en mesurant l’affinité d’assemblage de MraZ pour l’ADN, l’équipe a montré que la protéine se lie de manière coopérative : chaque boîte renforce l’adhérence globale. Des expériences rapporteurs utilisant un marqueur fluorescent ont confirmé que plus ces boîtes étaient perturbées, moins MraZ pouvait réprimer efficacement l’activité génique, soulignant leur importance comme panneau de contrôle finement réglé. 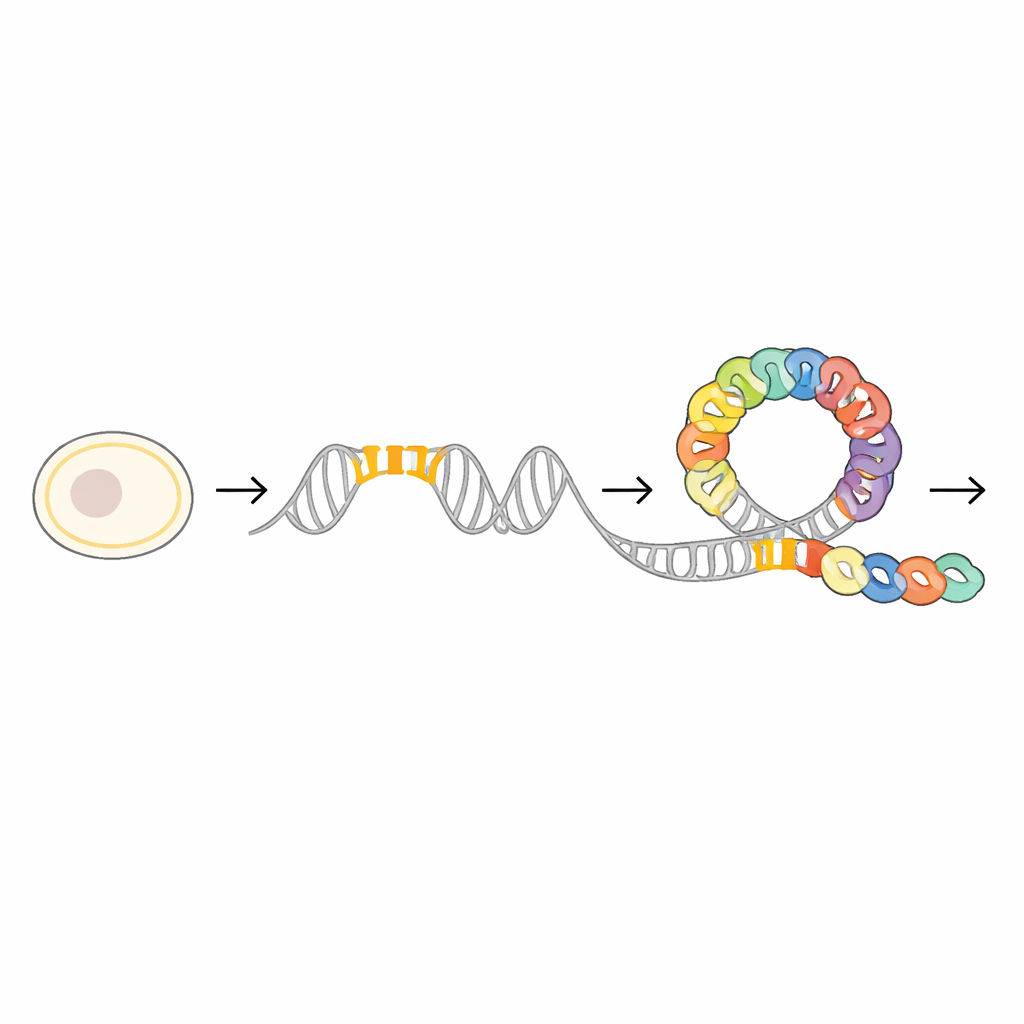
Une protéine en anneau qui s’ouvre pour embrasser l’ADN
Pour comprendre comment ce panneau de contrôle fonctionne au niveau atomique, les scientifiques ont utilisé la cryo‑microscopie électronique et la cristallographie aux rayons X pour résoudre plusieurs structures tridimensionnelles de MraZ seul et lié à l’ADN. Isolées, les molécules de MraZ s’assemblent en structures annulaires composées de huit ou neuf sous‑unités identiques. Ces anneaux présentent une surface caractéristique en « berceau » formée par une petite feuillet bêta, contrairement aux hélices spiralées souvent observées dans les protéines liant l’ADN. Lorsque MraZ rencontre son segment d’ADN comportant quatre boîtes, l’anneau ne se contente pas de se poser sur l’hélice ; il se fléchit et se réorganise de sorte que quatre de ses sous‑unités s’alignent le long de l’ADN, chacune enveloppant une boîte dans le grand sillon.
Points de contact clés qui lisent le code de l’ADN
Les structures haute résolution ont révélé que chaque sous‑unité en contact avec l’ADN utilise trois chaînes latérales chargées positivement — points précis à la surface de la protéine — pour lire la séquence d’ADN. Ces « doigts » chimiques pénètrent dans le sillon de la double hélice et forment des liaisons hydrogène précises avec des paires de bases particulières dans les boîtes conservées. Lorsque les chercheurs ont modifié l’un quelconque de ces trois résidus, MraZ perdait en grande partie sa capacité à se lier à l’ADN et à réprimer le gène rapporteur testé. Des contacts supplémentaires avec l’épine dorsale de l’ADN contribuent à stabiliser le complexe mais sont moins spécifiques à la séquence. Ensemble, ces résultats montrent comment MraZ combine une tête de lecture hautement spécialisée à un corps multi‑sous‑unités flexible pour reconnaître sa région cible. 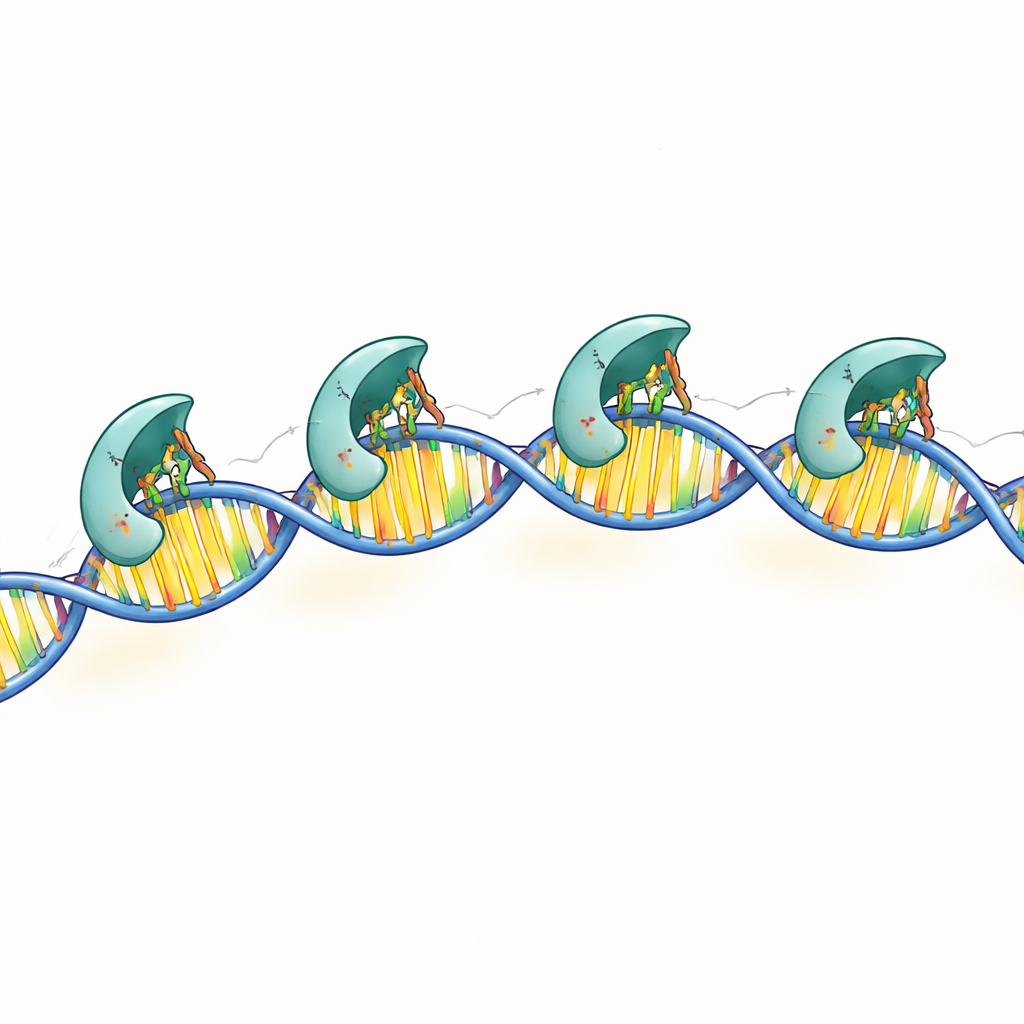
Des oligomères qui règlent l’intensité du contrôle
Parce que MraZ forme des anneaux et d’autres assemblages multi‑unités, l’équipe s’est demandé si ce regroupement était nécessaire pour la liaison à l’ADN ou se contentait de l’affiner. En concevant une version de MraZ incapable de s’assembler en anneaux, ils ont constaté que la protéine se liait encore à la séquence à quatre boîtes, mais avec une affinité réduite. Cette forme monomérique montrait particulièrement des difficultés lorsque l’espacement entre les boîtes était modifié, ce qui suggère que l’oligomère complet aide à relier et aligner des boîtes distantes, augmentant la concentration locale de motifs de liaison le long de l’ADN. Les auteurs proposent un modèle dynamique dans lequel MraZ bascule entre un anneau fermé et une forme ouverte engagée sur l’ADN, utilisant son état d’assemblage comme un réglage pour moduler la force avec laquelle il s’accroche au promoteur.
Ce que cela signifie pour les bactéries et au‑delà
En termes simples, ce travail explique comment une petite protéine dans une bactérie minimale saisit un motif répété sur l’ADN et l’utilise comme interrupteur maître pour les gènes de division cellulaire. La combinaison d’une tête de lecture en forme de berceau et d’un corps annulaire flexible permet à MraZ de reconnaître sa cible avec une grande précision tout en restant adaptable à différentes dispositions de l’ADN. Comme des protéines et des motifs d’ADN similaires apparaissent chez de nombreuses bactéries, le mécanisme mis au jour ici est probablement une stratégie partagée pour coordonner croissance et division. Les enseignements tirés de ce système épuré pourraient aider les chercheurs à concevoir des circuits génétiques simplifiés dans des cellules synthétiques et, à plus long terme, contribuer à de nouvelles façons de perturber la croissance bactérienne dans les maladies.
Citation: Sánchez-Alba, L., Varejão, N., Durand, A. et al. Structural basis for transcriptional regulation by the cell division regulator MraZ in Mycoplasma genitalium. Nat Commun 17, 2132 (2026). https://doi.org/10.1038/s41467-026-68809-2
Mots-clés: division cellulaire bactérienne, interaction ADN–protéine, régulation transcriptionnelle, cryo‑microscopie électronique, Mycoplasma genitalium