Clear Sky Science · fr
Une suppression courante de 19 pb dans un amplificateur d’APOE protège contre la maladie d’Alzheimer chez les Afro-Américains
Pourquoi cette découverte compte
La maladie d’Alzheimer vole des souvenirs et l’autonomie à des millions de personnes âgées, mais elle n’affecte pas tout le monde avec la même intensité. L’un des facteurs génétiques de risque les plus puissants connus, une version d’un gène appelé APOE, est particulièrement dangereuse chez les personnes d’ascendance européenne ou est-asiatique. Pourtant, les Afro-Américains portant cette même version à haut risque ne développent pas la maladie d’Alzheimer aussi souvent ni aussi tôt. Cet article met en lumière un petit segment d’ADN manquant qui aide à expliquer pourquoi — et ouvre des pistes pour dissocier le risque cérébral des problèmes cardiaques et du cholestérol.
Un gène à risque avec une exception intrigante
Les scientifiques savent depuis des décennies qu’une forme particulière du gène APOE, appelée epsilon‑4, augmente fortement les chances de développer la maladie d’Alzheimer à début tardif. Les personnes héritant de deux copies de cette version font face à certains des risques génétiques les plus élevés connus. Parallèlement, APOE participe aussi à la gestion des graisses et du cholestérol dans l’organisme, de sorte que les modifications de ce gène influencent à la fois la santé cérébrale et les lipides sanguins. Curieusement, les Afro-Américains et d’autres personnes d’ascendance africaine portant deux copies d’APOE‑ε4 ne présentent pas le même risque extrêmement élevé d’Alzheimer observé chez les personnes d’ascendance européenne, ce qui suggère que d’autres différences d’ADN voisines pourraient atténuer ce danger.
Découverte d’un tout petit morceau d’ADN manquant
Les chercheurs ont utilisé le séquençage du génome en lectures longues, une technologie qui lit de longues portions d’ADN d’un seul tenant, pour examiner la région autour d’APOE chez des personnes de divers horizons. Ils se sont concentrés sur les insertions et délétions — des endroits où de l’ADN est ajouté ou absent — plutôt que sur les changements d’une seule lettre déjà largement étudiés. Chez des personnes d’ascendance africaine, ils ont identifié une petite délétion de 19 paires de bases située juste au‑delà de la fin du gène APOE, à l’intérieur d’un élément régulateur lié par un facteur de transcription microglial appelé SPI1. Cette délétion est assez fréquente chez les Africains et les Afro‑Américains, souvent portée sur le même chromosome que APOE‑ε4, mais elle est presque absente chez les Européens. Ce profil en fait un candidat solide pour expliquer la différence de risque spécifique à l’ascendance.
Des preuves que la délétion protège le cerveau
Pour vérifier si cette minuscule délétion modifie le risque d’Alzheimer, l’équipe a analysé des données génétiques et cliniques provenant de milliers de participants afro‑américains du Alzheimer’s Disease Sequencing Project et du programme NIH All of Us. Après ajustement minutieux sur l’âge, le sexe, l’ascendance et le type d’APOE, ils ont constaté que les porteurs de la délétion avaient des chances réduites de développer la maladie d’Alzheimer par rapport aux non‑porteurs avec le même contexte APOE‑ε4. Parmi les personnes ayant deux copies d’APOE‑ε4 et une ascendance locale africaine dans cette région, celles porteuses de la délétion ont développé l’Alzheimer en moyenne environ trois ans plus tard que celles sans la délétion. Lorsque toutes les ascendances ont été regroupées, l’effet protecteur de cette petite délétion était comparable en intensité à celui de la variante protectrice bien connue APOE‑ε2.
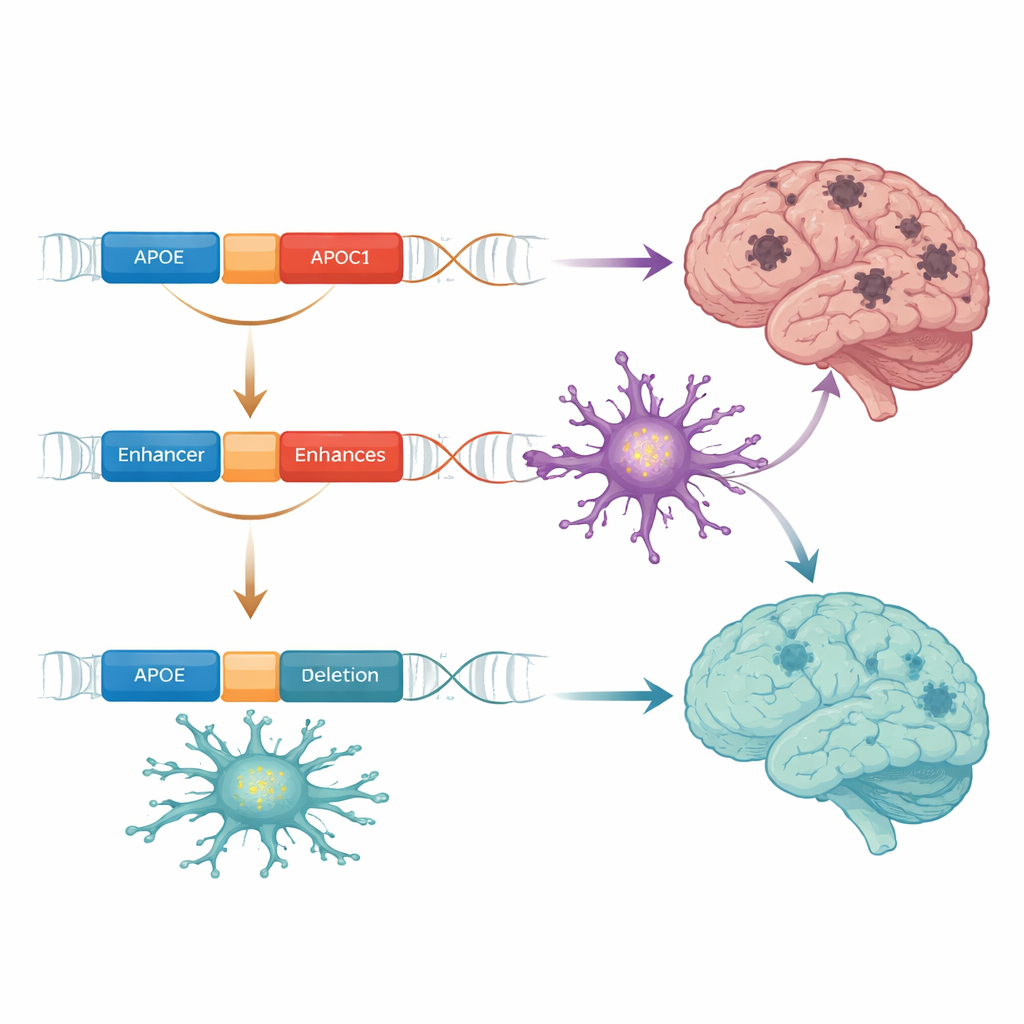
Comment la délétion peut modifier les cellules cérébrales et le cholestérol
Les scientifiques se sont ensuite demandé comment un segment d’ADN si petit pouvait avoir un tel impact. Ils ont inséré les séquences intactes et délétées dans des constructions rapporteurs et les ont introduites dans des cellules de type microglie cultivées en laboratoire. La séquence intacte, qui inclut le site de liaison de SPI1, agissait comme un frein sur l’activité génique voisine — réduisant l’expression d’un gène rapporteur lié. Quand le segment de 19 bases était absent, cette répression disparaissait. D’autres expériences ont montré qu’augmenter SPI1 dans ces cellules ne changeait pas directement les niveaux d’APOE, mais réduisait l’expression d’un gène voisin appelé APOC1 et modifiait un ARN long non codant s’étendant entre APOE et APOC1. La délétion semble donc reconfigurer la façon dont cet amplificateur communique avec APOC1 et, indirectement, avec APOE dans les microglies, les cellules immunitaires du cerveau qui participent à l’élimination des protéines toxiques.
Dissocier le risque cérébral du taux de lipides sanguins
Parce qu’APOE contrôle aussi les lipides sanguins, les chercheurs ont réalisé une étude d'association phénotypique étendue pour examiner comment les variantes d’APOE et la délétion influent sur des centaines de résultats de santé dans la cohorte All of Us. La variante à haut risque APOE‑ε4 augmentait à la fois le risque d’Alzheimer et les taux de cholestérol élevé et de lipides sanguins élevés, tandis que la variante APOE‑ε2 montrait le schéma inverse. En revanche, la délétion de 19 bases, une fois les effets du type APOE pris en compte, était associée à une protection contre l’Alzheimer et les démences apparentées mais avait peu d’effet indépendant sur les traits lipidiques. D’autres variantes dans la même région intergénique affichaient le schéma inverse — des effets marqués sur le cholestérol avec peu d’impact sur la maladie cérébrale. Ensemble, ces résultats suggèrent que l’ADN situé entre APOE et APOC1 peut découpler le risque neurologique des effets cardiovasculaires et lipidiques.
Ce que cela signifie pour les patients futurs
Concrètement, cette étude montre que certains Afro‑Américains portent une petite variation d’ADN naturellement présente qui atténue l’effet d’un des gènes de risque d’Alzheimer les plus dangereux. En affaiblissant un interrupteur répressif qui relie APOE à son voisin APOC1 dans les microglies, la délétion de 19 bases semble retarder ou réduire la maladie, même lorsqu’elle est portée sur un fond par ailleurs à haut risque APOE‑ε4. Comprendre ce mécanisme protecteur pourrait aider les chercheurs à concevoir des traitements qui en imitent l’effet — réduisant le risque d’Alzheimer sans aggraver les problèmes de cholestérol — et souligne l’importance d’inclure des populations diverses dans la recherche génétique pour identifier à la fois des variantes qui augmentent et qui réduisent le risque.
Citation: Brutman, J.N., Busald, T., Nizamis, E. et al. A common 19 bp APOE enhancer deletion is protective against Alzheimer’s disease in African Americans. Nat Commun 17, 2237 (2026). https://doi.org/10.1038/s41467-026-68808-3
Mots-clés: Maladie d’Alzheimer, gène APOE, ascendance africaine, protection génétique, microglie