Clear Sky Science · fr
Trajectoires cellulaires et transcriptionnelles de la spécification du destin neural chez l’anémone de mer révèlent deux modes de neurogenèse adulte
Comment une créature marine simple continue de produire de nouveaux neurones
La plupart des animaux, y compris les humains, produisent la majorité de leurs neurones tôt dans la vie puis cessent en grande partie. Pourtant, certains êtres apparemment simples, comme les anémones de mer, ajoutent continuellement de nouvelles cellules nerveuses à l’âge adulte. Cette étude explore comment l’anémone étoilée (Nematostella vectensis) renouvelle et remodèle en permanence son système nerveux diffus, révélant des stratégies qui pourraient refléter des solutions anciennes pour faire croître et réparer les tissus nerveux.
Un organisme qui grandit a besoin d’un réseau nerveux qui grandit
Les anémones de mer n’ont pas de cerveau ; elles possèdent à la place un réseau nerveux en toile réparti dans la paroi du corps. À mesure que ces animaux grandissent ou rétrécissent selon la disponibilité de la nourriture, leur réseau nerveux doit s’adapter en taille. En utilisant une protéine fluorescente sensible à la lumière comme horodatage, les auteurs ont marqué les neurones existants chez des jeunes adultes, puis observé l’apparition de cellules nouvellement nées au cours de la semaine suivante. Ils ont trouvé de nombreuses nouvelles cellules éparpillées le long de l’axe corporel, sans être confinées à une zone de croissance spécifique. Ces nouvelles cellules sont apparues tant du côté de la bouche que du côté opposé de l’animal, montrant que la neurogenèse adulte est spatialement étendue et continue.
Retracer l’origine des nouvelles cellules nerveuses
Pour déterminer d’où proviennent ces nouvelles cellules, les chercheurs ont combiné imagerie in vivo et séquençage ARN unicellulaire, une technique qui lit quels gènes sont actifs dans des milliers de cellules individuelles. Ils se sont concentrés sur des cellules portant des « reporters » fluorescents contrôlés par trois gènes clés : FoxL2, SoxC et Elav. FoxL2 marque un vaste pool de cellules progénitrices multipotentes en division ; SoxC s’active brièvement au début de la spécialisation ; et Elav est fortement actif dans les neurones peptidergiques, qui communiquent principalement via de petits peptides signal. L’équipe a montré qu’une population de progéniteurs FoxL2-positifs et Piwi1-positifs se comporte comme des cellules souches : elles s’auto-renouvellent tout en générant continuellement des descendants divers, y compris des neurones, des cellules urticantes appelées cnidocytes, et des cellules sécrétoires. En revanche, SoxC et Elav ne s’activent que lorsque les cellules quittent ce pool progéniteur et s’engagent vers des destins neuronaux particuliers.
Deux chemins différents vers les neurones adultes
En alignant le timing des reporters avec le profil d’expression génique de chaque cellule, l’étude a mis au jour deux voies distinctes menant aux cellules neuronales matures. Les neurones peptidergiques suivent une voie directe : ils proviennent de progéniteurs déjà porteurs d’un profil moléculaire « engagé peptidergique » puis se différencient rapidement en une variété de sous-types neuronaux. De nouveaux membres de chaque sous-type apparaissent en proportion de la fréquence de ce sous-type déjà présent, ce qui suggère que le système maintient un mélange équilibré de types neuronaux plutôt que de favoriser certains d’entre eux. Dans cette lignée, il n’y a pas de série claire d’étapes intermédiaires ; au lieu de cela, des sous-types neuronaux proches émergent en parallèle à partir de progéniteurs similaires et préconfigurés. 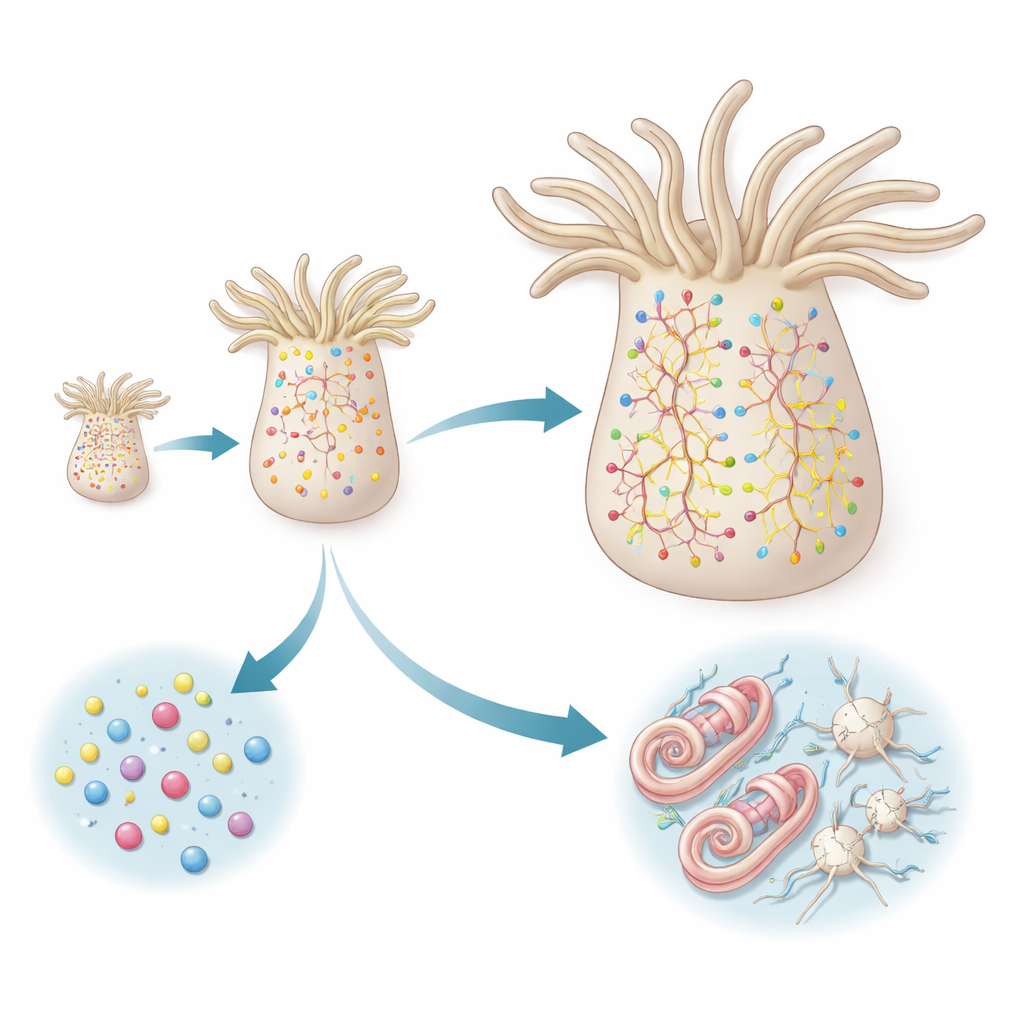
Le cas particulier des cellules urticantes
Les cnidocytes, les cellules urticantes propres aux cnidaires, empruntent une voie plus par étapes. Elles passent d’abord par une phase de « construction de capsule », durant laquelle elles fabriquent leurs organites sous pression caractéristiques capables de lancer un harpon microscopique. Cette étape repose sur un ensemble spécifique de gènes régulateurs et de protéines structurales en grande partie absent des autres types cellulaires. Ce n’est qu’après l’achèvement de ce programme intermédiaire que les cnidocytes activent un second programme plus conventionnel de type neural, ajoutant des canaux ioniques et d’autres composants nécessaires à la signalisation électrique. Des données génétiques issues de mutants bloquant la phase précoce renforcent ce modèle en deux phases : empêcher la transition empêche l’apparition des caractéristiques neuronales ultérieures. 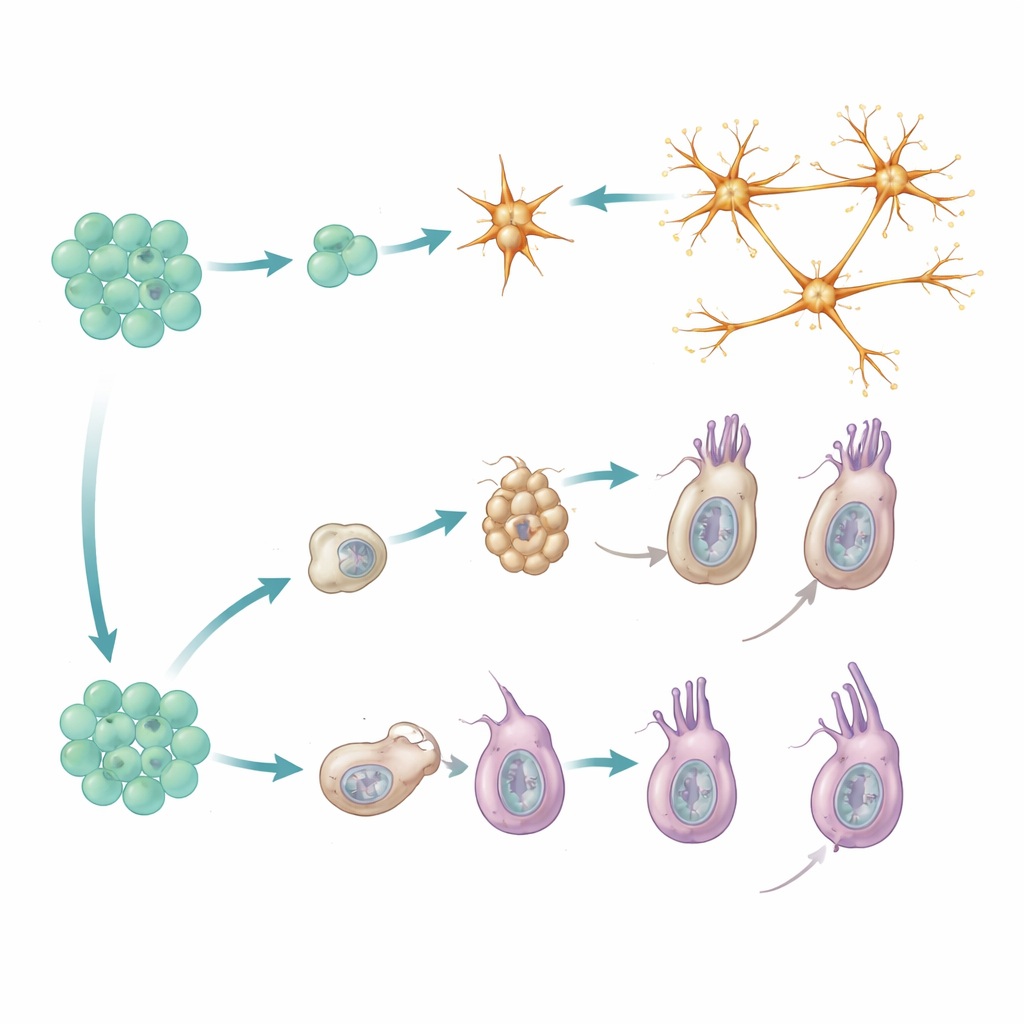
Règles partagées et racines anciennes
Malgré leurs trajectoires distinctes, les neurones peptidergiques et les cnidocytes s’appuient sur des familles de gènes régulateurs chevauchantes pour verrouiller leurs identités. Les caractéristiques neuronales larges sont associées à des facteurs de transcription bHLH et bZIP, tandis que l’identité fine de chaque sous-type neuronal est spécifiée par des combinaisons uniques de gènes à domaine homéodomaine et à doigts de zinc — un « code » rappelant la définition des types neuronaux chez des animaux plus complexes, y compris les vers et les vertébrés. Les auteurs soutiennent que ces stratégies modulaires — progéniteurs de type souches, activité transitoire de SoxC lors de l’engagement, et codes déterminant les sous-types basés sur des homéodomaines — pourraient représenter des principes profondément conservés de la neurogenèse. Chez l’anémone de mer, elles soutiennent le renouvellement à vie et l’ajustement du réseau nerveux ; chez d’autres animaux, des mécanismes apparentés pourraient sous-tendre à la fois une neurogenèse adulte limitée et les remarquables capacités régénératives observées dans certaines lignées.
Citation: Plessier, F., Marlow, H. Cellular and transcriptional trajectories of neural fate specification in sea anemone uncover two modes of adult neurogenesis. Nat Commun 17, 2611 (2026). https://doi.org/10.1038/s41467-026-68802-9
Mots-clés: neurogenèse adulte, anémone de mer, cellules progénitrices neurales, cnidocytes, transcriptomique unicellulaire