Clear Sky Science · fr
Livraison de coacervats peptidiques pour former des pôles d’interaction stables dans les cellules
Construire de nouvelles « stations de travail » à l’intérieur des cellules
Nos cellules regorgent de micro‑espaces où s’effectuent des tâches essentielles — comme la production d’énergie ou la réponse au stress. Avec le temps, ou en cas de maladie, ces stations de travail naturelles peuvent défaillir. Cette étude examine une méthode pour ajouter de nouveaux « pôles d’interaction » dans des cellules vivantes en utilisant de simples gouttelettes synthétiques élaborées à partir de peptides courts. Ces pôles artificiels peuvent capturer des protéines spécifiques, les concentrer, et même les aider à être détruites, ouvrant ainsi des pistes pour de futures thérapies et pour l’ingénierie cellulaire.
Pourquoi les cellules ont besoin d’espaces de travail sur mesure
Les cellules maintiennent l’ordre en séparant différentes tâches dans des compartiments distincts. Certains sont entourés de membranes, comme les mitochondries ; d’autres sont des structures plus souples et en forme de gouttelettes qui se forment lorsque certaines protéines et ARN se regroupent. Ces gouttelettes fluides, ou condensats, servent de centres réactionnels qui accélèrent ou arrêtent des voies biochimiques particulières. Les scientifiques ont déjà ingénieré de tels compartiments en forçant les cellules à produire des protéines échafaudage spéciales via des gènes insérés. Bien que puissant, ce procédé nécessite la délivrance de gènes et limite la quantité de matériau que la cellule peut produire. Les auteurs de cette étude ont choisi de contourner l’ADN et de fabriquer des compartiments prêts à l’emploi à l’extérieur de la cellule, puis de les délivrer directement sous forme de gouttelettes stables de l’ordre du micromètre.
Gouttelettes peptidiques qui forment des pôles stables
L’équipe a travaillé avec des peptides courts désordonnés connus sous le nom de HBpep et une variante redox‑sensible, HBpep‑SA. Dans des conditions légèrement acides, ces peptides restent dissous, mais lorsque le pH est ramené à des niveaux proches de la physiologie — ou quand la température baisse — ils se séparent en phase pour former des gouttelettes molles et gélifiées d’environ 1 à 5 micromètres. En ajustant la concentration en peptide, les chercheurs ont pu contrôler à la fois la taille et le nombre des gouttelettes. Par des techniques de fluorescence, ils ont montré que les molécules peptidiques à l’intérieur de ces gouttelettes se déplacent lentement, indiquant un état gélifié suffisamment robuste pour résister à la dilution et à la manipulation. Lorsqu’elles ont été ajoutées à des cultures de cellules cancéreuses humaines, de cellules de mélanome de souris et de cellules immunitaires humaines primaires, les gouttelettes ont été internalisées efficacement et se sont accumulées dans le cytoplasme. Les gouttelettes de plus grande taille, en particulier, sont restées intactes pendant au moins cinq jours, agissant effectivement comme des organites synthétiques de longue durée au sein de cellules vivantes.
Chargement et ciblage des pôles
Pour que ces pôles soient utiles, ils doivent contenir et organiser des protéines cargos. Les chercheurs ont d’abord amélioré le chargement en greffant une courte étiquette dérivée de HBpep à une protéine modèle, la GFP. Cette étiquette a favorisé le partitionnement fort de la GFP dans les gouttelettes et, fait intéressant, sa concentration près de leurs surfaces, générant une organisation cœur‑coquille. Ensuite, ils ont incorporé des nanocorps — des protéines compactes de type anticorps qui se lient fortement à des cibles choisies — à l’intérieur des gouttelettes. Un nanocorps fixant la GFP a permis aux pôles de capturer sélectivement la GFP tant en tube à essai qu’à l’intérieur des cellules. Parce que le gel peptidique est relativement dense, la majeure partie de la GFP capturée s’est initialement accumulée à la surface de la gouttelette. Mais lorsque la structure interne a été partiellement assouplie, soit en modifiant l’état redox soit en aidant les gouttelettes à échapper à leurs membranes endosomales environnantes, la GFP a aussi commencé à pénétrer l’intérieur. En cellules, des agents chimiques favorisant l’échappement endosomal ont considérablement augmenté la fraction de pôles recrutant avec succès leurs cibles.
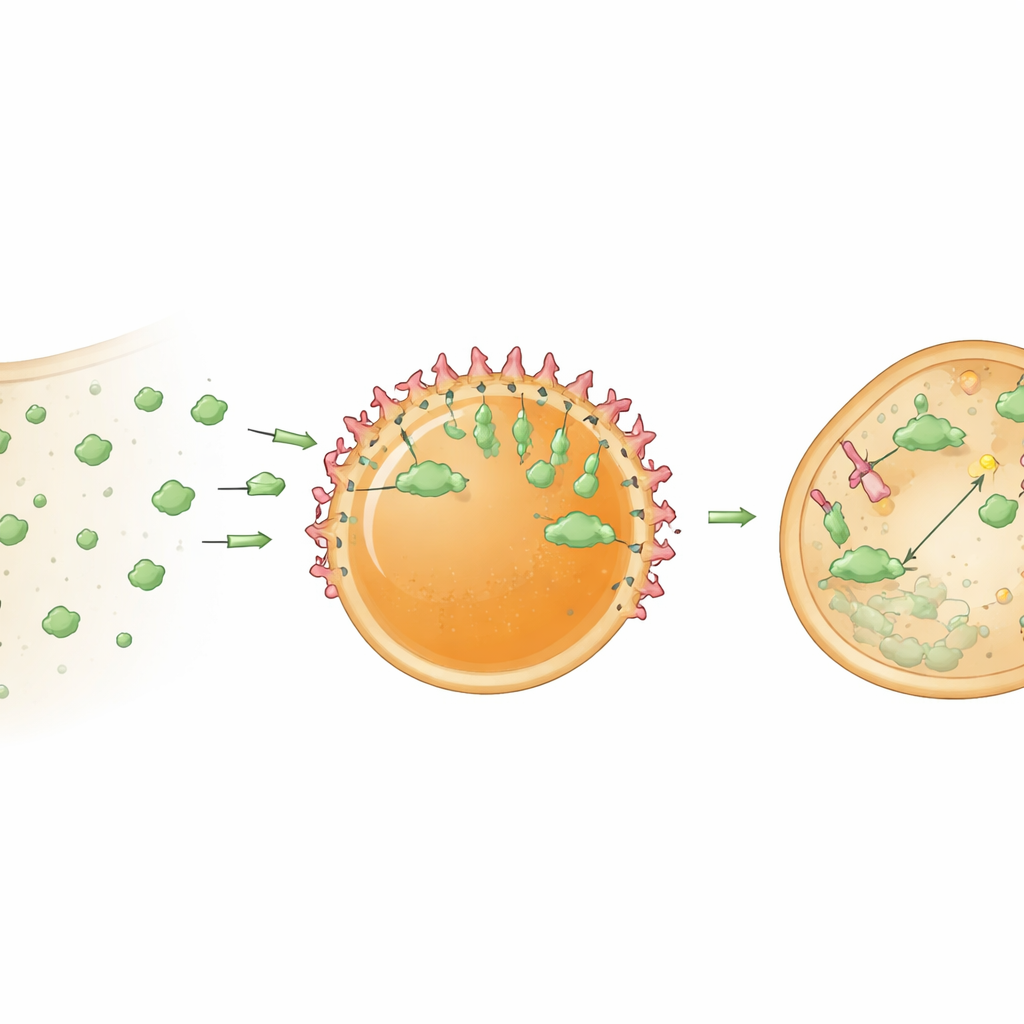
Transformer les pôles en broyeurs de protéines
Les auteurs ont ensuite fait évoluer ces pôles de pièges passifs à centres de traitement actifs. Ils ont chargé les gouttelettes avec un bioPROTAC — une protéine de fusion qui combine un nanocorps fixant la cible avec une partie d’un adaptateur enzymatique qui marque les protéines pour destruction par les machines d’élimination cellulaires. Lorsque ces gouttelettes « dégradosomes » ont été délivrées dans des cellules exprimant de manière stable la GFP, le niveau de GFP cytosolique a chuté d’environ 78 % en une journée. Des pôles‑contrôle contenant seulement le nanocorps séquestraient la GFP mais n’en diminuaient pas sensiblement le niveau global, confirmant que la forte baisse provenait d’une dégradation ciblée plutôt que d’une simple capture. Ces résultats suggèrent que le regroupement de bioPROTACs dans un micro‑environnement concentré les rend bien plus efficaces que lorsqu’ils sont dispersés librement dans le cytoplasme.
Ce que cela pourrait signifier pour les thérapies futures
En termes simples, ce travail montre que l’on peut fabriquer des gouttelettes peptidiques en éprouvette, les charger avec des outils protéiques sur mesure, puis les délivrer dans des cellules vivantes où elles se comportent comme de nouveaux organites durables. Ces pôles synthétiques peuvent attirer sélectivement des protéines naturelles et, lorsqu’ils sont équipés d’un dispositif de dégradation, éliminer activement des cibles choisies de la cellule. Parce que cette plateforme évite de modifier le génome cellulaire et est modulaire quant à sa charge utile, elle ouvre la voie à des thérapies visant à restaurer ou réécrire le comportement cellulaire — par exemple en éliminant des protéines nocives ou en réorientant des voies de signalisation défaillantes — en installant simplement de nouvelles « stations de travail » programmables dans nos cellules.
Citation: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Mots-clés: organites synthétiques, coacervats peptidiques, livraison intracellulaire, dégradation des protéines, ingénierie cellulaire