Clear Sky Science · fr
Un système de défense bactérien ciblant la cytosine modifiée de l’ADN génomique des phages
Comment les bactéries déjouent les virus envahisseurs
Les virus qui infectent les bactéries, appelés phages, sont engagés dans une course aux armements permanente avec leurs hôtes microbiennes. Beaucoup de ces phages réécrivent les lettres chimiques de leur ADN pour échapper aux défenses bactériennes. Cette étude révèle une contre-mesure bactérienne jusque-là cachée : un système protéique nommé CMoRE capable de repérer et de détruire l’ADN des phages portant ces modifications chimiques particulières. Au-delà d’un nouvel épisode dans la guerre microbe–virus, CMoRE pourrait devenir un outil précis pour détecter de subtils marquages de l’ADN associés à des maladies humaines.
Une étiquette cachée sur les lettres de l’ADN
Tant les phages que les animaux modifient parfois la lettre d’ADN cytosine en y ajoutant de petits groupes chimiques. Chez de nombreux phages de type T, y compris le classique T4 qui infecte E. coli, la cytosine est remplacée par une version modifiée appelée 5-hydroxyméthylcytosine (5hmC), qui peut ensuite être décorée pour former la 5-glucosyl-hydroxyméthylcytosine (5ghmC). Ces modifications aident les phages à contourner les défenses bactériennes courantes qui coupent normalement l’ADN « étranger » non modifié tout en épargnant le génome de la bactérie. Chez les mammifères, une marque apparentée, la 5hmC, est désormais considérée comme un signal épigénétique clé impliqué dans le contrôle des gènes, la fonction cérébrale et les cancers — mais elle est très rare et difficile à mesurer avec précision.
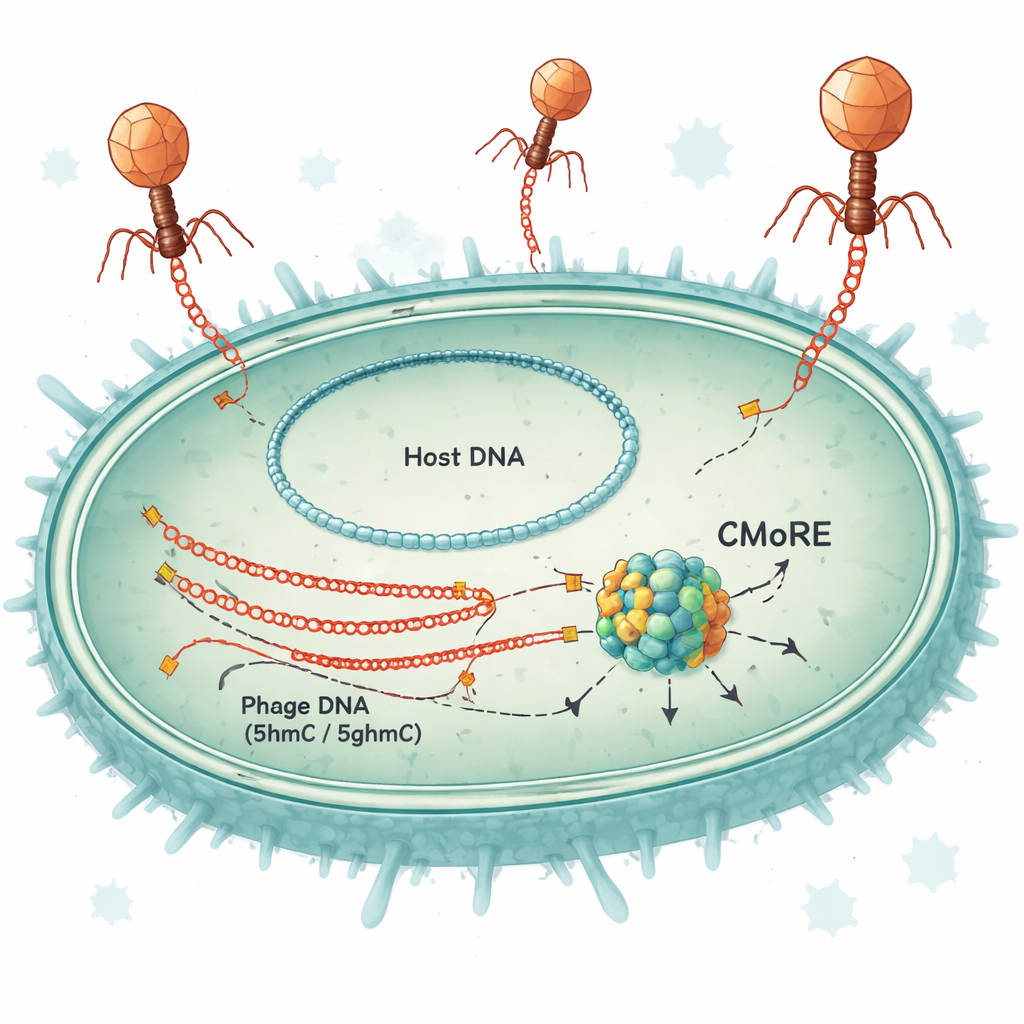
Un système de sécurité monoprotiéique
Les chercheurs ont étudié un gène de défense initialement trouvé dans certaines souches d’E. coli et de bactéries apparentées. Lorsqu’ils ont inséré ce gène — désormais renommé CMoRE — dans des souches de laboratoire qui en sont normalement dépourvues, les bactéries sont devenues presque complètement résistantes à plusieurs phages de type T, dont T2, T4 et T6. Lors d’attaques virales intenses, les cellules portant CMoRE ont continué à croître, montrant que le système protège sans sacrifier l’hôte par une réponse « suicidaire ». Des tests en culture liquide et sur gélose ont montré que l’infection par le phage chutait jusqu’à environ cent mille fois, tandis que les bactéries sans CMoRE restaient vulnérables.
Ciblage précis de l’ADN viral modifié
Pour savoir ce que CMoRE coupe réellement, l’équipe a purifié la protéine et l’a exposée à de l’ADN de différents phages et de bactéries. CMoRE a découpé sélectivement l’ADN des phages de type T mais a laissé l’ADN bactérien essentiellement intact. Lorsqu’ils ont fabriqué des fragments d’ADN tests contenant différentes versions de la cytosine, CMoRE a ignoré la cytosine normale et une forme methylée courante (5mC), mais a dégradé efficacement l’ADN contenant de la 5hmC ou de la 5ghmC. Un phage T4 mutant dont le génome utilisait la cytosine non modifiée est devenu complètement résistant à la défense, confirmant que c’est la modification chimique — et non une séquence particulière — que reconnaît CMoRE. Le séquençage des fragments d’ADN après clivage a montré que CMoRE agit comme une enzyme de restriction : il lie deux cytosines modifiées avec un espacement caractéristique et effectue des coupures nettes produisant de courts surplombs aux extrémités de l’ADN.
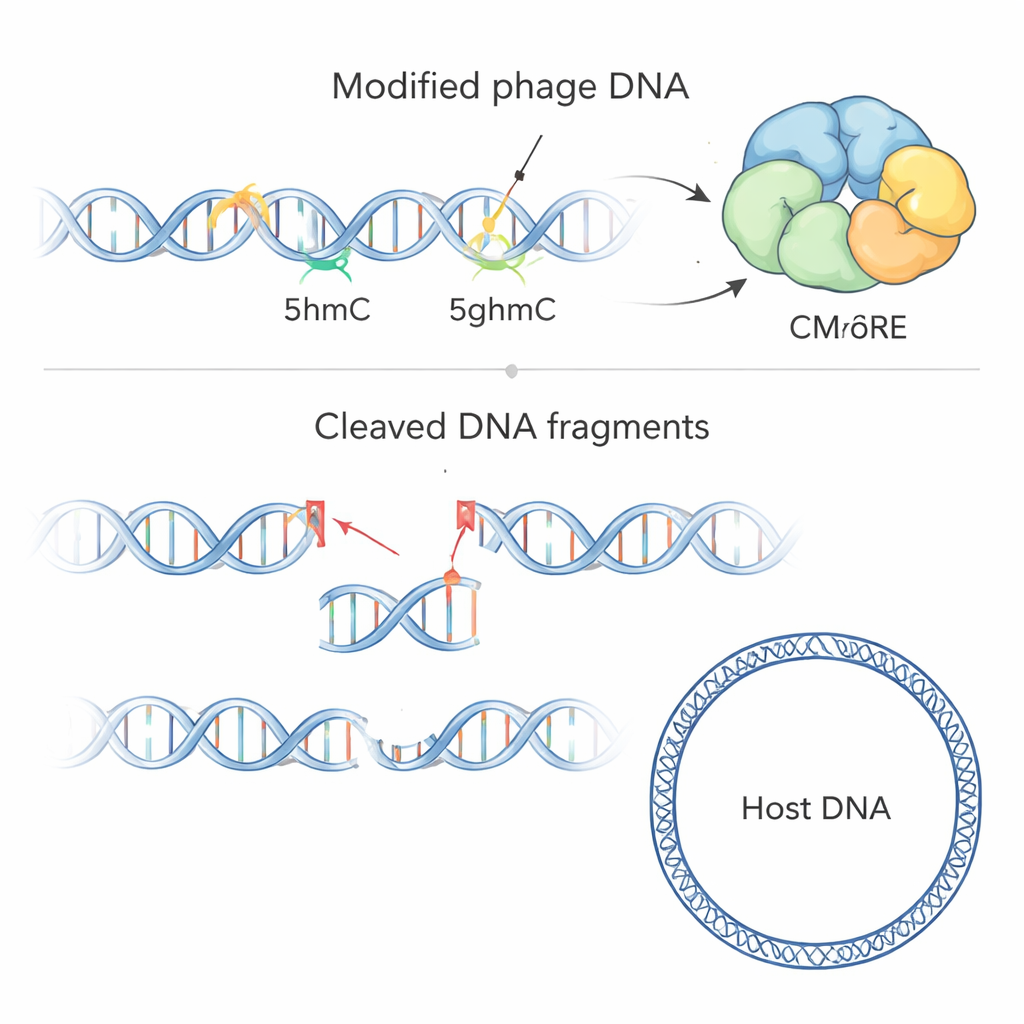
La structure et le verrou de sécurité de CMoRE
À l’aide de cristallographie aux rayons X, les auteurs ont résolu des structures haute résolution de CMoRE issues de deux espèces bactériennes. La protéine est composée de deux parties reliées : une extrémité N-terminale en « lame » qui effectue la coupure de l’ADN, appartenant à la famille des nucléases GIY-YIG, et une extrémité C-terminale « capteur » qui saisit la cytosine modifiée. Quatre copies de CMoRE s’assemblent pour former un tétramère compact, et perturber cet assemblage supprime en grande partie l’activité antivirale. Le domaine de coupe porte un motif distinctif « GIYxY–YIG » et une boucle inhabituelle riche en charges négatives qui surplombe le site actif comme un couvercle. Lorsque les chercheurs ont neutralisé cette boucle, CMoRE est devenu hyperactif, a commencé à attaquer l’ADN bactérien normal et a ralenti la croissance cellulaire — preuves que la boucle fait office de dispositif de sécurité intégré, aidant la protéine à discriminer fortement en faveur de l’ADN phagique marqué par la 5hmC ou la 5ghmC.
De la guerre microbienne aux outils médicaux
En analysant des milliers de génomes microbiens, l’équipe a trouvé des centaines de systèmes CMoRE apparentés dispersés dans de nombreux groupes bactériens, partageant tous les mêmes caractéristiques clés : la tyrosine supplémentaire dans le motif catalytique et la boucle de sécurité chargée négativement. Cela suggère que CMoRE est une stratégie largement utilisée dans la lutte bactérienne contre les phages chimiquement déguisés. Parce que CMoRE peut distinguer proprement la 5hmC et la 5ghmC de la 5mC presque identique, et parce que la protéine est stable et facile à manipuler en laboratoire, elle pourrait aussi servir de « scalpel moléculaire » hautement sélectif pour cartographier la 5hmC dans les génomes de mammifères. Cela pourrait améliorer les outils de détection des altérations épigénétiques liées aux maladies, offrant un bénéfice pratique découlant de la compréhension de la façon dont les bactéries survivent face à leurs ennemis microscopiques.
Citation: Liu, R., Tang, D., Niu, M. et al. A bacterial defense system targeting modified cytosine of phage genomic DNA. Nat Commun 17, 1920 (2026). https://doi.org/10.1038/s41467-026-68792-8
Mots-clés: défense contre les bactériophages, modification de l’ADN, 5-hydroxyméthylcytosine, enzyme de restriction, épigénétique